
题目列表(包括答案和解析)
1.美国劳仑斯国家实验室曾在1999年宣布用86Kr离子轰击208Pb靶得到118号元素的一种原子,其质量数为293。其后,反复实验均未能重现118号元素的信号,因此该实验室在2001年8月宣布收回该论文。但是科学家们相信,完成的第七周期包含的元素数目与第六周期相同。若118号元素将来被确认,则下列预测合理的是( )
A.它的中子数是118 B.它是第八周期元素
C.它是活泼的金属元素 D.它的最外层电子数是8
26、(10分)今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份各100mL溶液进行如下实验:
第一份加入AgNO3溶液有沉淀产生。
第二份加足量NaOH溶液加热后,收集到0.08 mol气体。
第三份加足量BaCl2溶液后,得到干燥沉淀12.54 g,经足量盐酸洗涤、干燥后,沉淀质量为4.66 g.。
根据上述实验,回答以下问题:
(1) 由第一份进行的实验推断该混合物是否一定含有Cl-
(2) 由第二份进行的实验得知混合物中应含有 离子,其物质的
量浓度为
(3) 由第三份进行的实验可知12.54g沉淀的成分为
请计算形成该沉淀的原混合物中各离子的物质的量。(要求写出计算过程)
(4) 综合上述实验,你认为以下结论正确的是
A. 该混合液中一定含有:K+、NH4+、CO32-、SO42-,可能含Cl-,且n(K+) ≥0.04mol
B. 该混合液中一定含有:NH4+、CO32-、SO42-,可能含K+、Cl-
C. 该混合液中一定含有:NH4+、CO32-、SO42-,可能含Mg2+、K+、Cl-
D. 该混合液中一定含有:NH4+、SO42-,可能含Mg2+、K+、Cl-
2009--2010学年度第二学期期末高一年级调查测试
25、(6分)已知有以下物质相互转化。试回答:

(1)写出B的化学式 ,D的化学式 。
(2)写出由E转变成F的化学方程式 。
(3)写出向G溶液加入A的有关离子反应方程式 。
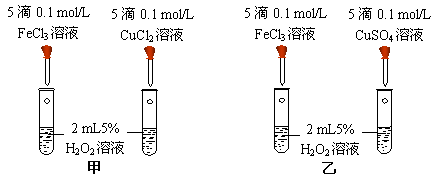
24、(共15分)I(8分) (1)(4分)为比较Fe3+ 和Cu2+ 对H2O2分解的催化效果,甲、乙两位同学分别设计了如图所示的实验。
甲、乙两同学可通过观察 ,定性比较得出结
论。观察两同学的方案,你认为 (填“甲”或“乙”)更合理。 理由
是 。
(2) (4分)丙同学另外设计了如下实验验证过氧化氢酶对H2O2分解的作用(新鲜鸡肝片中含有过氧化氢酶):
①在试管A中加入3%的双氧水5 mL,再加入新鲜的鸡肝片1 g,有气体产生;
②在试管B中加入3%的双氧水5 mL,再加入煮熟的鸡肝片1 g,无气体产生;
③在试管C中加入3%的双氧水3 mL和10%的H2SO42 mL,再加入新鲜的鸡肝片1 g,无气体产生。
由上述实验得到的结论是
_______________________________________________________________________,
_______________________________________________________________________。
写出①中产生气体的化学方程式:_____________________________________。
II(7分)利用含淀粉的物质可以生产醋酸。下面是生产醋酸的流程,根据流程回答下列问题:

B是日常生活中有特殊香味的常见有机物,在有些饮料中含有B。
(1)写出化学方程式,并注明反应类型:
①B与醋酸反应:_____________________________________,_________________反应。
②B→C:___________________________________________,_________________反应。
(2)可用于检验A的试剂是_________________________________________。
23、对于某些离子的检验及结论一定正确的是
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32-
B.加入氯化钡溶液有白色沉淀产生,再加入盐酸,沉淀不消失,一定有SO42-
C.加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NH4+
D.加入碳酸钠溶液产生白色沉淀,再加入盐酸白色沉淀消失,一定有Ba2+
22、X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是
A.X的气态氢化物比Y的稳定
 B.W的最高价氧化物对应水化物的酸性比Z的强
B.W的最高价氧化物对应水化物的酸性比Z的强
C.Z的非金属性比Y的强
D.X与Y形成的化合物都易溶于水
21、下列溶液中的Cl-浓度与50 mL 1 mol ·L-1 MgCl2溶液中的Cl-浓度相等的是
A. 150 mL 1 mol·L-1 NaCl溶液 B. 75 mL 0.5mol·L-1 CaCl2溶液
C. 150 mL 2 mol·L-1 KCl溶液 D. 75 mL 1 mol ·L-1 AlCl3溶液
20、用 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
A. 中含有的原子数为
中含有的原子数为
B.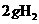 中含有的氢原子数为2
中含有的氢原子数为2
C.常温常压下,11.2L 中含有的分子数为0.5
中含有的分子数为0.5
D.1L0.1mol·L-1NaNO3溶液中含有的钠离子数为
19、下列物质不属于天然高分子化合物的是
A.淀粉 B.蚕丝 C.葡萄糖 D.纤维素
18、对于反应中的能量变化,表述正确的是
A.放热反应中,反应物的总能量大于生成物的总能量
B.断开化学键的过程会放出能量
C.加热才能发生的反应一定是吸热反应
D.氧化反应均为吸热反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com