
题目列表(包括答案和解析)
3.下列反应是吸热反应的是
A.液态水汽化 B. Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
C.铝和盐酸的反应 D. 灼热的炭与氧气反应
2. 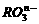 共有
共有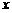 个核外电子,R的质量数为A,R的中子数是
个核外电子,R的质量数为A,R的中子数是
A. 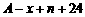 B.
B. 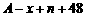
C. 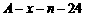 D.
D. 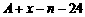
1. “保护环境,就是保护人类自己”。目前,在我国城市环境中主要的大气污染物是
A. 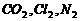 ,酸雨
B.
,酸雨
B. 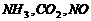 ,雾
,雾
C. HCl,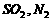 ,粉尘
D.
,粉尘
D. 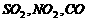 ,烟尘
,烟尘
29.(10分)将Cu与CuO的混合物75.2 g加人到100 mL 18.4 mol/L的浓H2SO4中,加热,固体完全溶解。反应液冷却后稀释至500 mL,测得c(H+)=1.2 mol/L。试计算:
(1)上述反应剩余硫酸的物质的量为 mol。
(2)反应过程中放出的气体在标准状况下的体积(不考虑气体在溶液中的溶解)为 L。
(3)向500 mL溶液中逐滴加入4 mol/L的NaOH溶液,当Cu2+刚好沉淀完全时,所加NaOH溶液的体积是 L。
巴中市四县中2009-2010学年度高一年级下学期期末联考
27. (15分)
短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和具有臭鸡蛋气味的气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F。溶液F在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。
请回答下列问题:
(1)组成单质A的元素位于周期表中第 周期,第 族。
(2)B的氧化物与氢氧化钠溶液反应的离子方程式为:
。
(3)G与氯酸钠(NaClO3)在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物为
,当生成2 二氧化氯时,转移电子
二氧化氯时,转移电子
 。
。
(4)溶液F在空气中长期放置生成H的化学反应方程式为:
。
(5)H的溶液与稀硫酸反应产生的现象为 。
28(12分)
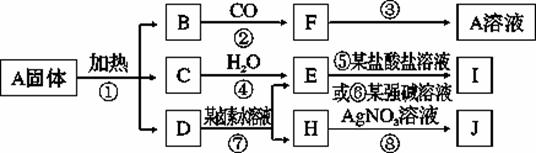 A是一种盐,其水溶液呈浅绿色,它能发生下列转化(某些次要的生成物已略去)。其中B是F的氧化物,B中氧的质量分数为30%,C在标准状况下为固体,D在常温下为气体,I是不溶于稀盐酸的白色沉淀,J是不溶于稀硝酸的浅黄色沉淀。
A是一种盐,其水溶液呈浅绿色,它能发生下列转化(某些次要的生成物已略去)。其中B是F的氧化物,B中氧的质量分数为30%,C在标准状况下为固体,D在常温下为气体,I是不溶于稀盐酸的白色沉淀,J是不溶于稀硝酸的浅黄色沉淀。
请回答:
(1)写出J、I的化学式:J ,I
(2)写出反应①的化学方程式:
(3)写出D转化为C的化学方程式:
(4)写出本题中某盐酸盐的名称为
(5)写出反应⑦的离子方程式:
26.(9分)
根据下图所示实验回答下列问题:

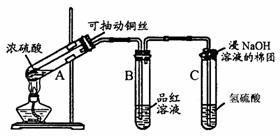
 (1)试管C口部的棉团上发生反应的离子方程式是
。
(1)试管C口部的棉团上发生反应的离子方程式是
。
 (2)试管B中的实验现象是
,若将该试管中反应后的溶液加热,可以观察
(2)试管B中的实验现象是
,若将该试管中反应后的溶液加热,可以观察 到
。试管C中溶液变浑浊,则证明SO2具有
性。
到
。试管C中溶液变浑浊,则证明SO2具有
性。
 (3)试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是
,如果浸NaHCO3溶液,则发生反应的化学方程式是 。
(3)试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是
,如果浸NaHCO3溶液,则发生反应的化学方程式是 。
25.(14分)
X、Y、Q、R、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中Y与Q、R与F为同一周期,X与R、Q与F分别为同一主族,Q元素的原子最外层电子数是次外层电子数的三倍,R是所在同周期原子半径最大的元素(0族除外)。又知六种元素所形成的常见单质在常温常压下有三种是气体、三种是固体。请回答下列问题:
(1)在前人探索的基础上,1869年,俄国化学家 (填名字)发现了元素周期律,并编制了第一个元素周期表。
(2)X、Q两元素可以组成A、B两种化合物,A在一定条件下可以分解为B。
①A的分子结构中含有 键和 键(填“极性”或“非极性”)。
②用电子式表示B的形成过程
(3)E是非金属元素,其单质在电子工业中有重要应用。请写出工业生产单质E的化学方程式:
该反应中氧化剂与还原剂的质量比为
(4)已知碳元素能与元素Q形成化合物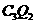 ,
, 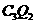 是无色有刺激性气味的气体,且是金星大气层的组成成份,
是无色有刺激性气味的气体,且是金星大气层的组成成份,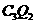 分子中各原子都满足8电子结构,则
分子中各原子都满足8电子结构,则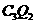 的电子式为
。
的电子式为
。
(5)由X、Q、R、F四种元素可形成两种中学常见化合物,写出它们在水溶液中加热时反应的离子方程式
24、若Na2S、Na2SO3、Na2SO4混合物中氧元素的质量分数为a%,则硫元素的质量分数为
A.a%
B.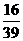 (1 - a)% C.
(1 - a)% C.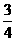 a%
D.
a%
D.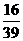 (100 - a)%
(100 - a)%
第I卷答题框(每小题2分,共48分)
|
期末联考试卷
第II卷(非选择题 共60分)
23. 在含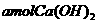 的石灰水中,缓缓地通入
的石灰水中,缓缓地通入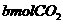 气体,实验过程中开始白色沉淀逐渐增多,后又部分消失,如果
气体,实验过程中开始白色沉淀逐渐增多,后又部分消失,如果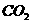 被充分吸收,则最后得到的白色沉淀的质量是
被充分吸收,则最后得到的白色沉淀的质量是
A. 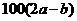 B.
B. 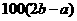 C.
C. 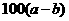 D.
D. 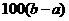
22. 银器饰品放置时间过久表面易变黑,为使饰品光亮无瑕可用双氧水清洗,其反应为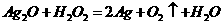 。如果过氧化氢中的氧原子为
。如果过氧化氢中的氧原子为 ,当反应完成后,含有
,当反应完成后,含有 的物质是
的物质是
A.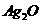 B.
B.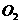 C.
C. 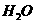 D.
D. 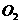 和
和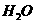
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com