
题目列表(包括答案和解析)
2.下列说法正确的是
A.42He原子核内含有4个质子
B.32He和42He互为同位素
C.32He原子核内含有2个中子
D.42He的最外层电子数为2,所以42He具有较强的金属性
1.目前我国许多城市和地区定期公布空气质量报告,在空气质量报告中,一般不涉及
A.SO2 B.NO2
C. CO2 D.可吸入颗粒物
34.Ⅰ.恒温、恒压下,在一个可变容积的容器中发生如下反应:
A(g)+B(g)
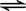 C(g)
C(g)
(1) 若开始时放入1 mol A和1 molB,到达平衡后,生成a molC,这时A的物质的量为 mol.
(2) 若开始时放入3 mol A和3 molB,到达平衡后,生成C的物质的量为 mol.
(3) 若开始时放入x molA、 2mol B和1mol C,到达平衡后,A和C的物质的量分别是y mol 和3a mol,则x= , y= .
平衡时,B的物质的量 (选填一个编号)。
(甲)大于2 mol
(乙)等于2 mol
(丙)小于2 mol
(丁)可能大于、等于或小于2 mol
作出此判断的理由是
(4) 若在(3)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是 。
Ⅱ.若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应。
(5)开始时放入1molA 和1molB 到达平衡后生成 b mol C。将b与(1)小题中的a进行比较 (选填一个编号)。
(甲)a<b
(乙)a>b
(丙)a=b
(丁)不能比较a和b的大小
作出此判断的理由是 。
33. 已知:①A、B、C、D四种物质均含元素X,有的还可能含有元素Y、Z。元素Y、X、Z的原子序数依次递增。
②X在A、B、C、D中都不呈现它的最高化合价。
③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。
④化合物D受热催化分解,可制得元素Y的单质。
(1)元素X是 ,Z是 。
(2)写出③中反应的化学方程式: 。
(3)写出④中反应的化学方程式: 。
32.(6分)在一密闭的1L的容器里装有4mol SO2和2mol O2,在一定条件下开始反应。2min末测得容器中有3.6mol SO2,试计算:
(1)2min末SO3的浓度。 (2)2min内SO2的平均反应速率。
(3)O2的转化率。
附加题:(每小题10分,共20分)
30.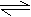 (6分)在2L密闭容器中发生3X(g)+Y(g)
Z (g)+2W(g)反应,现在控制下列三种不同的条件:
(6分)在2L密闭容器中发生3X(g)+Y(g)
Z (g)+2W(g)反应,现在控制下列三种不同的条件:
①在400°C时,9mol X 与3mol Y 反应
②在400°C时,15 mol X 与5mol Y 反应
③在300°C 时,9mol X 与3mol Y 反应
那么,(1)反应开始时,正反应速率最大的是(填序号,下同) ,正反应速率最小的是 ;
(2)在①条件下的反应进行到第10min时,测得Z为1mol,此时v(Z)=_______mol/(L·min);v(X)=_______mol/(L·min);
31(8分)、元素X、Y、Z、G均为短周期元素,其中元素X和Y位于同一周期,G和Y位于同一主族。Y是地壳中含量最多元素,在一定条件下,X和Y能直接化合生成无色气体XY2,Z和G能直接化合生成离子化合物Z2G,且它们的离子相差一个电子层,根据上述条件推断回答:
(1)元素X位于周期表第 周期 族
(2)元素Y的原子结构示意图
(3)用电子式分别表示化合物XY2和Z2G: XY2 Z2G
29. (6分)利用Cu + 2FeCl3 = CuCl2 + 2FeCl2反应,设计一个原电池,画出实验装置简图,写出电极反应式
28、(12分)下表为元素周期表的一部分。
 族周期 族周期 |
ⅠA |
ⅡB |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
一 |
(1) |
|
|||||
|
二 |
(2) |
|
|
(3) |
(4) |
(5) |
(6) |
|
三 |
(7) |
(8) |
(9) |
|
|
(10) |
(11) |
|
四 |
(12) |
|
|
|
|
|
(13) |
(注意:全部用元素符号或化学式表达)
(1)表中元素______的金属性最强;元素______的单质室温下呈液态;
(2)表中元素(6)(11)(13)氢化物的稳定性顺序:______ >______ >______;
(3)表中元素(10)和(11)最高价氧化物对应水化物的酸性:_______>________。
(4)表中元素(5)(6)(7)离子半径由大到小的顺序:______ >______ >______
(5)用电子式表示元素(1)和(6)的化合物形成过程:____________________________________。
27.(4分)下列各项分别与哪个影响化学反应速率的因素的关系最为密切?
(1)硫在氧气中比在空气中燃烧剧烈______________
(2) MnO2加入双氧水中反应更剧烈______________
(3)铁片和铁粉与足量的同浓度的盐酸反应,后者反应快____________
(4)镁粉在冷水中反应仅有微量气泡,但加热时则有大量气泡____________
26.(8分)由以下一些微粒:136C、3919K、4020Ca、126C、147N、4018Ar。
其中:(1)互为同位素的是________和________;
(2)质量数相等,但不能互称同位素的是_________和__________;
(3)中子数相等,但质子数不相等的是______和_____、______和_______
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com