
题目列表(包括答案和解析)
4、氯的原子序数为17,35Cl是氯的一种同位素,下列说法正确的是
A.35Cl原子所含质子数为18
B.1/18mol的1H35Cl分子所含中子数约为6.02×1023
C.3.5g35Cl2气体的体积约为22.4L
D.35Cl2气体的摩尔质量为71g.mol-1
3、下列表示物质结构的化学用语或模型图正确的是:
A.HClO的结构式:H-O-Cl
B.H2O2的电子式: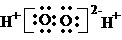
C.CO2的比例模型: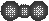 D.14C的原子结构示意图:
D.14C的原子结构示意图: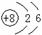
2、为了更好的解决能源问题,人们一方面研究如何提高燃料的燃烧效率,另一方面寻找新能源。以下做法不能提高燃料效率的是
A 将煤转化成煤气 B 液体燃料呈雾状喷出
C 通入大大过量的空气 D 将煤粉粉碎
1、下列关于化学观或化学研究方法的叙述中,错误的是
A.在化工生产中应遵循“绿色化学”的思想
B.在过渡元素中寻找优良的催化剂
C.在元素周期表的金属和非金属分界线附近寻找半导体材料
D.根据元素周期律,由HClO4可以类推出氟元索也存在最高价氧化物的水化物HFO4
30.(6分)取标准状况下2.24L某气态烃A置于密闭容器中,再通入足量的O2,用电火花引燃,燃烧产物的定量测定实验数据如下(图中的箭头表示气体的流向)。

试通过计算回答:
(1)烃A的分子式为 。
(2)写出烃A的所有同分异构体的结构简式: 。
(3)某有机物B仅含碳、氢、氧三种元素,其相对分子质量大于100,小于106。已知A、B分子中所含的氢原子数相同,则B的分子式为 。
29.(17分)已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
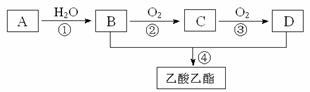
回答下列问题:
(1)A的结构式为 。
(2)写出下列反应的反应类型:① ,② ,④ 。
(3)B、D分子中的官能团名称分别是 、 。
(4)除去乙酸乙酯中所混有少量的D杂质,所需试剂的名称是: 。
(5)写出下列反应的化学方程式:(注明反应条件)
① ;
② ;
④ 。
(6)若184gB和120gD反应能生成106gE,计算该反应的产率为 。
(7)判定B能否直接被氧化为D,若能,指出所用的氧化剂是什么 (若不能,此空不填);若不能请说明理由 (若能,此空不填)。
28.(9分)A、B、C、D四种短周期元素,A、B同主族,C、D同周期。气体A2与气体C2按体积比2:1混和后点燃能够发生爆炸,且产物在常温常压下是一种无色无味的液体。B的阳离子与C的阴离子的核外电子排布相同。D能形成自然界硬度最大的单质。请根据上述所提供的信息回答下列问题。
⑴ 写出A、B、C三种元素的名称:A ;B ;C ;D在周期表中的位置是 。
⑵ 写出化合物B2C2的电子式 。
⑶ 写出B2C2和A2C反应的离子方程式: 。
⑷ 用电子式表示A2C形成的过程: 。
27. (14分)(1)如右图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)_________
______。
(14分)(1)如右图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)_________
______。
(2)乙烷中含有乙烯除杂试剂为 ;
反应的化学方程式为 。
(3)在10L密闭容器中充入2molA和1molB,发生的化学反应:3A(g)+B(g)  C(g)
C(g)
+2D(g),2min后反应达到平衡,在相同温度下,测得平衡时容器内气体的压强是反应前的5/6,试填写下列空白:
①用气体B表示的2min内的平均反应速率为 。
②平衡时,A的浓度为 mol/L。
(4)我国拥有完全自主产权的氢氧燃料电池车在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液。电池负极反应为 ,
正极反应 。
26.(4分)将下列物质进行分类:① H与
H与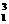 H ②O2与O3 ③乙醇与甲醚(CH3-O-CH3)
H ②O2与O3 ③乙醇与甲醚(CH3-O-CH3)
④H2O与D2O ⑤CH3CH2CH2CH2CH3与CH3-CH(CH3)-CH3 ⑥C60与C70
(1)互为同位素的是 (填编号、下同);
(2)互为同素异形体的是 ;
(3)互为同分异构体的是 ;
(4)互为同系物的是 。
25.某有机物的结构简式如右下式 , 该有机物 不可能具有的性质是
( )
不可能具有的性质是
( )
A.能跟NaOH溶液反应
B.能使酸性KMnO4溶液褪色
C.能发生水解反应
D.能发生酯化反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com