
题目列表(包括答案和解析)
6.下列说法中正确的是 ( )
A.从平衡常数的大小可以推断任意反应进行的程度
B. K值越大,反应的转化率越小
C. K值越大,反应的转化率越大
D.温度越高,K值越大
5.下列哪种说法可以证明反应.N2+3H2 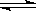 2NH3已达到平衡状态 ( )
2NH3已达到平衡状态 ( )
A.1个N≡N键断裂的同时,有3个H-H键形成
B.1个N≡N键断裂的同时,有3个H-H键断裂
C.1个N≡N键断裂的同时,有6个N-H键断裂
D.1个N≡N键断裂的同时,有6个N-H键形成
4.关于平衡常数,下列说法不正确的是 ( )
A.平衡常数不随反应物或生成物的浓度的改变而改变
B.平衡常数随温度的改变而改变
C.平衡常数随压强的改变而改变
D.使用催化剂能使平衡常数增大
3.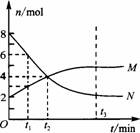 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是 ( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是 ( )
A.反应的化学方程式为:2M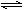 N
N
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
2. 14CO2与碳在高温条件下发生反应:14CO2+C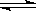 2CO,达到化学平衡后,平衡混合物中含14C的微粒有
( )
2CO,达到化学平衡后,平衡混合物中含14C的微粒有
( )
A.14CO2 B.14CO2,14CO
C.14CO2,14CO,14C D.14CO
1.化学平衡主要研究下列哪一类反应的规律 ( )
A.可逆反应 B.任何反应 C.部分反应 D.气体反应
14.一定温度下,反应2SO2 + O2 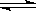 2SO2,达到平衡时,n(SO2):n(O2):n(SO3) = 2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是多少?
2SO2,达到平衡时,n(SO2):n(O2):n(SO3) = 2:3:4。缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是多少?
13.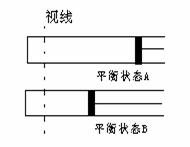 如图所示,600K时,在容积可变的透明容器内,反应2HI(g)
如图所示,600K时,在容积可变的透明容器内,反应2HI(g) 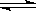 I2+H2(g)达到平衡状态A。保持温度不变,将容器的容积压缩成为原容积的一半,达到平衡状态B。按图示的观察方向________(填“能”或“不能”)看出两次平衡时容器内颜色深浅的变化,理由是___________ ______ ___________ __________
I2+H2(g)达到平衡状态A。保持温度不变,将容器的容积压缩成为原容积的一半,达到平衡状态B。按图示的观察方向________(填“能”或“不能”)看出两次平衡时容器内颜色深浅的变化,理由是___________ ______ ___________ __________
。
12.温度一定时, 于密闭容器中发生可逆反应: mA(g) + nB(g) 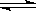 pC(g), 达到平衡后, 若将混合气体的体积压缩到原来的 1/2, 当再次达到平衡时, C的浓度为原平衡时C的浓度的 1 .9 倍, 试判断:⑴平衡向_ 方向移动;⑵C气体的体积分数_
(填增大、减少、不变)⑶.气体A的转化率_ (填增大、减少、不变) ⑷ m + n _ p(填“>、<、=” )。
pC(g), 达到平衡后, 若将混合气体的体积压缩到原来的 1/2, 当再次达到平衡时, C的浓度为原平衡时C的浓度的 1 .9 倍, 试判断:⑴平衡向_ 方向移动;⑵C气体的体积分数_
(填增大、减少、不变)⑶.气体A的转化率_ (填增大、减少、不变) ⑷ m + n _ p(填“>、<、=” )。
11.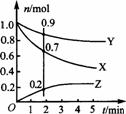 某温度时,在一个2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
某温度时,在一个2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
(1)该反应的化学方程式为
(2)反应开始至2 min,气体Z的平均反应速率为
(3)当反应达平衡时后
①若X、Y、Z均为气体,若此时只将容器的体积扩大为原来
的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应为
反应(填放热或吸热);达到新平衡时,容器内混合气体的平均分子量比原平衡时
(填“增大”“减小” 或“相等”)
②若只加大体系压强,Z的物质的量减少,若Y是气体,则X的聚集状态是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com