
题目列表(包括答案和解析)
13.美国阿波罗宇宙飞船上使用的氢氧燃料电池
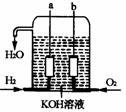
是一种新型的化学电池,其构造如图所示;两个电极
均由多孔性碳制成,通入的气体由孔隙中逸出,并在
电极表面放电。
(1)a极是 极,b极是 极,电极
反应式分别为 , 。
(2)飞船上宇航员的生活用水由燃料电池提供。已知这种电池发1度电时能生成350g水,试计算能量转化率。
 [2H2(g)+O2(g) 2H2O(l)+572kJ]
[2H2(g)+O2(g) 2H2O(l)+572kJ]
(3)这种电池的输出电压为1.2V。要使标有1.2V,1.5W的小灯泡连续发光0.5h,应消耗标准状况下的H2多少升?
(4)氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制。常用的燃料,往往是某些碳氢化合物,如甲烷(天然气)、汽油等。请写出将图中H2换成CH4时所构成的甲烷燃料电池中a极的电极反应式:
。此时电池内总的反应方程式为 。
12. 铅蓄电池放电时的总反应方程式为:PbO2+Pb+2H2SO4 2PbSO4+2H2O
铅蓄电池放电时的总反应方程式为:PbO2+Pb+2H2SO4 2PbSO4+2H2O
 据此判断其正极是 ,负极是
,电解质溶液是
,正极反应是
,负极反应是
,当转移0.5NA个电子时,蓄电池内消耗H2SO4的物质的量为
。
据此判断其正极是 ,负极是
,电解质溶液是
,正极反应是
,负极反应是
,当转移0.5NA个电子时,蓄电池内消耗H2SO4的物质的量为
。
11. 航天技术中使用的氢氧燃料电池具有高能、轻便、无污染等优点。氢氧燃料电池有酸式和碱式两种,它们放电时的总反应均可表示为:2H2+O2 2H2O。酸式燃料电池中的电解质是酸,其负极反应为:2H2-4e-=4H+,则正极反应为
。电池的电解质是碱,其正极反应为:O2+2H2O+4e-=4OH-,则负极反应为
。
航天技术中使用的氢氧燃料电池具有高能、轻便、无污染等优点。氢氧燃料电池有酸式和碱式两种,它们放电时的总反应均可表示为:2H2+O2 2H2O。酸式燃料电池中的电解质是酸,其负极反应为:2H2-4e-=4H+,则正极反应为
。电池的电解质是碱,其正极反应为:O2+2H2O+4e-=4OH-,则负极反应为
。
10.有人设计以铂和锌为电极材料,埋入人体作某种心脏病人的心脏起搏器的能源,它依靠人体血液中有一定浓度的O2和H2O进行工作。
(1)正极材料是 ,电极反应为 。
(2)负极材料是 ,电极反应为 。
9. 铅蓄电池的两极分别为Pb、PbO2,电解液为硫酸,工作时反应为Pb+PbO2+2H2SO4
铅蓄电池的两极分别为Pb、PbO2,电解液为硫酸,工作时反应为Pb+PbO2+2H2SO4
2PbSO4+2H2O,下列结论正确的是 ( )
A.Pb为正极被氧化 B.SO42-只向PbO2极移动
C.电池液密度不断减小 D.溶液的pH值不断减小
8.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧
化钾溶液为电解液。电池总反应式为:
 Zn(s)+2MnO2(s)+H2O(l) Zn(OH)2(s)+Mn2O3(s)
Zn(s)+2MnO2(s)+H2O(l) Zn(OH)2(s)+Mn2O3(s)
下列说法错误的是 ( )
A.电池工作时,锌失去电子
 B.电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e- Mn2O3(s)+2OH-(aq)
B.电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e- Mn2O3(s)+2OH-(aq)
C.电池工作时,电子由正极通过外电路流向负极
D.负电路中每通过0.2mol电子,锌的质量理论上减少6.5g
7.一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极上通乙烷
和氧气,其电极反应式为:C2H6+18OH--14e-=2CO32-+12H2O,7H2O+7/2O2+14e-=14OH-,
有关此电池的推断正确的是 ( )
A.电解质溶液中CO32-向正极移动
B.放电一段时间后,KOH的物质的量浓度不变
C.通乙烷的电极为负极
D.参加反应的O2和C2H6的物质的量比为7∶1
5.

 微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别为Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e- ZnO+H2O,Ag2O+H2O+2e- 2Ag+2OH-,总反应式为:Ag2O+ Zn 2Ag+ZnO。根据上述反应式,下列说法正确的是 ( )
微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别为Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e- ZnO+H2O,Ag2O+H2O+2e- 2Ag+2OH-,总反应式为:Ag2O+ Zn 2Ag+ZnO。根据上述反应式,下列说法正确的是 ( )
A.在使用过程中,电池负极区溶液的pH减小
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
|


 Cd(OH)2+2Ni(OH)2 Cd+2NiO(OH)+2H2O
Cd(OH)2+2Ni(OH)2 Cd+2NiO(OH)+2H2O
由此可知,该电池放电时的负极材料是 ( )
A.Cd(OH)2 B.Ni(OH)2 C.Cd D.NiO(OH)
4.燃料电池是燃料(例如CO,H2,CH4等)跟氧气或空气起反应,将此反应的化学能转变为电能的装置,电解质通常是KOH溶液。下列关于甲烷燃料电池的说法不正确的是( )
A.负极反应式为CH4+10OH--8e=CO32-+7H2O
B.正极反应式为O2+2H2O+4e=4OH-
C.随着不断放电,电解质溶液碱性不变
D.甲烷燃料电池的能量利用率比甲烷燃烧的能量利用率大
3.随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首
要原因是 ( )A。利用电池外壳的金属材料
B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C.不使电池中渗泄的电解液腐蚀其他物品
D.回收其中石墨电极
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com