
题目列表(包括答案和解析)
7. 一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g);DH<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
2C(g)+D(g);DH<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
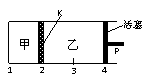


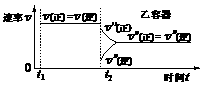
图1 图2 图3
(A)保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍
(B)保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均减少
(C)保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍
(D)保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略)
6. 已知 有相同容积的定容密封容器甲和乙,甲中加
有相同容积的定容密封容器甲和乙,甲中加
入H2和I2各0.1mol ,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的
平衡浓度大于乙中HI的平衡浓度,应采取的措施是
A.甲、乙提高相同温度 B.甲中加入0.1mol He,乙不改变
C.甲降低温度,乙不变 D.甲增加0.1mol H2,乙增加0.1mol I2
5. 下图表示反应X(g)
4Y(g)+Z(g),
下图表示反应X(g)
4Y(g)+Z(g), ,在某温度时X的浓度随时间变化的
,在某温度时X的浓度随时间变化的
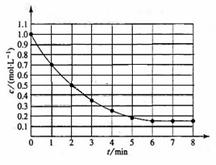 曲线:
曲线:
下列有关该反应的描述正确的是
A.第6min后,反应就终止了
B.X的平衡转化率为85%
C.若升高温度,X的平衡转化率将大于85%
D.若降低温度,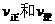 将以同样倍数减小
将以同样倍数减小
3. 恒温恒压下,在容积可变的器血中,反应2NO2(气) N2O4(气)达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
N2O4(气)达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
A 不变 B 增大 C 减小
D 无法判断
4.
已知反应mX(g)+nY(g) qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,
qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,
下 列说法正确的是
A.通入稀有气体使压强增大,平衡将正向移动
B.X的正反应速率是Y的逆反应速率的m/n倍
C.降低温度,混合气体的平均相对分子质量变小
D.增加X的物质的量,Y的转化率降低
2. 在一定体积的密闭容器中放入3升气体R和5升气体Q,在一定条件下发生反应:2R(气)+5Q(气) 4X(气)+nY(气)。反应完全后,容器温度不变,混和气体的压强是原来的87.5%,则化学方程式中的n值是
A 2 B 3 C 4 D 5
4X(气)+nY(气)。反应完全后,容器温度不变,混和气体的压强是原来的87.5%,则化学方程式中的n值是
A 2 B 3 C 4 D 5
1. 一个真空密闭容器中盛有1molPCl5,加热到200℃时发生如下反应:PCl5(气)  PCl3(气)+Cl2(气),反应达到平衡时,混合气体中PCl5所占体积分数为M%. 若在同一温度和同一容器中,最初投入是2molPCl5,反应达平衡时,混合气体中PCl5所占体积分数为N%.则M和N的关系
PCl3(气)+Cl2(气),反应达到平衡时,混合气体中PCl5所占体积分数为M%. 若在同一温度和同一容器中,最初投入是2molPCl5,反应达平衡时,混合气体中PCl5所占体积分数为N%.则M和N的关系
A.大于 B.小于 C.等于 D.不能肯定
13.把0.6 mol X气体和0.6 mol Y气体混合于2 L密闭容器中,使它们发生如下反应:2X(g)+
Y(g)===nZ(g)+2W(g)。2 min末已生成0.2 mol W,若测知以Z的浓度变化表示的反应速率为0.1 mol·L-1·min-1。,计算:(1)前2min内用X的浓度变化表示的平均反应速率;
12.A和B反应生成C,假定反应由A、B开始,它们的起始浓度均为1mol/L。反应进行2min
后A的浓度为0.8mol/L,B的浓度为0.6mol/L,C的浓度为0.6mol/L。则2min内反应的
平均速率VA=__________,VB=_____________,VC=___________。该反应的化学反应
方程式为___________________________。
11.在2SO2+O2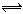 2SO3的反应里,开始SO2和O2的浓
2SO3的反应里,开始SO2和O2的浓
度均为0.5mol/L,2分钟后测得SO2的浓度为0.25mol/L,则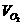 =_____________________,
=_____________________,
各物质所表示的反应速率的最简整数比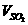 :
: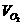 :
: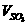 =___________。
=___________。
10.某温度时,在2 L容器中,X、Y、Z三种气体物质
的物质的量随时间变化的曲线图,由图中数据分析,
写出该反应的化学反应方程式?求反应开始至2s,
Z的平均反应速率?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com