
题目列表(包括答案和解析)
7.为研究金属腐蚀的条件和速率,某课外小组学生用金属丝将三根大小相同的铁钉分别固定在图示的三个装置中,再放置于玻璃钟罩里保存一星期后,下列对实验结束时现象描述不正确的是 ( )
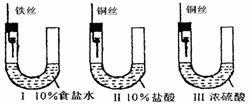
A.装置Ⅰ左侧的液面一定会上升 B.左侧液面装置Ⅰ比装置Ⅱ的低
C.装置Ⅱ中的铁钉腐蚀最严重 D.装置Ⅲ中的铁钉几乎没被腐蚀
6.钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为:2Fe+2H2O+O2 2Fe2++4OH-。
以下说法正确的是 ( )
A.负极发生的反应为:Fe-2e- Fe2+
B.正极发生的反应为:2H2O+O2+2e- 4OH-
C.原电池是将电能转变为化学能的装置
D.钢柱在水下部分比在空气与水交界处更容易腐蚀
5.关于金属腐蚀的如下各叙述中,正确的是 ( )
A.金属被腐蚀的本质是:M+nH2O=M(OH)n+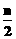 H2↑
H2↑
B.马口铁(锡铁)镀层破损后被腐蚀时,首先是镀层被氧化
C.金属在一般情况下发生的电化学腐蚀主要是吸氧腐蚀
D.常温下,置于空气中的金属主要发生化学腐蚀
4.以下现象与电化腐蚀无关的是 ( )
A.黄铜(铜锌)制作的铜锣不易产生铜绿
B.生铁比纯铁易生锈
C.铁质器件附有铜质配件,在接触处易生铁锈
D.银质奖牌久置后表面变暗
3.下列叙述正确的是 ( )
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,把氧化铝加入液态冰晶石中成为熔融体后电解
⑤钢铁表面常易锈蚀生成Fe2O3·nH2O
A.①②③④⑤ B.①③④⑤
C.①③⑤ D.②④
2.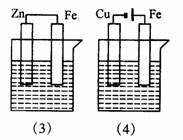
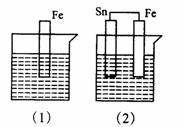 下图各容器中盛有海水,铁在其中腐蚀时由快到慢的顺序是 ( )
下图各容器中盛有海水,铁在其中腐蚀时由快到慢的顺序是 ( )
A.(4)>(2)>(1)>(3)
B.(2)>(1)>(3)>(4)
C.(4)>(2)>(3)>(1)
D.(3)>(2)>(4)>(1)
1.在空气中,钢铁与食盐水接触,发生电化腐蚀,在正极上发生的电极反应是 ( )
 A.Fe-2e- Fe2+
A.Fe-2e- Fe2+
 B.2H+2e- H2↑
B.2H+2e- H2↑
 C.Na++e- Na
C.Na++e- Na
 D.2H2O+O2+4e- 4OH-
D.2H2O+O2+4e- 4OH-
28. 通常人们把拆开1mol化学键所吸收的能量看成键能,键能的大小可以衡量化学键的强弱,也可以用于计算化学反应中的反应热(△H),化学反应中的△H等于反应中断裂的化学键的键能之和与反应中形成新的化学键的键能之和的差
|
化学键 |
Si-Cl |
H-H |
H-Cl |
Si-Si |
|
键能/KJ.mol |
360 |
436 |
431 |
176 |
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)==Si(s)+4HCl(g),该反应的反应热△H为多少?
27.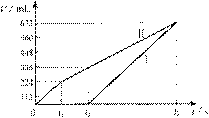 常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(气体体积已换算成标准状况下的体积),根据图中信息回答下列问题。
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(气体体积已换算成标准状况下的体积),根据图中信息回答下列问题。
⑴通过计算推测:
①原混合溶液NaCl和CuSO4的物质的量浓度。
②t2时所得溶液的pH。
⑵实验中发现,阳极产生的气体体积与阴极相比,明显小于对应时间段的理论值。试简要分析其可能原因。
26.(1)肼(N2H4)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。已知在l0lkPa时,32.0gN2H4在氧气中完全燃烧生成氮气和H2O,放出热量624kJ(25℃时),N2H4完全燃烧的热化学方程式是 。
(2)肼一空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液。肼一空气燃料电池放电时:正极的电极反应式是 ;负极的电极反应式是 。
(3)下图是一个电解过程示意图。
①锌片上发生的电极反应式是 。
②假设使用肼一空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标准状况下的空气 L(假设空气中氧气体积分数为20%)。
(4)传统制备肼的方法是以NaClO氧化NH3,制得肼的稀溶液,该反应的离子方程式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com