
题目列表(包括答案和解析)
27.(14分)
(1)__________________________________________________________。
(2)________个,________个,________,
____________________________________________________________________。
(3) ________(填写物质序号), ________(填写物质序号)。
(4)________________________________________________________________________
________________________________________________________________________。
26. (6分)
(6分)
Cl2 + SO2 + 2H2O = H2SO4 + 2HCl
氧化剂_____________,氧化产物_____________;
31.(6分)已知实验中用MnO2与浓盐酸反应制Cl2时,当溶液中盐酸浓度降为
4mol·L-1时即不再有Cl2产生。常用浓盐酸浓度为12mol·L-1。试根据上述信息分析回答:
(1)用8.7gMnO2与足量浓盐酸反应可产生Cl2 mL(标准状况)
(2)由题中信息计算将8.7gMnO2完全消耗,需浓盐酸的体积为 mL
而实际实验中消耗盐酸的体积偏大,可能原因是:
 台州中学2010-2011学年第一学期期中试题答题卷
台州中学2010-2011学年第一学期期中试题答题卷
高一 化学
第I卷 选择题(共50分)
选择题(本题包括25小题,每小题2分,共 50分。只有一个选项符合题意)
第II卷 非选择题(共50分)
30.(4分)在 NaCl与MgCl2的混合液中,Na+与Mg2+的物质的量之比为1:2。如果混合液中共有0.5 mol Cl-,溶液的体积为0.5 L,则混合液中氯化钠的质量为 ;MgCl2的物质的量浓度为 。
29.(10分)根据下图所示提供的仪器装置,完成提纯并测定Na2CO3样品纯度(其中只含NaHCO3杂质)的实验,试回答有关问题:

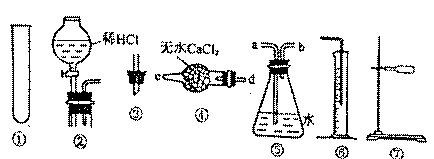
实验一:测定Na2CO3样品中NaHCO3加热分解放出CO2气体,连接装置的正确顺序是⑦①③④⑤⑥
(1)完成该实验尚缺的仪器是 (填名称)
(2)产生气体从装置④的 进入,从装置⑤的 进入。
实验二:测定上述实验完成后剩余固体与盐酸反应产生CO2的体积。
(3)应将实验一中的装置①换成装置 (填装置序号)
(4)当实验一加热至样品不再产生气体时,产生CO2为a mol,实验二在加入盐酸至无气体产生时,生成CO2为b mol,则样品中Na2CO3纯度的实测值为 .
28.(10分)现有稀盐酸、稀硫酸、氢氧化钡、碳酸钠四瓶失去标签的溶液,分别编号为A、B、C、D。每次取少量溶液两两混合,所观察到现象记录在下表中(“-”表示无明显现象;“↓”表示有沉淀生成;“↑”表示有气体生成)
(1)据此推断这四瓶溶液分别为
A ;B ; C ; D ;
(2)写出上述实验过程中有关物质间反应的离子方程式:
|
|
A |
B |
C |
D |
|
A |
|
↑ |
↓ |
- |
|
B |
↑ |
|
↓ |
↑ |
|
C |
↓ |
↓ |
|
- |
|
D |
- |
↑ |
- |
|
B+C ;
C+D ;
A+C ;
27.(14分)“探险队员”--盐酸,不小心走进了化学迷宫,不知怎样走出来,其中阴影方块是障碍物,不能通过,迷宫中的空白区域是路,路上有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
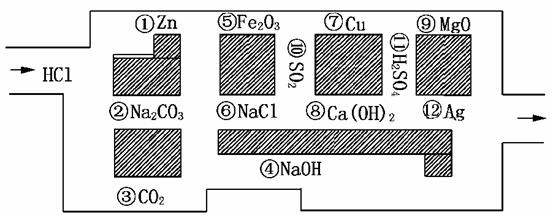
(1)请你帮助它走出迷宫(请用图中物质前的序号按序排列表示所走的路线)。________________________________________________________________________。
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有________个,属于氧化还原反应的有________个,其中能“吃掉”盐酸的盐是________(填写物质序号),写出该反应的离子方程式_____________________________________________________。
(3)在不能与盐酸反应的物质中,属于电解质的是________(填写物质序号),属于非电解质的是________(填写物质序号)。
(4)如果将盐酸换成氯气,它在一定条件下能沿着盐酸走出的路线“走出”这个迷宫吗?为什么?
________________________________________________________________________。
26.(6分)用双线桥标出下列反应中电子转移的方向和数目,并指出氧化剂和氧化产物。
Cl2 + SO2 + 2H2O = H2SO4 + 2HCl
氧化剂 ,氧化产物 ;
25.已知单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点就越高,下列溶液沸点最高的是 ( )
A.0.01 mol·L-1的蔗糖溶液
B.0.01 mol·L-1的CaCl2溶液
C.0.02 mol·L-1的NaCl溶液
D.0.02 mol·L-1的氨水高考资源
第II卷 非选择题(共50分)
24.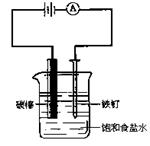 如图所示装配仪器,接通直流电源,电解饱和食盐水,
如图所示装配仪器,接通直流电源,电解饱和食盐水,
则电解一段时间后,在碳棒和铁钉表面都有气体生成,
其中碳棒表面生成的气体是 ( )
A.Cl2 B.O2 C.H2 D.HCl
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com