
题目列表(包括答案和解析)
3、下列反应中是离子反应,但不是氧化还原反应的是 ( )
A.金属钠放入水中生成氢氧化钠和氢气 B.金属钠在氯气中燃烧
C.铁片置于硫酸铜溶液中 D. 氯化钠溶液中滴入硝酸银溶液
2、下列属于强电解质的是 ( )
① NaOH ② NH3·H2O ③KCl ④ 醋酸 ⑤NaHCO3
A.①②⑤ B.①③④ C.②③④ D.①③⑤
1、下列物质的用途,利用了该物质氧化性的是 ( )
A. 用过氧化钠漂白织物 B. 医药上可用小苏打治疗胃酸过多
C. 用钠冶炼钛等金属 D. 用Na-K合金作原子反应堆的导热剂
31.(8分)标准状况下,22.4LHCl气体溶于50mL水再配成250mL溶液:
(1)求所得盐酸的物质的量浓度?
(2)若将此溶液再稀释成1L溶液,求稀释后盐酸的物质的量浓度?
(3)将(2)的溶液取出250mL与足量的Zn反应可以产生多少体积的H2(在标准状况下) ?
中山市实验高级中学2010-2011学年度高一上学期期中考试
30.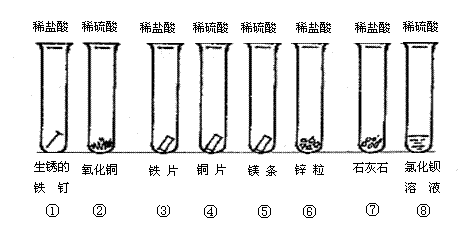 (14分)某课外活动小组进行下列实验(如下图所示)。
(14分)某课外活动小组进行下列实验(如下图所示)。
(1)某同学将这些实验分成三组,各组的试管编号是:第一组①②;第二组③④⑤⑥;第三组⑦⑧。
你认为如此分组的依据是: 。
(2)写出试管②⑤⑧的实验现象及有关的离子方程式:
② ; 。
⑤ ; 。
⑧ ; 。
29.(8分)从下列各组反应对比中,判断哪种粒子的氧化性最强,哪种粒子的还原性最强.
(1)铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质,则Cu、Fe、Ag中,___________还原性最强;Cu2+、Fe2+、Ag+中,_______________氧化性最强。
(2)铁钉在氯气中被锈蚀成棕褐色物质FeCl3,而在盐酸中生成淡绿色溶液(FeCl2)。则氯气分子、氯离子、氢离子中_____________具有氧化性,___________氧化性最强。
28.(10分)写出下列电离方程式或反应的离子方程式
(1)硫酸铝电离的电离方程式 ________________:
(2)向澄清石灰水中加硝酸 ________________;
(3)用石灰石与盐酸反应制取二氧化碳 _________________;
(4)锌粉加入硫酸溶液中 _______________;
(5)向Na2CO3溶液中滴加几滴稀盐酸: _______________。
27.用18.4 mol·L-1的浓硫酸配制100mL1.0mol·L-1稀硫酸。
(1)需量取浓硫酸的体积为 mL(保留一位小数)。
(2)若实验仪器有:
(A)100mL量筒 (B)托盘天平 (C)玻璃棒 (D)50mL容量瓶 (E)10mL量筒 (F)胶头滴管 (G)50mL烧杯 (H)100mL容量瓶
实验时选用的仪器除C、F、G外还应选用(填序号)
(3)配制过程中,下列情况会使配制结果偏高的是(填序号)
(A)定容时俯视刻度线观察液面;
(B)容量瓶使用时未干燥;
(C)定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
(4)在容量瓶的使用中,下列操作不正确的是(填序号)
(A)使用容量瓶前检查它是否漏水
(B)容量瓶用蒸馏水洗净后,不用待配制的溶液洗涤
(C)将氢氧化钠固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
(D)将准确量取的18.4mol·L-1的硫酸,注入已盛有30mL水的100mL的容量瓶中,加水至刻度线
(E)定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
26.现有一瓶A和B的混合液,已知它们的性质如下表。
|
物质 |
熔点/℃ |
沸点/℃ |
密度/g·cm-3 |
溶解性 |
|
A |
-11.5 |
198 |
1.11 |
A、B互溶, 且均易溶于水 |
|
B |
17.9 |
290 |
1.26 |
据此分析,将A和B相互分离的常用方法是: (填“过滤”、“蒸发”、“萃取”、“分液”、“蒸馏”等)
25.下列溶液中Cl-浓度最大的是( )
(A)200 mL 2 mol/L MgCl2溶液 (B)1000 mL 2 .5mol/L NaCl溶液
(C)250 mL 1 mol/L AlCl3溶液 (D)300 mL 5 mol/L KClO3溶液
第Ⅱ卷
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com