
题目列表(包括答案和解析)
2.当一束光通过鸡蛋清和水的分散系可以观察到丁达尔现象,这表明鸡蛋清和水的分散系属于
A.溶液 B.悬浊液 C.乳浊液 D.胶体
1.
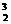 国庆期间,我国“嫦娥Ⅱ号”成功进入月球轨道。据科学家预测,月球的土壤中吸附着数百万吨的 He,每百吨 He核聚变所释放出的能量相当于目前人类一年消耗的能量。下列说法正确的是
国庆期间,我国“嫦娥Ⅱ号”成功进入月球轨道。据科学家预测,月球的土壤中吸附着数百万吨的 He,每百吨 He核聚变所释放出的能量相当于目前人类一年消耗的能量。下列说法正确的是
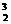
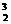 A. He原子的质量数为3
B. He和T(3H)互为同位素
A. He原子的质量数为3
B. He和T(3H)互为同位素
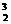
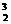 C.
He核聚变是化学变化
D. He原子核内含有3个质子
C.
He核聚变是化学变化
D. He原子核内含有3个质子
24.(4 分)欲除去KCl溶液中的Ba(OH)2杂质,若只准加一种试剂,则这种试剂是 ,反应的化学方程式是 。
梅州市曾宪梓中学2010-2011学年度第一学期期中考试
23.(10分)对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取等。下列各组混和物的分离或提纯应采用什么方法?
(1)实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用 的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒。
(2)提取碘水中的碘,用 方法。
(3)除去食盐溶液中的水,可采用 的方法。
(4)提纯食盐水,可采用 的方法。
(5)分离饱和食盐水和沙子的混合物,可采用 的方法。
22.(18分)实验室用氯化钠固体配制1.00 mol/L的NaCl溶液0.5 L,回答下列问题
(1)请写出该实验的实验步骤
① ,② ,③ ,④ ,⑤ ,⑥ ,⑦ 。
(2)所需仪器为:容量瓶 (规格: )、托盘天平、还需要哪些实验仪器才能完成该实验,请写出: 。
(3)试分析下列操作对所配溶液的浓度有何影响及造成该影响的原因。
①为加速固体溶解,可稍微加热并不断搅拌。在未降至室温时,立即将溶液转移至容量瓶定容。对所配溶液浓度的影响: (填“偏高”“偏低”或“不变”),原因是: 。
②定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响 (填“偏高”“偏低”或“不变”),原因是: 。
③溶解时所用过的烧杯、玻璃棒未洗涤。对所配溶液浓度的影响: (填“偏高”“偏低”或“不变”), 原因是: 。
21.(8分)322g Na2SO4·10H2O的物质的量是________,其中所含的Na+的物质的量是 ,SO42-的物质的量是 ;将322g Na2SO4·10H2O溶于水配成2L溶液,其物质的量浓度是_______ 。
20.为了除去粗盐中Ca2+ 、 Mg2+ 、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作。其中正确的操作顺序( )
①过滤 ②加过量的NaOH ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
A.①④②⑤③ B.④①②⑤③ C.②⑤④①③ D.⑤②④①③
第二卷 (非选择题,共40分)
19.下列溶液中Cl-浓度与50ml 1mol/L HCl 溶液中Cl-浓度相等的是( )
A.150 mL 1 mol·L-1NaCl溶液 B.75 mL 2mol·L-1NH4Cl溶液
C.150 mL 1 mol·L-1KCl溶液 D.75 mL 1mol·L-1FeCl3溶液
18.下列叙述正确的是( )
A.l mol H2O的质量为18 g/mol B.CH4的摩尔质量为16 g/mol
C.3.01×1023个SO2分子的质量为32 g D.标准状况下,1 mol任何物质体积均为22.4 L
17.下列实验操作中,错误的是 ( )
A.蒸发操作时,使混合物中的水分完全蒸干后,才停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口略低处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com