
题目列表(包括答案和解析)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
B |
C] |
D |
B |
B |
D |
C |
C |
|
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
|
D |
A |
D |
D |
D |
C |
A |
A |
17(每小题2分,共8分)
(1) ①⑤ (2) ①②⑩ (3) ③⑧⑨⑩ (4) ④⑥
18(每空1分,共9分
(1)K2CO3 (2)蒸发 玻璃棒
(3)盐酸 将过量的K2CO3转化成KCl
(4)(i)不正确 14.5
(ii)没有使用玻璃棒引流 烧杯和玻璃棒没有进行洗涤

16.下列说法中正确的是 ( )
A.在0℃、1.01×105 Pa的条件下,某气体的体积约为2.24×10-2 m3,该气体的物质的量为1 mol
B.1 mol某气体的体积为22.4 L,该气体所处的状况必定为标准状况
C.在20℃的温度下,1 mol某气体的体积约为22.4 L,该气体的压强为101 kPa
D.固态的二氧化碳又叫干冰,含CO2 1 mol的干冰在标准状况下的体积必定小于22.4 L
第II卷(52分)
17(8分)现有以下物质:①稀硫酸 ②钠 ③生石灰 ④无水酒精 ⑤空气 ⑥干冰
⑦金刚石 ⑧纯碱 ⑨NaOH晶体 ⑩熔化的K2SO4。(用序号回答)
(1)以上物质中属于混合物的是 ,
(2)以上物质中能导电的是 ,
(3)以上物质中属于电解质的是 ,
(4)以上物质中属于非电解质的是 。
18(9分) 实验室中有一瓶氯化钾和氯化钙的固体混和物,通过下面的实验除去氯化钾中的氯化钙,并利用纯净的氯化钾配制一定浓度的氯化钾溶液。根据实验步骤填写下列空白。

回答下列问题
(1)加入的A是___________________。[来
(2)操作②的名称是_______________________。操作①、②均要用到的玻璃仪器有__________________________。
(3)B物质是____________,加入过量的B物质理由是
(4)称取一定量纯净的KCl,配制一定浓度的氯化钾溶液。
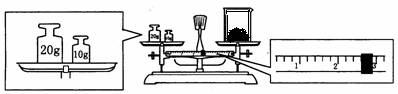
(i)某同学用托盘天平称取一定质量的KCl,称法如下图所示,天平的指针在标尺中间。此操作是否正确___________(填正确或不正确);若按此操作称量,所称KCl的实际质量为_______g (已知烧杯的质量为12.9克) 。
(ii)某学生将准确称量的KCl固体放入烧杯中,加入约30毫升蒸馏水,用玻璃棒搅拌使其溶解。将溶液由烧杯倒入100毫升容量瓶中,然后往容量瓶中小心地加蒸馏水,直到液面接近刻度1~2厘米处,改用胶头滴管加蒸馏水,使溶液凹液面最低点恰好与刻度相切,把容量瓶盖紧,再振荡摇匀。该生操作中的错误是 ____________________和__________________。
19(10分)在生产生活中,我们会遇到各种各样的化学反应。下面是其中的几个例子,请写出相应反应的化学方程式并完成填空。
① 胃舒平中含有氢氧化铝[Al(OH)3],可用来治疗胃酸(盐酸)过多。
化学方程式
② 碳铵(NH4HCO3)是一种常用化肥,应保存于阴凉处,因为在较高温度下,它会发生分解,生成氨气、水和二氧化碳。
化学方程式
③ 实验室常用锌和稀硫酸反应制取氢气。
化学方程式
④我国目前正在实施“西气东输”计划,用天然气(主要成分为CH4)逐步代替煤气作燃料。
化学方程式
⑤将生石灰(CaO)投入水中,即可得到建筑用的熟石灰[Ca(OH)2]
化学方程式
在上述反应中,属于化合反应的是(填序号,下同) ,属于分解反应的是 ,属于置换反应的是 ,属于复分解反应的是 ,属于氧化还原反应的是
20(5分)下列各组混合物的分离或提纯应采用什么方法最合适?
(1)除去Ca(OH)2溶液中悬浮的CaCO3颗粒,用 方法;
(2)除去乙醇中溶解的微量食盐,用 方法;
(3)除去氧化钙中的碳酸钙,用 方法;
(4)提取碘水中的碘,用 方法;
(5)除去食盐溶液中的水,可采用 方法
21(10分)A、B、C、D、E分别是NH4Cl、 Ba(OH)2 、 KCl、K2SO4 、(NH4)2SO4等无色溶液中的一种,将它们两两混合时产生的现象是:①A和B混合时产生白色沉淀,加热后无明显现象;②B和C混合时也有白色沉淀生成,加热后产生的气体使湿润的红色石蕊试纸变蓝;③B和E混合后无沉淀,但加热后能产生使湿润的红色石蕊试纸变蓝的气体;④D和任何一种溶液混合后,都无明显变化。
根据上述实验现象进行推断,写出有关溶液中溶质的化学式。
A B C D E
22(10分)欲用98%的浓硫酸(ρ=1.84g/mL)配制成浓度为0.25mol•L-1的稀硫酸1000mL。简要回答下列问题:
(1)所需浓硫酸的体积为 mL。
(2)如果实验室有15 mL、20 mL、50 mL的量筒,应选用 mL的量筒最好,量取时发现量筒不干净用水洗净后直接量取将使结果浓度 (填“偏高”“偏低”或“无影响”,下同)。
(3)将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并不断搅拌的目的是 ,
若搅拌过程中有液体溅出,结果会使浓度
(4)在转入容量瓶前烧杯中液体应 ,否则会使结果浓度 ;并洗涤烧杯2-3次,洗涤液也要转入容量瓶,否则会使结果浓度
(5)定容时必须使溶液凹液面与刻度线相平,若俯视会使结果浓度 ;仰视则使结果浓度
南安一中2010-2011学年度第一学期期中考试参考
15.中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃时制造出纳米级金刚石粉末。该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”。同学们对此有下列一些理解,其中错误的是 ( )
A.金刚石属于金属单质 B.制造过程中元素种类没有改变
C.CCl4是一种化合物 D.这个反应是置换反应
14.下列不存在丁达尔效应的分散系是( )
①有尘埃的空气 ②溴水 ③蒸馏水 ④沸水中加几滴FeCl3浓溶液 ⑤淀粉溶液
A.② B.②③④⑤ C.②③ D.①②③⑤
13.设NA为阿伏加德罗常数的值。下列说法中正确的是( )
A.1mol Na2SO4溶于水中,所得溶液中Na+个数为NA
B.18g水含有原子数为3NA,所含的电子数为8NA
C. 22.4L氢气含有氢原子个数为2NA
D.NA个氢分子和NA个氧分子的质量比为1︰16
12.焰火“脚印”、“笑脸”、“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”知识相关。下列说法中正确的是( )
A.非金属单质燃烧时火焰均无色 B.所有金属及其化合物灼烧时火焰均有颜色
C.焰色反应均应透过蓝色钴玻璃观察 D.NaC1与Na2CO3灼烧时火焰颜色相同
11.下列实验操作中错误的是 ( )
A.蒸发操作时,混合物中还有少量的水就停止加热 ,利用余热蒸干
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
10.在标况下,1体积水溶解700体积氨气,所得溶液的密度为0.9g•cm-3,这种氨水的物质的量浓度为( )
A.18.4 mol/L B.20.4 mol/L C.34.4 mol/L D. 38.5 mol/L
9.精确配制一定物质的量浓度的NaOH溶液,下列实验操作中,正确的是( )
A.称量时,将NaOH固体直接放在天平托盘上面的纸上
B.将称好的NaOH固体放入容量瓶中,加入少量水溶解
C.在烧杯中溶解NaOH固体后,立即将所得溶液注入容量瓶中
D.将烧杯中已冷却的NaOH溶液注入未经干燥的容量瓶中
8.已知某溶液中c(Na+)=0.2mol/L,c(Mg2+)=0.25mol/L,c(Cl-)=0.4mol/L,如果溶液中还有SO42-,那么c(SO42-)应为( )
A.0.1 mol/L B.0.3 mol/L C.0.15 mol/L D.0.5 mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com