
题目列表(包括答案和解析)
30、(12分)某研究性学习小组在做氯气的喷泉实验时(装置如图),发现含有酚酞的NaOH溶液喷入烧瓶后,溶液的红色褪去。为什么会出现这些现象呢?该小组的同学对溶液的红色褪去提出了猜想,并进行了实验探究。
[作出猜想]
甲:因为氯气与NaOH溶液反应,使溶液碱性减弱甚至呈酸性.所以溶液红色褪去。
乙:因为氯气溶于水并与水反应,(模仿甲完成乙的猜想)__________▲_________。
[实验验证]
验证甲同学的猜想是否正确的方法是:
__________________▲___________________。
[拓展延伸]
类似“褪色喷泉实验”还有多种“变色的喷泉实验”,请你按实验要求,分别设计1个“变色喷泉实验”并填写下列表格:
|
编号 |
实验要求 |
烧杯中的溶液 |
滴管中的液体 |
烧瓶中的气体 |
|
① |
无色变红色喷泉 |
▲ |
H2O |
▲ |
|
② |
红色变无色喷泉 |
▲ |
▲ |
HCl |
29、A、B、C、D四种短周期元素的原子序数依次增大。A、D同主族,B、C同周期。A、B组成的化合物甲为气态,其中A、B原子数之比为4︰1。由A、C组成的两种化合物乙和丙都为液态,乙中A、C原子数之比为1︰1,丙中为2︰1。由D、C组成的两种化合物丁和戊都为固态,丁中D、C原子数之比为1︰1,戊中为2︰1。
⑴写出甲的分子式和丁的电子式:甲 、丁 ;
⑵写出B元素的最高价氧化物跟丁发生反应的化学方程式: 。
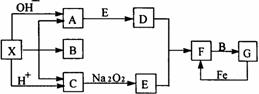
28、 下图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据右图关系推断:
下图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据右图关系推断:
(1)化学式:
X____________,A___________,B____________。
 (2)实验室收集气体D和F的方法依次是___________法、_______________法。
(2)实验室收集气体D和F的方法依次是___________法、_______________法。
(3)请写出A与E反应生成D的化学方程式_______________________________________。
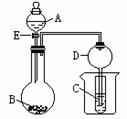
27、在如图所示的实验装置中,当A、B、C分别为以下不同组合时,回答有关问题。
(1)当A为盐酸、B为贝壳(粉末)、C为水玻璃时,小试管中的现象是 ,其中发生的
离子反应方程式是 。
 (2)当A为浓氨水、B为生石灰、C为AlCl3溶液,小试管中出现的现象是
,反应的离子方程式为
(2)当A为浓氨水、B为生石灰、C为AlCl3溶液,小试管中出现的现象是
,反应的离子方程式为
(3)当A为浓硫酸、B为Mg、Al、Fe、Cu中的一种银白色片状金属、
C为品红溶液,小试管中溶液红色褪去,则B为 (填元素符号),
A和B反应的方程式是
(4)装置D的作用是 。
26.下列顺序不正确的是
A.微粒半径Na+<K+<Cl-<S2- B.稳定性HI>HBr>HCl>HF
C.酸性H4SiO4<H3PO4<H2SO4<HClO4 D.碱性KOH>Ca(OH)2>Mg(OH)2>Al(OH)3
(非选择题,共计48分)
25.为确定下列置于空气中的物质是否变质,所选检验试剂(括号内物质)不能达到目的的是
A.Na2SO3溶液(BaCl2) B.FeCl2溶液(KSCN) C.KI(淀粉溶液) D.Na2S(H2O)
24.镁与很稀的硝酸反应生成硝酸镁、硝酸铵和水。当生成1 mol硝酸镁时,被还原的硝酸的物质的量为:
A.2mol B.1 mol C.0.5mol D.0.25mol
23.下列化学反应的离子方程式正确的是:
A.碳酸氢铵溶液与足量的氢氧化钠溶液混合:NH4+ + HCO3- +2OH- = NH3·H2O+ CO32-+ H2O
B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
C.用稀HNO3溶解FeS固体:FeS+2H+=Fe2++H2S↑
D.氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-=CaSO4↓+H2O
22、下列叙述正确的是
A.同周期元素中,ⅦA族元素的原子半径最大
B.ⅥA族元素的原子,其半径越大,越容易得到电子
C.室温时,零族元素的单质都是气体
D.所有主族元素的原子,形成单原子离子时的化合价和它的族序数相等
21、下列叙述正确的是
A.同周期元素中,ⅦA族元素的原子半径最大
B.ⅥA族元素的原子,其半径越大,越容易得到电子
C.室温时,零族元素的单质都是气体
D.所有主族元素的原子,形成单原子离子时的化合价和它的族序数相等
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com