
题目列表(包括答案和解析)
28、学生利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去)
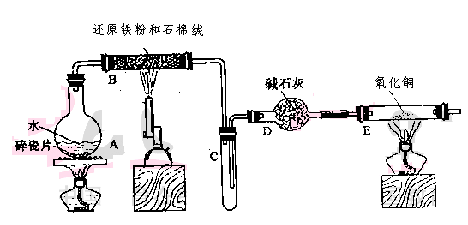
(1) 回答下列问题:所用铁粉中若有杂质,欲除去不纯铁粉中混有的铝粉可以选用的试剂为__ __(填序号)。
A.稀盐酸 B.氢氧化钠溶液 C.浓硫酸 D. FeCl3溶液
此步涉及反应的离子方程式为 。经除杂后的铁粉进一步干燥后装入反应容器。
(2)反应发生后装置B中发生反应的化学方程式是_______________ ____。
D装置的作用:________________.
(3)该小组学生把B中反应后的产物加入足量的盐酸,过滤,用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
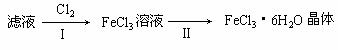
①用离子方程式表示步骤I中通入Cl2的作用
(用单线桥表示电子转移的方向和数目)
②为了检验某未知溶液是否是FeCl2溶液,同学们设计了以下实验方案加以证明。
向一支装有该未知溶液的试管中先通入氯气,再滴加KSCN溶液,溶液呈现红色,证明该未知溶液是FeCl2溶液。你认为此方案是否合理 (填”合理”或”不合理”)。
27、(10分)已知有以下物质相互转化 www.k@s@5@ 高#考#资#源#网
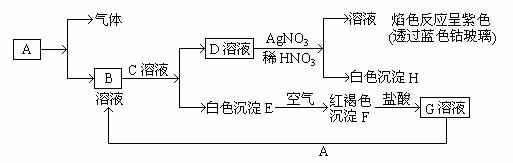
试回答:(1)写出B的化学式_______________;D的化学式_____
(2)写出由E转变成F的化学方程式____________________。
(3)写出鉴别G溶液中阳离子的试剂及现象___________________________;
(4)向G溶液加入A的离子反应方程式___________________
26、A、B、C、D、E五种物质的焰色反应都显黄色,A、B与水反应都有气体放出,A与水的反应放出的气体具有氧化性,同时都生成溶液C,C与适量的CO2反应生成D,D溶液与过量的CO2反应生成E,E加热能变成D。
(1)写出A与CO2反应的化学方程式
(2)写出D溶液与过量的CO2反应的离子方程式
(3)E可治疗胃酸(0.2%-0.4%的盐酸)过多,反应的离子方程式为______
(4)等质量的D和E分别与足量盐酸反应时生成CO2的量,前者_____后者(填“>”、“<”或“=”)。
25、将一定量的Na、Na2O、Na2O2的混合物与足量的水反应,在标准状况下得到a L混合气体。将该混合气体通过电火花引燃,恰好完全反应,则原混合物中Na、Na2O、Na2O2的物质的量之比可能为
A.2:1:1 B.1:1:2 C.1:2:1 D.4:3:2
24、 在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如下图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为
A、6:1 B、1:1 C、2:1 D、1:2
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如下图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为
A、6:1 B、1:1 C、2:1 D、1:2
23、镁铝合金5.1 g溶于300mL2mol/L的HCl,在标准状况下放出气体的体积为5.6 L。向反应后的溶液中加入足量氨水,产生沉淀的质量为
A.5.1g B.10.2g C.13.6g D.15.3g
22、密闭容器中装有1mol NaHCO3和0.8mol Na2O2,加热充分反应后,容器内残留的固体是 www.k@s@5@ 高#考#资#源#网
A.0.8molNa2CO3和0.6molNaOH B.0.5molNa2CO3和1molNaOH
C.0.8molNa2CO3和1molNaOH D.1molNa2CO3和0.6molNaOH
21、在一定温度下,向饱和的烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原温,下列说法正确的是 ( )
A.溶液中Na+浓度增大,有O2放出 B.溶液的OH-浓度不变,有O2放出
C.溶液中Na+数目减少,有O2放出 D.OH-浓度增大,有O2放出
20. 把下列各组溶液的后者滴入前者,由于滴加的量不同,产生的现象不同的是
A.AlCl3 和NaOH B.NaHCO3和HCl
C.Na2CO3和HCl D.NaCl和AgNO3
19、某溶液能溶解Al(OH)3,则此溶液中一定能大量共存的离子组是 ( )
A.Mg2+ 、Cl-、Na+、NO3- B.K+、Na+、NO3-、HCO3-
C.Na+、Ba2+、Cl-、NO3- D.Fe3+、Na+、AlO2-、SO42-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com