
题目列表(包括答案和解析)
23、(9分)某研究性学习小组为测定镁和铝的混合物中铝的质量分数,称取该混合物a g,溶于200ml5mol/LHCl溶液中,共收集到标准状况下的氢气3.36L。
(1)a的取值范围是 ;
(2)向反应后所得溶液中逐渐加入4mol/L的NaOH溶液。当沉淀质量达到最大值时,加入的NaOH溶液的体积是 ml,沉淀的最大质量为 g(用含a的代数式表示)。
(3)继续加入NaOH溶液至沉淀质量不再发生变化时,过滤、洗涤并灼烧沉淀至恒重,所得残余固体的质量仍为ag,计算原混合物中铝的质量分数。(写出计算过程)
第Ⅱ卷(非选择题 共52分)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
A |
C |
D |
C |
B |
C |
A |
B |
|
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
|
A |
D |
B |
B |
C |
D |
D |
A |
22、(11分)某结晶水合物是一种复盐,含有两种阳离子和一种阴离子。称取两份质量均为1.96的该结晶水合物,分别制成溶液。一份加入足量Ba(OH)2溶液,生成白色沉淀,随即沉淀转变为灰绿色,最后变为红褐色,用足量稀盐酸处理沉淀物,经洗涤和干燥,得到白色固体2.33g,另一份加入含0.001molKMnO4的酸性溶液,MnO4-恰好全部被还原为Mn2+。加热该结晶水合物,产生有刺激性气味的碱性气体。
问:(1)1.96g结晶水合物中阴离子是 ,物质的量为 ;
(2)该结晶水合物中含有的两种阳离子是 和 ;物质的量分别为
和 ;
(3)该结晶水合物的化学式为 。
21、(8分)工业纯碱中常含有NaCl、Na2SO4等杂质,为了测定工业纯碱中Na2CO3的含量,某同学设计了如下图装置:
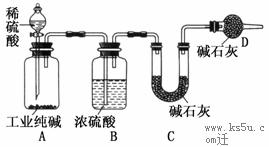
试回答下列问题:
(2)装置A中发生反应的离子方程式为:______________________________________。
(3)装置D的作用是______________________________________________。
(4)利用上述装置进行实验,即使气密性良好,并缓慢滴加了过量的稀硫酸使反应完全,装置C中装有足量碱石灰,其他操作也正确,测定结果还是偏低,原因可能是:_____________________________________________________________。
(5)实验前所取工业纯碱质量为m g,装置C中碱石灰和U形管的总质量为m1 g,加入足量稀硫酸,反应结束后,装置C中碱石灰和U形管的总质量变为m2 g,则上述实验中测得的工业纯碱中Na2CO3的质量分数为___________。
(5)利用上图A、B装置(B中仍用浓硫酸做干燥剂),还可以制取哪些气体?__________________(填两种气体的化学式)。
20、(8分)某铝合金(硬铝)中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如下实验:
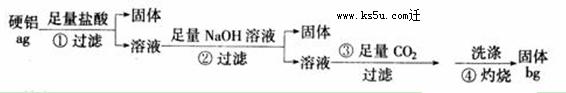
(1) 补全上述①②③④各步反应的离子方程式:
①Mg+2H+===Mg2++H2↑ , ;
②H++OH-==H2O ,Mg2++2OH-===Mg(OH)2↓, ;
③OH-+CO2==HCO3-,__________________________________;
④2A1(OH)3===Al2O3+3H2O
(2)该样品中铝的质量分数是 ;
(3)第②步中加入Na0H溶液不足时,会使测定结果( )
第④步中的沉淀没有用蒸馏水洗涤时,会使测定结果( )
第④步对沉淀灼烧不充分时,会使测定结果( )
A.偏高 B.偏低 C.不影响
19、(4分)试样X由氧化亚铁和氧化铜组成。取等质量的两份试样按下图所示进行实验:

(1)请写出步骤ƒ中所发生的全部反应的离子方程式: 。
(2)若全部的溶液Y和全部的粉末Z充分反应后,生成的不溶物W的质量是m g,则每份试样X中CuO的质量为 (用m表示)。
18、(4分)2001年9月11日,美国世贸大厦轰然倒蹋。在清理废墟中,人们发现很多石棉材料,石棉价格低廉,但是有毒,能使人患肝癌。
有一种石棉叫做石棉矿青石棉,其化学式为Na2Fe5Si8O22(OH)2,分子中铁的化合价为 ,写成氧化物的形式为 ;
17、(8分)写出下列各反应的离子方程式:
(1)向饱和Na2CO3溶液中不断通入二氧化碳,将有晶体析出:
(2)钠投入氯化铁溶液中:
(3)向眀矾溶液中加足量氢氧化钡溶液:
(4)除去Na2CO3溶液中混有的NaHCO3:
21、加热20g由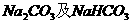 组成混合物,至质量不再发生变化,称得剩余物质的质量变为13.8g.计算(1)原混合物中
组成混合物,至质量不再发生变化,称得剩余物质的质量变为13.8g.计算(1)原混合物中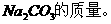
(2)原混合物中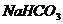 的质量分数。
的质量分数。
20.A.B.C是单质,其中A是金属,各物质间的转化关系如下图根据图示转化关系回答。
(1)写出下列物质的化学式
A_______________________________ B______________________________________
乙_______________________________ 丁______________________________________
(2)写出下列变化的方程式
①A与NaOH溶液反应化学方程式_____________________________________
②乙中加入过量盐酸反应离子方程式__________________________________
(3)将一定量的A加到NaOH溶液中,产生的C在标准情况下的体积为3.36L.则消耗A的物质的量为______________,反应中转移电子的数目为___________________.
19.某课外活动小组设计了下图所示的实验装置进行实验,请回答下列问题。
(1)实验开始时弹簧夹e是打开的,A中发生反应的化学方程式为______________________.
B中可观察到的现象是_______________________________。
(2)数分种后夹上弹簧夹e,B中可观察到的现象是_____________________________
B中反应的离子方程式为________________________________________。
(3)如果开启活塞f放掉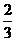 的液体,B中可能出现的现象是_____________________________,B中反应的化学方程式为______________________________________
的液体,B中可能出现的现象是_____________________________,B中反应的化学方程式为______________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com