
题目列表(包括答案和解析)
3.科学家已发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H3和H2相同的是( )
A.原子数 B.分子数 C.体积 D.物质的量
2.悬浊液、乳浊液、溶液和胶体都是( )
A.稳定的液体 B.透明的液体 C.混合物 D.化合物
1.下列物质属于非电解质的是( )
A.HCl B.NaOH C. NaHCO3 D. CO2
21.向一定量的Fe、FeO、Fe2O3混合物中加入1.00mol/l的盐酸100ml,可恰好使混合物完全溶解,放出224ml标准状况下的气体,向所得溶液中加入硫氰化钾,无血红色出现。
(1)若用足量的CO在高温下还原相同质量的混合物,能得到铁的质量是多少?
20.(9分)欲用浓硝酸法测定某铜银合金中铜的质量分数(测定反应后生成气体的量),但资料表明:①反应中除生成NO2气体外还有少量NO生成;②常温下NO2和N2O4混合存在,在低于0℃时,几乎只有无色的N2O4液体或晶体存在。为完成测定并验证确有NO生成,有人设计了如图所示的实验装置。
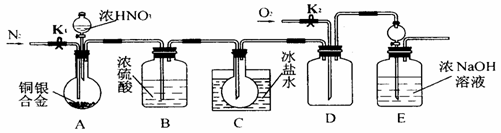
(1)实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是___________________________________________。
(2)装置中B瓶的作用是 。
(3)A中的反应停止后,打开D中的活塞K2,并通入氧气,若反应确有NO产生,则D中应出现的现象是_______________________________________。
(4)为减少测量误差,在A中反应完成和D中出现现象后,还应继续进行的操作是___________。
(5)C装置烧瓶中的物质是 ,用简单的实验证实你的判断: 。
(6)实验已测出一定质量的铜银合金完全反应后E装置的生成物中含氮元素的质量,为确定合金中铜的质量分数还需测定的数据是____________________________。
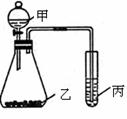
19.(12分)利用下图装置采用适当试剂可完成实验某探究实验,并得出相应实验结论,实验所用试剂或所得结论列于表中。请回答:
|
实验试剂 |
实验结论 |
||
|
甲 |
乙 |
丙 |
|
|
① |
高锰酸钾 |
② |
氧化性:KMnO4>Cl2>Br2 |
 (1)图中①为
,②为
。
(1)图中①为
,②为
。
 (2)请你根据上述实验装置再设计一个实验,并将选择的试剂、丙中的现象以及根据实验现象得出的实验结论填入下表;(不允许再验证氧化性顺序)
(2)请你根据上述实验装置再设计一个实验,并将选择的试剂、丙中的现象以及根据实验现象得出的实验结论填入下表;(不允许再验证氧化性顺序)
|
试剂甲 |
试剂乙 |
试剂丙 |
丙中现象 |
实验结论 |
|
|
|
|
|
|
18.(8分)从海水中可以获得淡水、食盐,并可提取镁和溴等物质;其中海水淡化的常用方法主要有 (填一种)。
从海水中提取溴和镁的流程如下图所示:

(1)提取Br2时第一次通入Cl2后发生反应的离子方程式是 ;反应中②中SO2表现出___ (填“氧化”或“还原”)性;
第二次通入Cl2后,要提取Br2还要进行的操作为 ]
(2)为了实现对镁离子的富集,①中加入的足量试剂是 _____ (填化学式);
试从节约能源,提高金属镁的纯度分析,以下最适宜的冶炼的方法是 (填字母)。
A.Mg(OH)2 MgO
MgO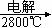 Mg
Mg
B.Mg(OH)2 MgO
MgO Mg
Mg
C.Mg(OH)2 无水MgCl2
无水MgCl2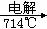 Mg
Mg
D.Mg(OH)2 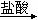 MgCl2溶液
MgCl2溶液 Mg
Mg
17.(8分)可逆反应的特点是同一反应,能同时向相反的两个方向,充分反应后最终各种物质共存在一起。现将0.2molSO3放在某密闭容器中加热使其分解:2SO3 2SO2+O2。
2SO2+O2。
(1)容器中SO2与O2分子数目比为___________,质量比为__________
(2)最终容器内硫原子与氧原子个数比为__________
(3)反应中,气体分子数目_________(填增加、减少、不变),将充分反应后的混合气体通入适量的BaCl2溶液中,生成的沉淀是_____________;若是通入到足量的NaOH 溶液中,则生成的盐化学式为________________________
16.(8分)已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
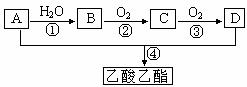
回答下列问题:
(1)写出A的电子式 。
(2)B、D分子中的官能团名称分别是 、 。
(3)写出下列反应的反应类型: ① ,④ 。
(4)写出下列反应的化学方程式:
① ;
② ;
15.amol的下列物质分别与足量的稀硝酸反应(假设还原产物只有一种),消耗硝酸的物质的量均可看作两部分,一部分为作氧化剂的硝酸,另一部分为作酸的(即以硝酸根离子的形式存在于反应后的溶液中维持溶液的电中性),下列各选项中正确的是(单位:mol)
( )
①Fe:3a+a ; ②Fe3O4:9a+ ;
③Fe(OH)2:3a+ ; ④FeSO4:a+
A.①②③④ B.只有①② C.只有③④ D.只有①②③
第II卷(满分55分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com