
题目列表(包括答案和解析)
19.(10分)MnO2和浓盐酸在一定温度下反应会生成黄绿色的氯气。其变化可表述为:
MnO2+4HCl(浓)===MnCl2+Cl2↑+2H2O
(1)用线线桥法表示该反应转移的电子数目和方向_______________ ____________
(2)浓盐酸在反应中显示出来的性质是________________(填写编号,多选倒扣)。
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(3)该反应的氧化剂是______ 氧化产物是______
(4)产生0.1molCl2,则转移的电子的物质的量为______mol。被氧化的HCl的物质的量是_______mol
18.(12分)(1)下列物质能导电的是 ,(均填标号)属于电解质的是 ,
属于非电解质的是 。
①水银 ②烧碱 ③碳酸钙 ④氯化钠晶体 ⑤盐酸 ⑥氨气 ⑦蔗糖 ⑧氯气 ⑨液态氯化氢 ⑩硫酸溶液
(2)按要求写出下列方程式:
① KAl(SO4)2电离的电离方程式:
② 小苏打与氢氧化钠溶液反应的离子方程式:
③ 澄清石灰水中通入过量二氧化碳反应的离子方程式:
17、(12分)(1)CCl4和蒸馏水都是无色液体,请按下列要求用实验方法鉴别之(简要地写出实验过程)
① 只允许用一种试剂
② 不用任何试剂
(2)NaCl溶液中含有少量的CaCl2,某学生用过量的Na2CO3使Ca2+离子转化为沉淀而除去,确认Na2CO3已过量的实验方法是
(3)在配制一定体积的溶液中,下列操作使得到的溶液浓度偏高、偏低还是无影响?
(1)将溶解溶质的烧杯内的液体倒入容量瓶后,未洗涤烧杯就进行定容。
________________________________________________________________________
(2)定容时,液面超过容量瓶颈上的刻度线,用胶头滴管将过量的液体吸出。
________________________________________________________________________
(3)定容摇匀后,发现瓶内液面略低于瓶颈刻度线。
________________________________________________________________________
16.相对分子质量为M的气态化合物V L(标准状况),溶于mg水中,得到质量分数为w%的溶液,物质的量浓度为cmol/L,密度为ρ g·cm-3,则下列说法正确的是 ( )
A.相对分子质量M=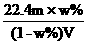 B.物质的量浓度c=
B.物质的量浓度c=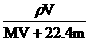
C.溶液的质量分数w%=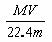 D.溶液密度ρ=
D.溶液密度ρ=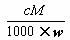
第II卷(共52分)
15.下列反应的离子方程式书写正确的是( )
A.稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑
B.氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-=BaSO4↓
C.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑
D.氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu
14.两份质量相同的CH4和NH3比较,下列结论错误的是 ( )
A.分子个数比为17∶16 B.原子个数比为17∶16
C.氢原子个数比为17∶12 D.氢原子质量比为17∶12
12.在碱性溶液中能大量共存且溶液为无色透明的离子组是( )
A.K+ 、MnO4-、Na+、Cl- B.K+、Na+、NO3-、CO32-
C.Na+、H+、NO3-、SO42- D.Fe3+、Na+、Cl-、SO42-
13.能用H++OH-=H2O表示的化学反应是( )
A.稀硫酸与氢氧化钡溶液反应 B.稀盐酸与氢氧化钠溶液反应
C.稀盐酸与氢氧化铜反应 D.稀硝酸与氢氧化铝反应
11.某溶液中只含有Na+、Al3+、Cl-、SO42- 四种离子,已知前三种离子的个数比为3∶2∶1,则溶液中Al3+和 SO42-的离子个数比为( )
A.1∶2 B.1∶4 C.3∶4 D.3∶2
10.用NA表示阿伏德罗常数,下列叙述正确的是( )
A.标准状况下,22.4LH2O含有的分子数为1 NA
B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C.通常状况下,1 NA 个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol·/L的MgCl2溶液中,含有Cl- 个数为1 NA
9.下列叙述正确的是( )
A.1 mol H2O的质量为18g/mol B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g D.标准状况下,1 mol任何物质体积均为22.4L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com