
题目列表(包括答案和解析)
2.下列电离方程式中,正确的是( )
A.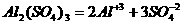 B.
B.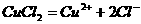
C.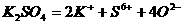 D.
D.
1.下列物质属于非电解质的是( )
A.金属钠 B.CaCl2 C.H2SO4 D.SO2
26.(14分)甲溶液可能含有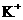 、
、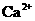 、
、 、
、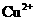 、
、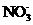 、
、 、
、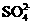 、
、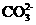 八种离子中的若干种。为确定甲溶液的组成,将其分成两等份,进行如下实验:
八种离子中的若干种。为确定甲溶液的组成,将其分成两等份,进行如下实验:
①向一份溶液中加入足量的 浓溶液并加热,产生的气体在标准状况下体积为4.48L。
浓溶液并加热,产生的气体在标准状况下体积为4.48L。
②向另一份溶液中加入0.6mol/L的 溶液500mL,恰好可以与溶液中的离子完全反应,过滤得66.3g沉淀及滤液。
溶液500mL,恰好可以与溶液中的离子完全反应,过滤得66.3g沉淀及滤液。
③向上述沉淀中加入过量的盐酸,产生的气体通入足量澄清的石灰水中,得到一定量的沉淀X。
④向上述滤液中加入1mol/L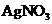 溶液650mL,恰好可完全反应。据此,请回答下列问题(用相应的离子符号表示):
溶液650mL,恰好可完全反应。据此,请回答下列问题(用相应的离子符号表示):
(1)上述实验③中得到沉淀X的质量为__________________;生成沉淀X的离子方程式为_____________________________________。
(2)甲溶液中一定不存在的离子是______________;可能存在的离子是____________。
(3)甲溶液一定存在的离子中,物质的量最大的离子是___________;物质的量最小的离子是_____________,此物质的量最小的离子其物质的量为____________。
孝感高中2010-2011学年度上学期期中考试
25.(8分)标准状况下,向10L由 、
、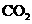 、
、 、
、 组成的混合气体中通入
组成的混合气体中通入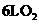 ,用电火花引燃,使之充分反应后,测得气体体积为7.5L,将这些气体通入盛有过量
,用电火花引燃,使之充分反应后,测得气体体积为7.5L,将这些气体通入盛有过量 溶液的洗气瓶气体的体积变为2L,这2L气体的密度是相同状况下
溶液的洗气瓶气体的体积变为2L,这2L气体的密度是相同状况下 密度的15.5倍。则原混合气体中各种气体的体积(以上数据均在标准状况下测定)为:
密度的15.5倍。则原混合气体中各种气体的体积(以上数据均在标准状况下测定)为:
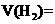 _______________;
_______________;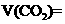 _________________;
_________________;
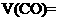 _______________;
_______________;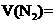 _________________。
_________________。
24.(8分)请将5种物质: 、
、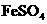 、
、 、
、 和
和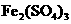 分别填入下面对应的横线上,组成一个未配平的化学方程式。
分别填入下面对应的横线上,组成一个未配平的化学方程式。
(1)_______+_______--_______+_______+_______+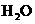 。
。
(2)反应物中发生氧化反应的物质是___________,被还原的元素是____________。
(3)反应中1mol氧化剂___________(填“得到”或“失去”)___________mol电子。
(4)请将反应物的化学式及配平后的化学计量数填入下列相应的位置中:
□________+□________--
23.(8分)氧化还原反应有多种分类方法,其中根据参与电子转移的元素种类不同的分类方法最常见。下列反应中电子转移发生在相同价态的同种元素之间的有________(填反应编号,下同);电子转移发生在不同价态的同种元素之间的有________;电子转移发生在不同元素之间的有__________。下列反应中转移电子数为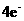 的有_____________。
的有_____________。
①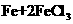 ===
===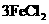
 ②
②
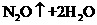
 ③
③

 ④
④
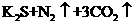
⑤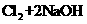 ===
===
 ⑥
⑥
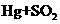
22.(12分)某校学生课外活动小组的同学设计下图所示实验装置,用来验证一氧化碳具有还原性,回答下列问题:
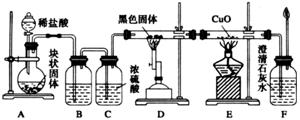
(1)写出装置A中所发生反应的离子方程式:__________________________________。
(2)装置B中的试剂是饱和 溶液,其作用是_______________________。
溶液,其作用是_______________________。
(3)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是____
___________________________________________________________________________。
(4)装置D中反应的化学方程式为___________________________________________。
(5)根据实验中的_____________________________________________________现象,
可证明CO具有还原性,有关反应的化学方程式是________________________________。
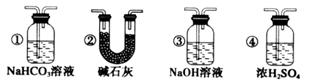
(6)若要根据装置F中澄清石灰水变浑浊的现象确认一氧化碳具有还原性,应在上图装置_________与________之间连接下图中的__________装置(填序号)。
21.(10分)实验室需用 晶体配制
晶体配制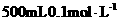 的
的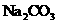 溶液,请回答下列问题。
溶液,请回答下列问题。
(1)应用托盘天平称取 晶体_______g。
晶体_______g。
(2)若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上(1g以下使用游码),天平平衡时,实际称量的 晶体是__________g。
晶体是__________g。
(3)本实验用到的主要仪器有:托盘天平、量筒、烧杯、玻璃棒、________、________。
(4)以下情况会使所配溶液的浓度产生何种影响(填“偏高”、“偏低”、“不变”。):
a.溶解晶体用的烧杯和玻璃棒未洗涤。____________
b.定容时俯视刻度线。____________
c.所用 晶体已失去部分结晶水。____________
晶体已失去部分结晶水。____________
(5)若 晶体中混有少量
晶体中混有少量 固体,且用所配制的
固体,且用所配制的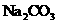 溶液与盐酸反应来测定某盐酸的物质的量浓度,所测盐酸的浓度会________。(填“偏高”、“偏低”、“不变”。)
溶液与盐酸反应来测定某盐酸的物质的量浓度,所测盐酸的浓度会________。(填“偏高”、“偏低”、“不变”。)
20.某学生用 和
和 组成的混合物与盐酸反应并进行实验,测得如下数据(盐酸的物质的量浓度相等)
组成的混合物与盐酸反应并进行实验,测得如下数据(盐酸的物质的量浓度相等)
|
|
50mL盐酸 |
50mL盐酸 |
50mL盐酸 |
|
m(混合物) |
9.2g |
15.7g |
27.6g |
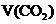 (标准状况) (标准状况) |
2.24L |
3.36L |
3.36L |
则下列分析推理中不正确的是( )
A.盐酸的物质的量浓度为
B.根据表中数据能计算出混合物中 的质量分数
的质量分数
C.加入混合物9.2g的一组实验中盐酸过量
D.15.7g混合物恰好与盐酸完全反应
第Ⅱ卷(非选择题,共60分)
19.如图所示,横坐标表示燃烧时消耗可燃气体X(X=A、B、C)的体积V(X),纵坐标表示消耗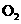 的体积
的体积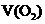 ,A、B是两种可燃气体,C是A和B的混合气体,则C中n(A):n(B)为( )
,A、B是两种可燃气体,C是A和B的混合气体,则C中n(A):n(B)为( )
A.2:1 B.1:2 C.1:1 D.任意比
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com