
题目列表(包括答案和解析)
22.有下列6种物质:Na2SO4、Na2SO3、K2SO4、I2、H2SO4、KIO3组成一个氧化还原反应,请回答下列问题:
(1)将这6种物质分别填入下面对应的横线上,组成一个未配平的化学方程式:
________+Na2SO3+________→________+________+________+H2O
(2)反应物中发生氧化反应的物质是_________(填化学式),被还原的元素是_______。
(3)反应中1mol氧化剂_______(填“得到”或“失去”)________mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:
□__________ +□__________ +□__________ →
安陆二中 应城二中 孝昌二中 英才外校 航天中学
2010-2011学年度上学期期中联合考试
21.取100mL Na2CO3和Na2SO4的混合溶液,加入适量Ba(OH)2溶液100 mL后,恰好完全反应,过滤、干燥后得到14.51g白色沉淀,再用足量的稀硝酸处理沉淀,最后减少到4.66g,并有气体放出。计算(请写出计算过程,没有过程不得分)
(1)原混合液中Na2SO4的物质的量浓度
(2)产生的气体在标准状况下的体积
20.如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。
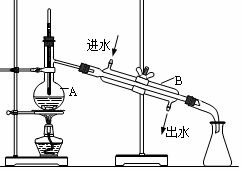
(1)图中的两处明显的错误是
_________________________________ ;_________________________________。
(2)A仪器的名称是____________,B仪器的名称是_______________。
(3)实验时A中除加入少量自来水外,还需加入少量_______,其作用是__________
________________________________ 。
19.今欲用NaHCO3固体配制480mL 0.2mol/L的NaHCO3溶液。根据题意填空:
(1)有以下仪器:①烧杯 ②量筒 ③1000 mL容量瓶 ④500 mL容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码)
配制时,必须使用的仪器有 (填代号),还缺少的仪器
是 、 。
(2)用托盘天平称取 g固体NaHCO3。
(3)将称好的NaHCO3固体放至500mL的大烧杯中,倒入约250mL蒸馏水,用玻璃棒搅拌至完全溶解。待冷却至室温后,将烧杯中的溶液用玻璃棒引流转移至容量瓶。
(4)用少量蒸馏水洗涤烧杯2-3次,并将每次洗涤的溶液都注入容量瓶,轻轻晃动容量瓶,使溶液混和均匀。
(5)向容量瓶中加入蒸馏水,直到液面离刻度线约1-2厘米时,改用胶头滴管 滴加蒸馏水至液面与__________________。盖好瓶塞,摇匀。
(6)配制好的溶液 (填“能”或“不能”)长期存放在容量瓶中。
(7)以下因素会造成实验结果偏低的是 _________
A.定容时观察液面仰视
B.定容后发现液面低于刻度线补加蒸馏水
C.有少量NaHCO3溶液残留在烧杯中
D.容量瓶中原来有少量蒸馏水
18.有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、NaCl混合而成,为检验它的成分做了如下实验:
①将固体混合物溶于水,搅拌后得无色透明溶液
②往此溶液中滴加硝酸钡溶液,有白色沉淀生成
③过滤,将沉淀物置于稀硝酸中,发现沉淀全部溶解,试判断:
(1)固体混合物中肯定有 ,肯定没有 ,可能有 。
(2)写出③反应中的离子方程式 ____________________________________________
(3)对可能有的物质,如要检验其是否存在,将如何操作?_______________________
17.(1)在标准状况下,CO和CO2混合气体的质量为36g,体积为22.4L,则CO所占的体积为 L,质量为 g,混合气体中CO2的分子数为 。
(2)3.01×1023个OH-的物质的量为 ,质量为 ,这些OH-与标准状况下体积为 L的NH3的物质的量相等,与 g Na+含有的离子数相同。
16.将标准状况下的a L氯化氢气体溶于1 L水中,得到的盐酸的密度为bg/mL,则该盐酸的物质的量浓度是( )
A.a/22.4 mol·L-1 B.ab/22400 mol·L-1
C.ab/(22400+36.5a) mol·L-1 D.1000ab/(22400+36.5a) mol·L-1
第Ⅱ卷 (非选择题 共52分)
15.在某无色酸性溶液中能大量共存的一组离子是
A.Na+、K+、HCO3-、NO3- B.NH4+、SO42-、Al3+、NO3-
C.Na+、Ca2+、NO3-、CO32- D.K+、MnO4-、NH4+、NO3
14.ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2: 2KClO3+H2C2O4+H2SO4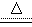 2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是( )
A.KClO3在反应中失电子 B.ClO2是氧化产物
C.H2C2O4在反应中被氧化 D.1 molKClO3参加反应有2mol电子转移
13.混合气体由N2和CH4组成,测得混合气体在标准状况下的密度为0.821g/L,则混合气体中N2和CH4的体积比为( )
A.1∶1 B.1∶4 C.4∶1 D.1∶2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com