
题目列表(包括答案和解析)
24.有下列6种物质:Na2SO4、Na2SO3、K2SO4、I2、H2SO4、KIO3
组成一个氧化还原反应,请回答下列问题:
(1)将这6种物质分别填入下面对应的横线上,组成一个未配平的化学方程式:
________+Na2SO3+________→ Na2SO4 +________+________+H2O
(2)反应物中发生氧化反应的物质是_________(填化学式),被还原的元素是_______。
(3)反应中1mol氧化剂_______(填“得到”或“失去”)________mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:
□__________ +□__________ +□__________ →




23.将碱溶液A、盐溶液B按如下程度进行实验,根据下述现象判断:
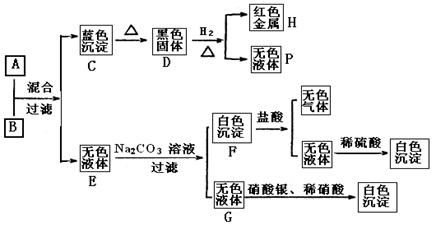
(1)A的化学式 B的化学式 。
(2)完成下列转化的化学方程式,并用单线桥标明电子转移的方向和数目:
D→H+P:
(3) 写出下列反应的离子方程式:
A+B:
F+盐酸:
22.今欲用NaHCO3固体配制480mL 0.2mol/L的NaHCO3溶液。根据题意填空:
 (1)有以下仪器:①烧杯 ②量筒 ③1000 mL容量瓶 ④500 mL容量瓶 ⑤玻璃棒
(1)有以下仪器:①烧杯 ②量筒 ③1000 mL容量瓶 ④500 mL容量瓶 ⑤玻璃棒
⑥托盘天平(带砝码)
配制时,必须使用的仪器有 (填代号),还缺少的仪器
是 、 。
 (2)用托盘天平称取 g固体NaHCO3。
(2)用托盘天平称取 g固体NaHCO3。
 (3)将称好的NaHCO3固体放至500mL的大烧杯中,倒入约250mL蒸馏水,用玻璃棒
(3)将称好的NaHCO3固体放至500mL的大烧杯中,倒入约250mL蒸馏水,用玻璃棒
搅拌至完全溶解。待冷却至室温后,将烧杯中的溶液用玻璃棒引流转移至容量瓶。
 (4)用少量蒸馏水洗涤烧杯2-3次,并将每次洗涤的溶液都注入容量瓶,轻轻晃动容
(4)用少量蒸馏水洗涤烧杯2-3次,并将每次洗涤的溶液都注入容量瓶,轻轻晃动容
量瓶,使溶液混和均匀。
 (5)向容量瓶中加入蒸馏水,直到液面离刻度线约1-2厘米时,改用胶头滴管 滴加蒸
(5)向容量瓶中加入蒸馏水,直到液面离刻度线约1-2厘米时,改用胶头滴管 滴加蒸
馏水至液面与__________________。盖好瓶塞,摇匀。
 (6)配制好的溶液
(填“能”或“不能”)长期存放在容量瓶中。
(6)配制好的溶液
(填“能”或“不能”)长期存放在容量瓶中。
 (7)以下因素会造成实验结果偏低的是
_________
(7)以下因素会造成实验结果偏低的是
_________
 A.定容时观察液面仰视 B.定容后发现液面低于刻度线补加蒸馏水
A.定容时观察液面仰视 B.定容后发现液面低于刻度线补加蒸馏水
C.有少量NaHCO3溶液残留在烧杯中 D.容量瓶中原来有少量蒸馏水
21.草木灰中含有可溶性钾盐(主要成分是K2SO4、K2CO3、KCl)。某学生按下列操作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤.取滤液;③蒸发滤液;④冷却结晶。
(1)在①、②、③、④的操作中需要用到玻璃棒是 (填序号)。
(2)为检验草木灰中的离子,取少量晶体溶于水,并把溶液分成四份,完成以下实验报告(在横线上填写相关的内容):
|
实验步骤 |
实验现象 |
实验结论 |
ⅰ、取第一份溶液和适量稀盐酸加入下列装置的试管中,把澄清的石灰水加入烧杯中  |
, 澄清的石灰水变浑浊 |
证明含有碳酸根离子 |
|
ⅱ、取第二份溶液,分别滴加 和 |
|
证明含有硫酸根离子 |
|
ⅲ、取第三份溶液加入过量BaCl2溶液,过滤,除去SO42-和CO32-,再滴加AgNO3溶液和稀硝酸 |
有白色沉淀生成 |
证明含有氯离子。 |
|
ⅳ、取第四份溶液进行焰色反应 |
透过蓝色钴玻璃火焰呈紫色 |
证明含有K+ |
(3)步骤ⅲ所得的结论,你认为是否正确? (填是或否);为什么?
。
(4)写出步骤ⅱ有关现象的离子方程式 。
20.ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:
2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是( )
A.H2C2O4在反应中被氧化
B.KClO3在反应中得到电子
C.CO2是还原产物
D.4 molKClO3参加反应有8 mol电子转移
第Ⅱ卷 (非选择题,共52分)
19.相同质量的Na、Mg、Al分别与过量的盐酸反应,在相同条件下置换出H2的体积比是
A. 1∶2∶3 B. 23∶12∶9 C. 9∶12∶23 D. 36∶69∶92
18.下列化学反应中,离子方程式表示正确的是
A.石灰石溶解在稀HCl中 CO32-+ 2H+ == CO2↑+ H2O
B.铁屑在稀H2SO4作用下产生H2 Fe + 2H+ === Fe2+ + H2↑
C.金属铝溶于氢氧化钠溶液 Al + 2OH- = AlO2- + H2
D.硫酸铜溶液与氢氧化钡溶液混合 Cu2+ + 2OH- == Cu(OH)2↓
17.对某无色溶液进行酸碱性测定,测得结果呈强酸性。则下列各组离子一定不可能大量存在的是
A.Na+、Mg2+、Cl-、SO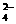 B.Mg2+、Ca2+、HCO
B.Mg2+、Ca2+、HCO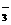 、Cl-
、Cl-
C.Ba2+、Al3+、Cl-、NO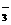 D.K+、Cu2+、Cl-、SO
D.K+、Cu2+、Cl-、SO
16.下列说法正确的是(NA表示阿伏加德罗常数的值)
A.1mol H2中含有的电子数为2NA
B.22.4L氧气所含的氧原子数为2NA
C.常温常压下,28g氮气所含的原子数为2NA
D.1molNa作为还原剂可得到的电子数为NA
15. 在AgNO3、Cu(NO3)2和Zn(NO3)2混合溶液中,加入一定量的铁粉,充分反应后过滤,在滤渣中加入稀盐酸,有气体产生。则下列结论正确的是
A.滤液中一定有Fe(NO3)3
B.滤渣只含Ag和Cu,一定无Zn
C.滤渣中一定有Ag、Cu和Fe,一定无Zn
D.滤渣中一定有Ag、Cu、Fe和Zn
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com