
题目列表(包括答案和解析)
4.下列对于“摩尔”的理解正确的是
A.摩尔是国际科学界建议采用的一种物理量
B.摩尔是物质的量的单位,简称摩,符号为mol
C.摩尔可以把物质的宏观数量与微观粒子的数量联系起来
D.国际上规定,0.012kg碳原子所含有的碳原子数目为1摩
3.分类是化学学习和研究的常用手段。下列分类依据和结论都正确的是
A.HNO3、浓H2SO4都是含氧酸
B.H2O、Cu2(OH)2CO3均含有氧元素,都是氧化物
C.CH3COOH、CH3CH2OH都易溶于水,都是电解质
D.CH3COOH、H2SO4分子中均含有两个氢原子,都是二元酸
2.下列实验操作中错误的是
A.用规格为10mL的量筒量取6.0mL的液 B.用药匙或者纸槽把粉末状药品送入试管的底部
C.过滤时玻璃棒的末端应轻轻靠在三层的滤纸上
D.如果没有试管夹,可以临时手持试管给固体或液体加热
1.下列实验仪器不宜直接用来加热的是
A.试管 B.坩埚 C.蒸发皿 D.烧杯
25.(8分)向100mLBa(OH)2溶液中加入过量的NaHCO3溶液生成BaCO3沉淀,过滤,将沉淀置于过量盐酸中,在标准状况下收集到4.48L气体。将滤液加水稀释至250mL,取出25mL恰好与20mL盐酸完全反应并收集到1.12L(标准状况下)气体。
(1)Ba(OH)2与过量的NaHCO3溶液反应的化学方程式 。
(2)生成BaCO3沉淀的质量__________g。
(3)100mL Ba(OH)2溶液中溶质Ba(OH)2的物质的量浓度__________mol/L。
(4)最初加入的NaHCO3溶液中含NaHCO3的物质的量__________mol。
24.(16分)下面是用98%的浓H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的500mL稀H2SO4溶液的操作,请按要求填空:
(1)所需浓H2SO4的体积为 mL。
(2)如果实验室有15mL、20mL、50mL量筒,应选用 mL量筒最好。量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将 (偏高、偏低、无影响)。
(3)将量取的浓H2SO4沿烧杯内壁慢慢注入盛有约100mL蒸馏水的 里,并不断搅拌。
(4)将冷却至室温的上述溶液沿 注入 中,并用蒸馏水洗涤烧杯2-3次,洗涤液也要注入其中,并摇匀。
(5)加水至距刻度线下 cm时,改用 加水,使溶液的凹液面正好跟刻度相切。
23.(10分)下列三组物质中,均有一种物质的类别与其它三种不同
A.MgO、Na2O、CO2、CuO
B.HCl、H2O、H2SO4、HNO3
C.NaOH、Na2CO3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):A ;B ;C 。
(2)这三种物质相互作用可生成一种新物质NaHCO3,该反应 (“是”或“不是”)
氧化还原反应。
(3)写出物质C与足量稀硫酸溶液反应的离子方程式: 。
22.(8分)某溶液有Cl-、CO32-、SO42-等,今要求在一次样液中先后检验出这三种离子,请完成下列实验设计:先加足量__________溶液,生成气泡,确定CO32-存在;再加足量__________溶液,现象是_________,确定SO42-存在;过滤后加__________溶液,现象是生成白色沉淀,确定Cl-存在。
21.(8分)在反应5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O中,氧化剂是__________,还原
剂是__________;氧化剂具有__________性;被氧化和被还原的原子数之比是__________。
20. 把a L含(NH4)2SO4和NH4NO3 的混合液分为两等份:一份加入bmol 烧碱并加热,恰好把NH3全部赶出,另一份需含c molBaCl2溶液,使沉淀反应刚好完全,则NO3ˉ的浓度是
A. 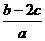 mol/L
B.
mol/L
B. 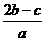 mol/L
mol/L
C.
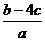 mol/L
D.
mol/L
D.  mol/L
mol/L
第Ⅱ卷(非选择题 共50分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com