
题目列表(包括答案和解析)
4.市场上出售含碘盐的包装袋上明确写明“煮好菜后下盐保持碘效”及“防潮、防热、避光”贮存。请你根据碘元素在自然界的分布、存在形式以及有关性质对说明书的注意事项加以评论,并设计两种试纸,方便准确地测试含碘盐以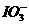 还是I-形式存在。
还是I-形式存在。
已知碘化物某些性质如下表所列:
|
|
KI |
NaI |
KIO3 |
NaIO3 |
|
m·p |
681
℃ |
661
℃ |
560
℃ |
分解 |
|
b·p |
1 330 ℃ |
1 304 ℃ |
>1 000 ℃ |
开始分解 |
思路解析:(1)碘在自然界主要以KI(NaI)或NaIO3(KIO3)形式存在。
KIO3加热会分解:2KIO3 2KI+3O2↑(高温下)
2KI+3O2↑(高温下)
KI也易于被氧化:2KI+1/2O2+H2O====KOH+I2
正如包装说明中所写,加碘盐无论加入的是KIO3、KI(或NaIO3、NaI),均不宜长期高温受热,且应尽量避光保存,因此说明书要求炒菜后才加碘盐,以确保碘效。
5I-+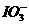 +6H+====3I2+3H2O
+6H+====3I2+3H2O
分析试纸:(1)自制KI淀粉试纸检测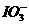 :取少许食盐,并加入1-2滴0.1
mol·L-1 HCl,使试纸与之接触,若试纸变蓝,说明食盐中含KIO3(或NaIO3)。
:取少许食盐,并加入1-2滴0.1
mol·L-1 HCl,使试纸与之接触,若试纸变蓝,说明食盐中含KIO3(或NaIO3)。
(2)自制KIO3淀粉试纸检测I-:取少许食盐,并加入1-2滴0.1 mol·L-1 HCl,使试纸与之接触,若试纸变蓝,说明食盐中含KI或NaI。
答案:KI或KIO3。自制KI淀粉试纸或自制KIO3淀粉试纸。
3.为确定氯水的新制溶液进行如下实验,请填写下表:
|
操作步骤 |
实验现象 |
实验结论及有关反应的离子方程式 |
|
①取少量溶液于一试管中,加入镁粉 |
有无色可燃性气体生成 |
|
|
②在一试管中取少量溶液,加入AgNO3溶液和稀HNO3 |
有白色沉淀生成 |
|
|
③在一试管中取少量溶液,加入NaBr粉末少许及少量CCl4,振荡 |
CCl4层由无色变为橙红色 |
|
|
④将蓝色布条投入该溶液中 |
布条蓝色褪去 |
|
根据以上事实,完成下列问题:
(1)该物质溶液中有哪些分子及离子________________________________________________。
(2)向该物质溶液中加入紫色石蕊试液,先见石蕊变红,后红色又褪去,其原因是________
_______________________________________________________________________________。
思路解析:加入镁粉有氢气产生,说明溶液中有大量的氢离子存在;加入酸化的硝酸银溶液有白色沉淀产生,说明溶液中存在着氯离子;能将溴化钠溶液中的溴置换出来,说明溶液中有氯分子;可使蓝色布条褪色,说明溶液中存在着次氯酸。
答案:
|
操作步骤 |
实验现象 |
实验结论及有关反应的离子方程式 |
|
①取少量溶液于一试管中,加入镁粉 |
有无色可燃性气体生成 |
有氢气产生,说明溶液中存在着大量H+;Mg+2H+====Mg2++H2↑ |
|
②在一试管中取少量溶液,加入AgNO3溶液和稀HNO3 |
有白色沉淀生成 |
有白色沉淀生成,说明溶液中存在着大量Ag+;Ag++Cl-====AgCl↓ |
|
③在一试管中取少量溶液,加入NaBr粉末少许及少量CCl4,振荡 |
CCl4层由无色变为橙红色 |
氯气将溴化钠中的溴置换出来了,说明溶液中存在着氯分子;Cl2+2Br-====Br2+2Cl- |
|
④将蓝色布条投入该溶液中 |
布 条 蓝 色褪去 |
具有漂白性,说明溶液中存在着次氯酸 |
(1)Cl2、HClO、H2O、H+、Cl-、ClO-及少量的OH-(水电离的)
(2)溶液呈酸性,所以可以使石蕊显红色;溶液中还有次氯酸,接着将溶液漂白了
2.下列说法正确的是( )
A.漂白粉的有效成分是氯酸钠 B.氟化氢在空气中呈现白雾,这种白雾有剧毒
C.碘化钾水溶液能使淀粉变蓝 D.氟气通入水中有氧气生成
思路解析:A项中漂白粉是将氯气通入石灰乳中所得,它的有效成分是次氯酸钙;C项中能使淀粉变蓝的是I2而不是I-。
答案:BD
1.冰箱制冷剂氟氯甲烷在高空中受紫外线辐射产生Cl原子,并进行下列反应:Cl+O3→ClO+O2,ClO+O→Cl+O2下列说法不正确的是 ( )
A.反应后将O3转变为O2 B.Cl原子是总反应的催化剂
C.氟氯甲烷是总反应的催化剂 D.Cl原子反复起分解O3的作用
思路解析:此反应式为:2O3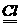 3O2,从反应的特征和催化剂的定义可以判断:Cl起催化作用。
3O2,从反应的特征和催化剂的定义可以判断:Cl起催化作用。
答案:C
5.从以下公共安全事件中,你能得到关于氯气性质的一些什么信息?
马来西亚中部怡保市郊区2010年3月22日下午发生氯气中毒事件,造成近千人受到不同程度的中毒,其中有16人中毒较重,被送入怡保中央医院治疗。
2004年4月15日下午,处于主城区的重庆天原化工总厂氯氢分厂工人在操作中发现,2号氯冷凝器出现穿孔,有氯气泄漏,厂方随即进行处置。16日1时左右,裂管发生爆炸;凌晨4时左右,再次发生局部爆炸,大量氯气向周围弥漫。由于附近民居和单位较多,重庆市连夜组织人员疏散居民。16日17时57分,5个装有液氯的氯罐在抢险处置过程中突然发生爆炸,事故共造成9人死亡和失踪,3名重伤已脱离生命危险。死伤人员均为天原化工总厂领导技术人员和职工。事故发生后,重庆市消防特勤队员昼夜连续用高压水网(碱液)进行高空稀释,在较短的时间内控制了氯气的扩散。
思路解析:氯气中毒首先说明了氯气有毒的性质;氯气冷凝器出现穿孔说明氯气对金属有一定的腐蚀性;液氯罐在抢险过程中发生爆炸,说明液氯受热后很容易汽化,导致容器内压强过大而爆炸;消防队处理时用高压水网(碱液),说明碱液可以消除氯气的毒性。
答案:氯气有毒;氯气对金属有一定腐蚀性;液氯容易汽化;碱液可吸收氯气消除氯气的毒性。
10分钟训练(强化类训练,可用于课中)
4.观察与思考是学习科学知识的基本方法之一。家里用自来水养金鱼时,总要将自来水晾晒之后才加入鱼缸中。你知道这里面的奥妙吗?
思路解析:用于自来水消毒的是氯气,但氯气是有毒的,直接用来养鱼可能使金鱼中毒。所以必须在使用之前进行晾晒,使溶解在自来水中的氯气全部从自来水中逸出,防止金鱼中毒。
答案:使溶解在自来水中的氯气全部从自来水中逸出,防止金鱼中毒。
3.当你打开家里的自来水龙头时,会闻到一股刺鼻的气味,它是什么?请你试着给大家解释解释。
思路解析:家里的自来水都是消过毒的饮用水,它里面的气味很可能是消毒剂的气味。
答案:它是氯气的气味。因为一般的自来水厂都是采用氯气来给自来水消毒,氯气在自来水中的溶解度不是很大,但在空气中仍然可以闻到刺鼻的气味。
2.检验氯化氢气体中是否混有Cl2,可采用的方法是( )
A.用干燥的蓝色石蕊试纸 B.用干燥有色布条
C.将气体通入硝酸银溶液 D.用湿润的淀粉碘化钾试纸
思路解析:检验氯气采用湿润的KI淀粉试纸,而干燥的有色布条、干燥的蓝色石蕊试纸不能检验氯气。硝酸银溶液则与氯化氢和氯气的现象相同。
答案:D
1.下列元素在化合物中,可变化合价最多的是( )
A.铝 B.氯 C.镁 D.氧
思路解析:铝、镁、氧都没有可变化合价,只有氯的可变化合价多。
答案:B
11.用铜锌合金制成的假金元宝欺骗行人的事件屡有发生。
(1)下列不易区别其真伪的方法是 ( )
A.测定密度 B.放入硝酸中 C.放入盐酸中 D.观察外观
(2)你能判断出:合金的性质与组成合金的某单一金属的性质相同吗?
(3)你能举出生活中常见的合金的例子吗?
思路解析:铜锌合金的外观与金的外观极为相似,所以常有用铜锌合金来冒充金元宝进行诈骗的事例见诸于报端,所以观察外观不易区分假元宝的真伪。但铜锌合金的密度及与硝酸和盐酸反应的性质与金则存在着较大的差异,很容易将其伪装揭开。合金与其组分的性质不一样。生活中这样的合金的例子很多,如铁制品一般都是铁碳合金(只要合理即可)。
答案:(1)D
(2)不一样
(3)生铁、熟铁等
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com