
题目列表(包括答案和解析)
2.下列叙述正确的是( )
A.元素的单质可由氧化或还原含该元素的化合物来制得
B.得电子越多的氧化剂,其氧化性就越强
C.阳离子只能得到电子被还原,只能作氧化剂
D.含有最高价元素的化合物不一定具有强的氧化性
思路解析:A项正确,一般金属用还原其相应化合物的方法获得,非金属用氧化其相应化合物的方法获得;B项将得电子能力与得电子多少混为一谈,实际上氧化性只与得电子能力有对应关系;C项绝对化,也有阳离子如Fe2+可以继续被氧化,作还原剂;D项正确,如H2O中H元素就是最高价,但它只有极弱的氧化性。
答案:AD
1.(2004全国春季高考理综)在下图所表示的粒子中,氧化性最强的是( )
A.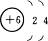 B.
B.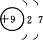 C.
C.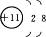 D.
D.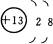
思路解析:氧化性的本质是物质得电子的能力,从粒子结构示意图可以很清楚地知道:最容易得电子的是B项中粒子。
答案:B
4.比较氯化钠和氯化氢的形成过程,总结其区别与联系。
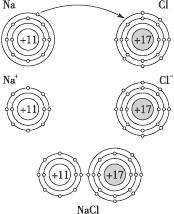

思路解析:分析氯化钠和氯化氢形成过程中电子的得失或转移、化合价的变化情况。
答案:氯元素的原子在氯化钠和氯化氢形成的过程中化合价都降低了,被还原,发生的是还原反应;钠元素的原子失去电子,化合价升高被氧化,发生的是氧化反应;氢元素虽然不能得到电子,但它与氯原子共用的电子对偏离氢原子,氢的化合价升高,被氧化,发生的是氧化反应
10分钟训练(强化类训练,可用于课中)
3.根据以下几种常见元素原子的原子结构示意图,指出它们在化学反应中得失电子的趋势。
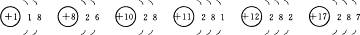
氢 氧 氖 钠 镁 氯
思路解析:最外层电子数越多,电子层数越少,得电子能力越强。
答案:氧和氯主要得电子,钠和镁主要失电子,氢得失电子能力都不强;氖则既不易得电子,又不易失电子。
2.生活中有很多氧化反应,如金属腐蚀、细胞老化。请你总结氧化反应的本质,然后再在你的生活中找一找,还有哪些是氧化反应。
思路解析:金属腐蚀是金属的化合价升高,细胞老化可能是得到了氧原子或失去了氢原子,其实质还是化合价升高。生活中最典型的莫过于燃烧反应,燃烧的物质总是得到氧原子化合价被氧化。
答案:实质是化合价升高。燃烧也是氧化反应。(其他合理答案亦可)
1.将木炭与氧化铜的粉未混合加热,可得到红色的铜。试写出其反应的化学方程式,指出其中的氧化反应与还原反应并考虑它们的关系。
思路解析:C+2CuO 2Cu+CO2↑,从反应过程来看,氧化铜失去氧原子被还原为铜,炭得到氧原子被氧化为二氧化碳,前者为还原反应,后者为氧化反应,两者在一个反应中同时进行,氧原子在两个反应中进行传递。
2Cu+CO2↑,从反应过程来看,氧化铜失去氧原子被还原为铜,炭得到氧原子被氧化为二氧化碳,前者为还原反应,后者为氧化反应,两者在一个反应中同时进行,氧原子在两个反应中进行传递。
答案:氧化铜失去氧原子被还原为铜,炭得到氧原子被氧化为二氧化碳,前者为还原反应,后者为氧化反应,两者在一个反应中同时进行,氧原子在两个反应中进行传递
11.①A、B、C、D四种物质均含有元素X,有的还可能含有元素Y或者Z。元素Y、X、Z的原子序数依次递增。
②X在A、B、C、D中的化合价分别为0、-1、+1、+5。
③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。
④化合物D受热催化分解,可制得元素Y的单质。
请完成下列问题:
(1)写出元素X、Y、Z的元素符号:X._____________________;Y._______________________;Z.________________________。
(2)写出A、B、C、D的化学式:A.________________________;B.________________________;C._________________________;D.________________________。
(3)写出③中反应的化学方程式:________________________________________________。
(4)写出④中反应的化学方程式:________________________________________________。
思路解析:本题的题眼是:具有多种变价的元素是氯,则A、B、C、D均为含有氯元素的物质。再根据实验室用催化分解氯酸钾制氧气的性质,则可将密码解出。
答案:(1) Cl O K
(2)Cl2 KCl KClO KClO3
(3)Cl2+2KOH====KCl+KClO+H2O
(4)2KClO3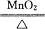 2KCl+3O2↑
2KCl+3O2↑
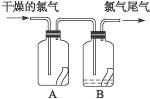
10.(1)如右图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_________________________________________________________。
(2)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用_________________溶液吸收多余的氯气,原理是(用化学方程式表示)________________________________________。根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是______________________(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是______________________(用字母代号填)。
A.O2 B.Cl2 C.CO2 D.HClO
思路解析:(1)为一对比实验,藉此说明干燥的氯气没有漂白作用,而潮湿的氯气有漂白作用。(2)的方法可从题目提示中得到有用的信息,即用碱溶液吸收氯气,效率高。
答案:(1)潮湿的有色布条褪色而干燥的有色布条不褪色
(2)氢氧化钠(NaOH) 2NaOH+Cl2====NaClO+NaCl+H2O Ca(ClO)2 C
9.甲、乙、丙、丁分别是盐酸、碳酸钠、氯化钙、硝酸银4种溶液中的一种,将它们两两混合后,观察到的现象如下表所示,其中丁与乙混合产生的是无色气体。
|
|
甲 |
乙 |
丙 |
丁 |
|
甲 |
- |
↓ |
↓ |
|
|
乙 |
↓ |
- |
↓ |
↑ |
|
丙 |
↓ |
↓ |
- |
↓ |
|
丁 |
|
↑ |
↓ |
- |
请完成下面的问题:
(1)写出丁与乙反应的离子方程式:______________________________________________。
(2)这四种溶液分别是:甲、________________;乙、________________;丙、_______________;丁、_______________。(用溶质的化学式表示)
思路解析:物质推断关键在于题眼的寻找,本题的题眼是高频信息--丙能与另外三种物质都生成沉淀,它肯定是硝酸银;另一高频信息--乙除与丙生成沉淀外,还能与一种物质生成沉淀,与另一种物质产生气体,它是碳酸钠;最后确定丁为盐酸、甲为氯化钙。
答案:(1)2H++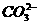 ====H2O+CO2↑
====H2O+CO2↑
(2)CaCl2 Na2CO3 AgNO3 HCl
8.如果实验室中临时没有蒸馏水,可以用自来水配制某些急需的药品,但有些药品若用上述自来水配制,则明显会导致药品变质。下列药品中不能用上述自来水配制的是( )
A.Na2SO4 B.NaCl C.AgNO3 D.AlCl3
思路解析:用氯气消毒后的自来水中含有氯离子,易与加入的AgNO3中银离子反应生成氯化银沉淀。
答案:C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com