
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
1.ЯђзЯЩЋЪЏШяШмвКжаМгШыЙ§СПNa2O2ЗлФЉЃЌеёЕДЃЌПЩЙлВьЕНЕФЯжЯѓЮЊ(ЁЁЁЁ )
A.ШмвКШдЮЊзЯЩЋЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.ШмвКзюжеБфЮЊРЖЩЋ
C.зюжеШмвКЭЪЩЋЃЌЖјЮоЦфЫћЯжЯѓЁЁЁЁЁЁ D.ШмвКжагаЦјХнВњЩњЃЌШмвКзюжеБфЮЊЮоЩЋ
ЫМТЗНтЮіЃК2Na2O2+2H2O====4NaOH+O2ЁќЃЌгабѕЦјВњЩњЃЌЙЪШмвКжагаЦјХнЗХГіЃЌгжвђЮЊNa2O2гаЦЏАзадЃЌЙЪШмвКзюжеБфЮЊЮоЩЋЁЃВЛФмжЛПМТЧЗДгІЩњГЩNaOHЃЌШЯЮЊШмвКБфЮЊРЖЩЋЃЌЖјКіТдNa2O2гаЦЏАзадЁЃ
Д№АИЃКD
10.ТёВидкЕиЯТЕФЧрЭЦїатЪДЙ§ГЬПЩвдБэЪОЮЊЃК
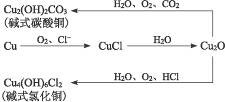
(1)ЧрЭЦїатЪДЙ§ГЬжаЕФВњЮяга__________________________________________________ЁЃ
(2)ЧрЭЦїГіЭСКѓЗРжЙЧрЭЦїМЬајатЪДЕФЙиМќЪЧ____________________________________ЁЃ
ЫМТЗНтЮіЃКЧрЭЦїатЪДЙ§ГЬжаЕФВњЮяДгЭМжаПЩвдЧхГўПДГіЁЃДгЭМжаПДГіатЪДЗДгІЕФЬѕМўЪЧДцдкO2ЁЂЫЎМАЫсадЦјЬхШчCO2ЁЂHClЕШЃЌЦфжаO2ЪЧЙиМќЁЃ
Д№АИЃК(1)CuClЃЌCu2OЃЌCu2(OH)2CO3ЃЌCu4(OH)6Cl2ЕШЁЁ (2)гыH2OКЭO2ЕШИєОј
ПьРжЪБЙт
ЮЈвЛЕФЦђиЄ
ЁЁЁЁ вЛШКгЬЬЋШЫеОдкЯязгРяЃЌУПШЫЖМдкЮЊздМКзЃИЃЃЌгаЕФЯыГЩЮЊИЛЮЬЃЌгаЕФЯыШЂИЛЮЬЕФХЎЖљЃЌ
гаЕФзЃдИЦозгФмЩњИіаЁКЂЁЃдкетШКШЫжаМфгавЛИіЦђиЄЃЌЫћвВрЋрЋЕиЖдЬьЦэЕЛзХЪВУДЁЃ
ЁЁЁЁ ЁАЮЙЃЁЁБгаШЫЮЪЫћЃЌЁАФњЮЊздМКЦэЕЛЪВУДбНЃПЁБ
ЁЁЁЁ ЁАЮвзЃдИздМКЪЧетзљГЧЪаРяЮЈвЛЕФЦђиЄЁЃЁБ
30ЗжжгбЕСЗ(ЙЎЙЬРрбЕСЗЃЌПЩгУгкПЮКѓ)
9.НёгУТСЁЂЯЁСђЫсКЭЧтбѕЛЏФЦШмвКЮЊдСЯЃЌЪЕбщЪвжЦБИвЛЖЈСПЕФЧтбѕЛЏТСЁЃЗжБ№ВЩгУШчЯТЛЏбЇЗНГЬЪНЫљБэЪОЕФСНжжЗНЗЈЃК
Ђй2Al+3H2SO4====Al2(SO4)3+3H2ЁќЁЁ Al2(SO4)3+6NaOH====2Al(OH)3Ё§+3Na2SO4
Ђк2Al+2NaOH+2H2O====2NaAlO2+3H2ЁќЁЁ 2NaAlO2+H2SO4+2H2O====2Al(OH)3Ё§+Na2SO4
(1)ЧыЮЪЩЯЪіФФвЛжжЗНЗЈБШНЯНкдМЪдМСЁЃ(ЬсЪОЃКвдУПЩњВњ2 mol Al(OH)3ЫљКФЗбЕФЪдМСгУСПгшвдЫЕУї)
(2)дСЯЯрЭЌЃЌЧыЩшМЦвЛжжИќЮЊНкдМЪдМСЕФЗНЗЈЁЃ(вдЗНГЬЪНБэЪОЃЌВЂЫЕУїЦфПЩвдзюНкдМЪдМСЕФИљОн)
ЫМТЗНтЮіЃК(1)ДгЛЏбЇЗНГЬЪНПДГіЃЌЭЌбљЪЧжЦБИ2 molЕФAl(OH)3ЃЌЗНЗЈЂйЫљашдСЯЮЊЃК2 mol AlЃЌ3 mol H2SO4ЃЌ6 mol NaOHЃЛЖјЗНЗЈЂкЫљашдбљЮЊЃК2 mol AlЃЌ1 mol H2SO4ЃЌ2 mol NaOHЁЃ
(2)Ђй2Al+3H2SO4====Al2(SO4)3+3H2Ёќ
Ђк2Al+2NaOH+2H2O====2NaAlO2+3H2Ёќ
ЂлAl2(SO4)3+6NaAlO2+12H2O====8Al(OH)3Ё§+3Na2SO4
гЩЗНГЬЪНПДГіЃЌжЦБИ8 molЕФAl(OH)3ЃЌЫљашдСЯЮЊЃК8 mol AlЁЂ3 mol H2SO4ЁЂ6 mol NaOHЁЃЯрЕБгкжЦБИ2 mol Al(OH)3ЃЌЫљашСПЮЊЃК2 mol AlЃЌ3/4 mol H2SO4ЃЌ3/2 mol NaOHЃЌЦфгУСПЮЊзюЩйЁЃ
Д№АИЃК(1)ЕкЂкжжЗНЗЈБШНЯНкдМЪдМСЁЃ
(2)МћНтЮіЁЃ(ЗНГЬЪНЂйКЭЂкЕФЫГађПЩНЛЛЛ)
8.ШєНЋКЌHCl 0.20 molЕФЯЁбЮЫсЕЮШы0.15 mol Na2CO3ЕФШмвКжаЃЌОГфЗжЗДгІКѓЃЌШмвКжаИїШмжЪЕФЮяжЪЕФСПЮЊ(ЕЅЮЛЃКmol)(ЁЁЁЁ )
|
ЁЁ |
Na2CO3 |
HCl |
NaCl |
NaHCO3 |
|
A |
0 |
0 |
0.05 |
0.10 |
|
B |
0.5 |
0 |
0.20 |
0 |
|
C |
0 |
0 |
0.20 |
0.10 |
|
D |
0 |
0.05 |
0.15 |
0.15 |
ЫМТЗНтЮіЃКбЮЫсКЭNa2CO3ЗДгІЃЌгыЕЮМгЫГађгаЙиЃЌгІв§Ц№зуЙЛжиЪгЁЃ
ЗжЮіБОЬтПЩжЊСНЬѕживЊаХЯЂЃК(1)вђЯЁбЮЫсЪЧЕЮШыЕНNa2CO3ШмвКжаЕФЃЌЫљвдетжжЧщПіЯТбЮЫсКЭЬМЫсФЦЕФЗДгІЪЧЗжВННјааЕФЃК
Na2CO3+HCl====NaCl+NaHCO3Ђй
NaHCO3+HCl====NaCl+CO2Ёќ+H2O Ђк
(2)ЗДгІЮябЮЫсЕФСПЯрЖдгкNa2CO3ЕФЕквЛВНЗДгІЪЧЙ§СПЕФ(гр0.05 mol)ЃЌЯрЖдгкNa2CO3ЕФЭъШЋЗДгІЪЧВЛзуСПЕФ(Вю0.10 mol)ЁЃетбљРћгУЬтЪОаХЯЂНјвЛВНЗжЮіПЩжЊЃКГфЗжЗДгІКѓЗДгІЮяNa2CO3КЭHClЖМвбЯћКФЭъШЋЃЛСНВНЗДгІжаЕФHClЖМзЊЛЏЮЊNaClЃЌЦфзЊЛЏЙиЯЕЮЊ1ЁУ1(ЮяжЪЕФСПжЎБШ)ЁЃвђДЫЩњГЩЕФNaClЮЊ0.2 molЃЛЖјNaHCO3ЕФСПдђОвЛВНЗДгІЩњГЩ0.15 mol(АДВЛзуСП)ЃЌЕкЖўВНЗДгІгжзЊЛЏСЫ(ЗХCO2)0.05 molЃЌзюКѓЪЃ0.10 molЁЃ
Д№АИЃКC
7.РТќЙтЦзжЄЪЕШмвКжаВЛДцдк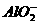 ЃЌЪЕМЪДцдкЃлAl(OH)4Ѓн-ЁЃ200
mL 0.2 molЁЄL-1 NaЃлAl(OH)4ЃнШмвКгы250 mL 0.2 molЁЄL-1ЁЁ H2SO4ЛьКЯЃЌЭъШЋЗДгІКѓЃЌШмвКжаAl3+гы
ЃЌЪЕМЪДцдкЃлAl(OH)4Ѓн-ЁЃ200
mL 0.2 molЁЄL-1 NaЃлAl(OH)4ЃнШмвКгы250 mL 0.2 molЁЄL-1ЁЁ H2SO4ЛьКЯЃЌЭъШЋЗДгІКѓЃЌШмвКжаAl3+гы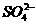 ЮяжЪЕФСПжЎБШЮЊ(ЁЁЁЁ )
ЮяжЪЕФСПжЎБШЮЊ(ЁЁЁЁ )
A.4ЁУ5ЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁB.2ЁУ3ЁЁЁЁЁЁЁЁЁЁЁЁ C.2ЁУ5ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.1ЁУ2
ЫМТЗНтЮіЃК2NaЃлAl(OH)4Ѓн+H2SO4====Na2SO4+2Al(OH)3Ё§+2H2OЃЌ
2Al(OH)3+3H2SO4====Al2(SO4)3+6H2OЁЃ
АДЗДгІЗНГЬЪНЗжСНВНМЦЫуЃКЕквЛВНЃЌСђЫсЙ§СПЃЌЪЃгрСђЫсЮЊ0.3 molЃЌЩњГЩЧтбѕЛЏТС0.2 molЃЛЕкЖўВНЃЌСНжжЗДгІЮяЧЁКУЗДгІЃЌЩњГЩСђЫсТСЃЌДЫЪБШмвКжаAl3+ЮЊ0.2 molЃЌ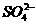 ЮЊ0.5 molЁЃ
ЮЊ0.5 molЁЃ
Д№АИЃКC
6.дкЯѕЫсТСКЭЯѕЫсУОЕФЛьКЯШмвКжаЃЌж№ЕЮМгШыЯЁЧтбѕЛЏФЦШмвКЃЌжБжСЙ§СПЁЃЯТСаБэЪОЧтбѕЛЏФЦМгШыСП(X)гыШмвКжаГСЕэЮяЕФСП(Y)ЕФЙиЯЕЪОвтЭМжае§ШЗЕФЪЧ(ЁЁЁЁ )
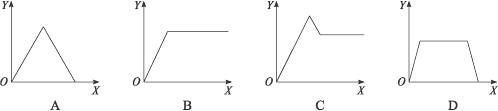
ЫМТЗНтЮіЃКЗДгІЗжЮЊСНИіНзЖЮЃК(1)Al(NO3)3+3NaOH====Al(OH)3Ё§+3NaNO3ЃЌ
Mg(NO3)2+2NaOH====Mg(OH)2Ё§+2NaNO3ЃЛ(2)Al(OH)3+NaOH====NaAlO2+2H2OЁЃГСЕэЪзЯШЪЧж№НЅдіЖрЃЌДяЕНзюДѓжЕКѓЃЌЙ§СПЕФЧтбѕЛЏФЦгжНЋЧтбѕЛЏТСГСЕэШмНтЁЃ
Д№АИЃКC
5.ЯТСаЮяжЪжаЃЌПЩгУгкжЮСЦЮИЫсЙ§ЖрЕФЪЧ(ЁЁЁЁ )
A.ЬМЫсФЦЁЁЁЁЁЁЁЁЁЁЁЁ B.ЧтбѕЛЏТСЁЁЁЁЁЁЁЁЁЁЁЁ C.ЧтбѕЛЏФЦЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.ЬМЫсБЕ
ЫМТЗНтЮіЃКжЮСЦЮИЫсЙ§ЖрЃЌвЛЗНУцвЊФмЯћКФЫсЃЌСэвЛЗНУцБиаыЪЧЮоЖОЁЂЖдШЫЬхУЛгаЧПДЬМЄадЩѕжСИЏЪДзїгУЃЌвВВЛФмВњЩњДѓСПЦјЬхЃЌЪЙЮИжаГфЦјЙ§ЖрЁЃ
Д№АИЃКB
4.ЯђЯТСаШмвКЕЮМгЯЁСђЫсЃЌЩњГЩАзЩЋГСЕэЃЌМЬајЕЮМгЯЁСђЫсЃЌГСЕэгжШмНтЕФЪЧ(ЁЁЁЁ )
A.Na2SiO3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.BaCl2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁC.FeCl3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.NaAlO2
ЫМТЗНтЮіЃКСђЫсгыбЁЯюжаЮяжЪЕФЗДгІЃКNa2SiO3+H2SO4====Na2SO4+H2SiO3Ё§ЃЛBaCl2+H2SO4====BaSO4Ё§+2HClЃЛ2NaAlO2+H2SO4+2H2O====2Al(OH)3Ё§+Na2SO4ЃЌ
2Al(OH)3+3H2SO4====Al2(SO4)3+6H2OЁЃ
Д№АИЃКD
3.ЯТСаа№Ъіе§ШЗЕФЪЧ(ЁЁЁЁ )
A.ВнФОЛвЕФжївЊГЩЗжЪЧK2CO3
B.ЭСШРжаМидЊЫиЕФКЌСПНЯЩйЃЌвђДЫашвЊВЙГф
C.МиЗЪвЫдкЯТгъЧАЪЉгУЃЌвдБуШмНтЮќЪе
D.ЮЊСЫЪЙХЉзїЮягааЇЮќЪеNЁЂPЁЂKЕШдЊЫиЃЌМиЗЪвЫИњNH4H2PO4ЕШЛьКЯЪЉгУ
ЫМТЗНтЮіЃКЭСШРжаЕФМидЊЫиКЌСПВЂВЛЩйЃЌжЛЪЧПЩБЛжВЮяжБНгЮќЪеЕФВПЗжНЯЩйЃЛМиЗЪЖМЪЧвзШмгкЫЎЕФбЮЃЌгъЧАЪЉгУЃЌШнвзБЛгъЫЎСмЪЇЃЛМиЗЪЬиБ№ЪЧЬМЫсМиВЛФмгыяЇбЮЛьгУЃЌвђЮЊЖўепЗЂЩњЗДгІКѓЃЌЪЙяЇбЮзЊЛЏЮЊАБЦјЃЌвнШыПеЦјжаЁЃ
Д№АИЃКA
2.АбЫЎЕЮШыЯТСаЮяжЪжаЃЌВЛВњЩњЦјЬЌЩњГЩЮяЕФЪЧ(ЁЁЁЁ )
A.Й§бѕЛЏФЦЁЁЁЁЁЁЁЁЁЁ B.Н№ЪєФЦЁЁЁЁЁЁЁЁЁЁЁЁЁЁ C.бѕЛЏФЦЁЁЁЁЁЁЁЁЁЁ D.Н№ЪєМи
ЫМТЗНтЮіЃКгыЫЎЗДгІЕФЮяжЪЃЌЪЧНќФъИпПМжаЕФШШЕуЁЃбЁЯюжаЕФЫФжжЮяжЪЖМПЩвдКЭЫЎЗЂЩњЗДгІЁЃЙ§бѕЛЏФЦгыЫЎгабѕЦјВњЩњЃЛН№ЪєФЦКЭМигыЫЎгаЧтЦјВњЩњЁЃ
Д№АИЃКC
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com