
题目列表(包括答案和解析)
(二)欲配1mol/L NaOH溶液250ml,需称取NaOH固体 g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小 (填字母),并在下图中选出能正确表示游码位置的选项 (填字母)。
 附表砝码规格
附表砝码规格
|
|
a |
b |
c |
d |
e |
|
砝码大小/g |
100 |
50 |
20 |
10 |
5 |
20.(一)欲用98%的浓硫酸(ρ=1.84 g·cm-3)配制成浓度为0.25 mol·L-1的稀硫酸500mL。
(1)选用的主要仪器有:①量筒,②烧杯,③ ④ ⑤ 。
(2)请将下列各操作,按正确的序号填在横线上。
A.用量筒量取浓硫酸 B.反复颠倒摇匀 C用胶头滴管滴加水至刻度线 D.洗涤所用仪器 E.稀释浓硫酸 F.将溶液转移到容量瓶中
其操作正确的顺序依次为 。
(3)简要回答下列问题:
①所需浓硫酸的体积为 mL。
②如果实验室有5mL、10mL、20mL、50 mL的量筒,则应选 mL量筒若量取浓硫酸时仰视刻度,将会使结果浓度 (填“偏高”偏低”“无影响”,下同)。
③将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并不断搅拌的目的是 。
在转入容量瓶前烧杯中液体应 ,否则会使结果浓度 ;转移后洗涤烧杯和玻璃棒2-3次,洗涤液也要转入容量瓶,否则会使结果浓度 。
④定容时必须使溶液凹液面与刻度线相平,若俯视会使结果浓度 。
⑤使用洁净的容量瓶前,瓶中残留有少量蒸馏水,使结果浓度 。
19.(8分)已知乙醇的沸点为78.3℃,与水以任意比互溶,且在78.15℃时与水可形成95.57%的恒沸混合物(即水和酒精可同时挥发)。酒精中的水可加入生石灰除去,反应如下:CaO+H2O=Ca(OH)2,CaO和Ca(OH)2均不溶于酒精,加热也难挥发。
某化学活动小组要用35%的酒精制取无水酒精,设计了如下四个方案:
方案一:对35%的酒精直接蒸馏得无水酒精。
方案二:向35%的酒精中直接加入生石灰,然后进行蒸馏得无水酒精。
方案三:用CCl4对35%的酒精进行萃取,然后对酒精的CCl4溶液进行蒸馏得无水酒精。
方案四:先对35%的酒精蒸馏得95.57%的酒精,再加入生石灰,然后进行蒸馏得无水酒精。
请对四个方案进行评价,回答下列问题:
(1)最好的方案是 ,错误的方案是 ,错误的原因是 。
(2)其余方案的不足是 。
(3)用最好的方案进行实验时,所用到的玻璃仪器有酒精灯、牛角管、锥形瓶、 。
18.(12分)(1)某气态氧化物化学式为XO2,在标准状况下,2.56g该氧化物的体积为896mL,则该氧化物的摩尔质量为 ,X的相对原子质量为 。
(2)已知CO、CO2混合气体质量共29g,标准状况下体积为16.8L,则可推知该混合气体中含CO g,所含CO2的标准状况下体积为 L,此混合气体对H2的相对密度为 。
(3)同温同压下,SO2与氦气的密度之比为 ,若质量相同,两种气体的体积比为 ;若体积相同时,两种气体的质量比为 。
(4)已知某硫酸溶液甲:C甲mol/L,V甲mL ,ρ甲g·cm-3
某硫酸溶液乙:C乙mol/L,V乙mL ,ρ乙g·cm-3
将甲、乙各取V mL混合,混合液密度为ρg·cm-3,则混合液中C混= mol/L(选择以上字母表达计算式,要求化简)。
17.(6分)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液 B.升华 C.结晶 D.分液 E.蒸馏 F.过滤 G.洗气
(1) 分离饱和食盐水与沙子的混合物。
(2) 从硝酸钾和氯化钠的混合溶液中获得硝酸钾。
(3) 分离水和CCl4的混合物。
(4) 分离汽油、煤油的混合物。
(5) 分离碘的CCl4溶液。
(6) 干燥H2。
16.把1000mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为( )
A.5(b-2a)mol·L-1 B.10(2a-b)mol·L-1
C.(b-a)mol·L-1 D.0.1(b-2a)mol·L-1
15. 如图所示是医院中病人输液使用的一瓶质量分数为5%的葡萄糖(C6H12O6)
注射液标签,请认真观察标签上所列内容,正确的是( )
如图所示是医院中病人输液使用的一瓶质量分数为5%的葡萄糖(C6H12O6)
注射液标签,请认真观察标签上所列内容,正确的是( )
A.溶液密度为1g·L-1
B.5%的葡萄糖溶液与等质量的水混合后,质量
分数小于2.5%
C.5%的葡萄糖溶液与10%的葡萄糖溶液等体积
混合后,溶液质量分数大于7.5%
D.溶质的物质的量浓度约为0.28mol/L
14.20℃时,饱和KCl溶液的密度为1.174g·cm-3,物质的量浓度为4.0mol·L-1, 则下列说法中,正确的是( )
①25℃时,饱和KCl溶液的浓度大于4.0mol·L-1 ②此溶液中KCl的质量分数为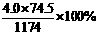 ③20℃时,密度小于1.174g·cm-3的KCl溶液是不饱和溶液 ④将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174g·cm-3
③20℃时,密度小于1.174g·cm-3的KCl溶液是不饱和溶液 ④将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174g·cm-3
A.①②③ B.①②③④ C.③④ D.①④
13.V mL密度为ρg·mL-1的某溶液中,含有相对分子质量为M的溶质m g,该溶液中溶质的质量分数为ω%,物质的量浓度为c mol·L-1,那么下列关系正确的是( )
A.c=1000ρω/M B.c=1000m/VM C.ω%=(cM/1000ρ)% D.m=Vρω/1000
12.在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
A.甲的分子数比乙的分子数多
B.甲的摩尔体积比乙的摩尔体积小
C.甲的物质的量比乙的物质的量少
D.将甲、乙气体混合(温度、压强不变,且甲、乙不反应),则混合气体中甲所占体积分数比乙大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com