
题目列表(包括答案和解析)
6.将4gNaOH固体溶于水配成50mL溶液,其物质的量浓度为( )
A.0.1mol/L B.0.5mol/L C.1mol/L D.2mol/L
5.下列物质中所含分子数目最多的是 ( )
A.0.5mol CO2 B.6.02×1022个水分子
C.标准状况下, 11.2L H2 D.28g CO
4.标准状况下,下列物质所占的体积最大( )
A.28gN2 B.71gCl2 C.48gO2 D.1000gH2O
3.下列关于阿伏加德罗常数的说法,正确的是( )
A.阿伏加德罗常数是12g碳中所含的碳原子数
B.阿伏加德罗常数是0.012kg12C中所含的碳原子数
C.阿伏加德罗常数是6.02×1023mol-1
D.阿伏加德罗常数的符号是N
2.下列表示方法中,错误的是( ) A.2mol氮 B. 1molH2O C. 4mole- D. 0.5molH2SO4
1.下列解释正确的是( ) A.物质的量就是物质的质量 B.物质的量就是物质的数量 C.物质的量可以认为是物质量 D. 物质的量是一个物理量,表示含有一定数目粒子的集体
21.(10分)
(1)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
请写出FeCl3溶液与铜反应的化学方程式: 。
检验反应后的溶液中存在Fe3+的试剂是: 。
(2)某一反应体系有反应物和生成物共五种物质:O2 、H2CrO4 、Cr(OH)3 、H2O 、H2O2 。已知该反应中H2O2只发生如下过程:H2O2→O2
① 该反应中的还原剂是 。
② 该反应中,发生还原反应的过程是 → 。
③ 如反应转移了0.3mol电子,则产生的气体在标准状况下体积为 。
20.(17分)甲、乙、丙三位同学分别用如下实验装置及化学药品(碱石灰为氢氧化钠和生石灰的混合物)制取氨气。请你参与探究,并回答问题:
(1)制取氨气的化学方程式为: ;
(2)三位同学都用向下排空气法收集氨气,其原因是 ;
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨(实验操作都正确),你认为没有收集到氨气的同学是 填(“甲”、“乙”或“丙”);
(4)检验氨气是否收集满的方法是(简述操作方法、现象和结论):
。
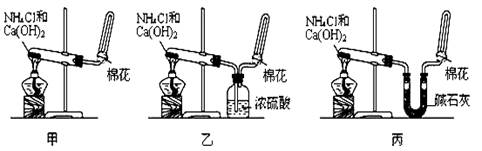
(5)三位同学都认为,采用上述各自的装置,还可用于加热碳酸氢铵固体的方法来制取纯净的氨气,你认为那位同学能够达到实验目的 (填“甲”、“乙”或“丙”)。他们还认为,装置中的NH4HCO3固体可用NH4Cl固体代替,你认为 (填“能”或“不能”)。
(6)某课外活动小组查阅有关资料知,铂丝是氨氧化的催化剂。并设计进行了如图实验。实验过程中观察到:瓶口气体变为红棕色,瓶内出现白烟。
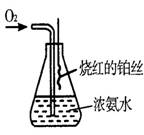 写出此实验过程中化学反应方程式:
写出此实验过程中化学反应方程式:
_______________ ;
____ ;
___________ ___;
__________________ 。
19.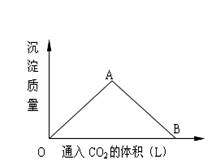 (10分)右图为一定量的饱和Ca(OH)2澄清溶液中通入二氧化碳气体后,产生碳酸钙白色沉淀的质量与通入二氧化碳气体体积的关系曲线,请回答下列问题:
(10分)右图为一定量的饱和Ca(OH)2澄清溶液中通入二氧化碳气体后,产生碳酸钙白色沉淀的质量与通入二氧化碳气体体积的关系曲线,请回答下列问题:
(1)写出O-A段曲线与A-B段曲线所表
现的离子方程式:
OA: ,
AB: ;
(2)A点处,参加反应的二氧化碳与氢氧化钙的物质的量之比为: ;
(3)B点处,溶液中存在离子的浓度最大的两种离子是:
。
18.(10分)下图表示某些物质之间的转化关系,每个字母代表一种物质,部分产物已略去。A是一种酸式盐,也是一种常用的化学肥料,B是能使湿润的红色石蕊试纸变蓝色的无色气体,D是无色无味的气体。回答下列问题。

(1)物质A的名称是:
(2)写出物质B的一种主要用途:
(3)写出工业上制取气体B的化学方程式:
(4)实验室收集E、F的方法:E_______ __ D____ _____
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com