
题目列表(包括答案和解析)
2.同温同压下,等质量的下列气体所占有的体积最大的是 ( )
A.O2 B.CH4 C.CO2 D.SO2
1.环境污染问题越来越受到人们的关注,造成环境污染的主要原因大多是由于人类生产活动中过度排放有关物质引起的。下列环境问题与所对应的物质不相关的是 ( )
A.温室效应--CO2 B.光化学污染--NO2
C.酸雨--SO2 D.臭氧层破坏--CO
23.(19分)在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。 请回答该实验中的问题。
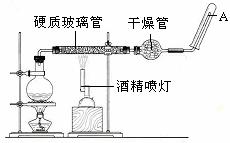
(1)写出该反应的化学方程式 ,其中氧化剂是 ,还原剂是 。8.4g铁粉参加反应,转移电子 mol。
(2)玻璃管中石棉绒的作用是 ,实验开始时应先点燃 ,实验结束时应先熄灭 。
(3)圆底烧瓶中盛装的水,该装置受热后的主要作用是 ;烧瓶里应事先放置 ,其作用是 。
(4)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的
成分是 ,若溶液未变红色则说明硬质试管中固体物质的
成分是 。
(5)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是
 (用离子方程式表示)。
(用离子方程式表示)。
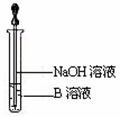
(6)该同学马上另取少量溶液B,使其跟NaOH溶液反应。
若按右图所示的操作,可观察到生成白色沉淀,迅速变成
灰绿色,最后变成红褐色的现象,请写出与上述现象相关
的反应的化学方程式 ,
。
(7)一段时间后,该同学发现(4)中未变红的溶液变成红色,说明Fe2+ 具有 性。由此可知,实验室中含Fe2+的盐溶液现用现配制的原因是 ,
并且配制含Fe2+的盐溶液时应加入少量 。
梅州市曾宪梓中学2010-2011学年度第一学期期末考试试卷
22.(10分)在实验室里,某同学取一小块金属钠做与水反应的实验。试完成下列问题:
(1)切开的金属钠暴露在空气中,最先观察到的现象是 ,所发生反应的化学方程式是 。
(2)将钠投入水中后,钠融化成一个小球,根据这一现象你能得出的结论是
① ,② 。
将一小块钠投入盛有饱和石灰水的烧杯中,不可能观察到的现象是
A.有气体生成 B.钠融化成小球并在液面上游动
C.溶液底部有银白色的金属钙生成 D.溶液变浑浊
(3)钠与水反应的离子方程式为 。
在反应过程中,若生成标准状况下224mL的H2,则转移的电子的物质的量为 。
(4)根据上述实验过程中钠所发生的有关变化,试说明将金属钠保存在煤油中的目的是
。
21.(11分)某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图
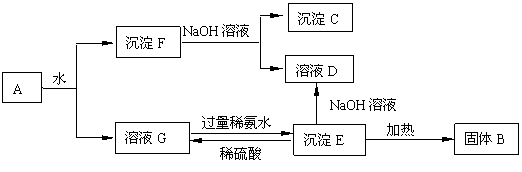 所示的变化。
所示的变化。
请回答下列问题。
(1)图中涉及分离溶液与沉淀的方法是 。
(2)B、C、D、E 4种物质的化学式为:
B 、C 、D 、E 。
(3)沉淀F与NaOH溶液反应的离子方程式为 。
沉淀E与稀硫酸反应的离子方程式为 。
溶液G与过量稀氨水反应的化学方程式为 。
20.设NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A.常温常压下,11.2 LCO2所含的原子数为1.5NA
B.常温常压下,48 g O3含有的氧原子数为3NA
C.标准状况下,22.4 L H2O所含分子数为NA
D.标准状况下,22.4 L H2中所含原子数为2NA
第二卷 非选择题(共40分)
19.下列各组中的离子,能在溶液中大量共存的是( )
A.Mg2+、H+、C1-、OH- B.K+、Cu2+、NO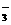 、SO
、SO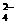
C.Na+、OH-、Cl-、CO D.Na+、Ba2+、CO
D.Na+、Ba2+、CO 、NO
、NO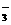
18.下列各选项中的杂质,欲用括号内物质除去,其中能达到目的的是 ( )
A.CO2中有少量CO(灼热的氧化铜) B.CaO中有杂质CaCO3 (稀HCl)
C.NaCl溶液中有杂质Na2SO4(硝酸钡) D.FeSO4溶液中有杂质CuSO4(铁粉)
17.下列反应能用离子方程式:CO32- + 2H+ === CO2 ↑ + H2O表示的是 ( )
A.Na2CO3 + 2HCl== 2NaCl+ CO2 ↑ + H2O
B.CaCO3 + 2HCl ==CaCl2 + H2O + CO2 ↑
C.K2CO3 + H2SO4 == K2SO4 + CO2 ↑ + H2O
D.BaCO3 + 2HNO3 ==Ba(NO3 )2+ CO2 ↑ + H2O
16.下列说法正确的是( )
A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L
B.从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液中氢离子的浓度为2 mol/L
C.配制480 mL 0.5 mol/L的CuSO4溶液,需称取62.5 g胆矾
D.中和100 mL 1mol/L的H2SO4溶液,需NaOH为4 g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com