
题目列表(包括答案和解析)
6.下列说法中正确的是

A.氧化剂发生氧化反应 B.还原剂发生还原反应
C.失电子的元素化合价降低 D.得电子的元素化合价降低
5. 只用哪一种试剂就可将AgNO3、KSCN、稀H2SO4 、NaOH 四种无色溶液区分开
A.FeCl3溶液 B.FeCl2溶液 C.BaCl2溶液 D.Fe(NO3)3溶液
4. 下列物质不能与二氧化碳反应的是( )
A. NaHCO3溶液 B. Na2CO3溶液 C. CaCO3溶液 D.NaOH溶液
3. 在有水参加的下列氧化还原反应中,水既不是氧化剂又不是还原剂的是
A. C+H2O(气) CO+H2 B. Cl2+H2O=HCl+HClO
CO+H2 B. Cl2+H2O=HCl+HClO
C. 2F2+2H2O=4HF+O2 D.2Cl2+2H2O=4HCl+O2
2. 下列化学反应中,属于氧化还原反应的是
A.Na2CO3+2HCl=2NaCl+CO2↑+H2O B.CaO+H2O=Ca(OH)2
C. 2CO +O2  2CO2
D. CaCO3
2CO2
D. CaCO3 CaO+CO2↑
CaO+CO2↑
1. 下列物质组别,不属于同素异形体的是
A.O2和O3 B.白磷和红磷 C.金刚石和C60 D.H2O和H2O2
26.(12分)将6.4 g 铜加入到50 mL a mol/L的硝酸溶液中,铜全部溶解,得到NO2和NO的混合气体。将反应后溶液稀释至100 mL,测得NO3-的浓度为3 mol/L。
(1)混合气体中NO2和NO的总物质的量为 mol(用含a的式子表示)。
(2)稀释后的溶液中H+的物质的量浓度为 mol/L。
(3)若a=9,则混合气体中NO2的物质的量为 mol。
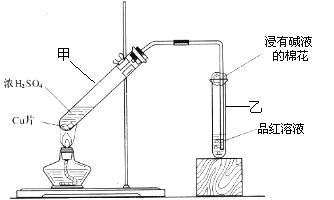
25.(16分)某教师在课堂上用右图所示
的装置来验证浓硫酸与铜是否发生反
应,并探讨反应所产生气体的性质。请
回答下列问题:
(1)通过试管乙中发生的
现象说明了铜和浓硫酸发生了化学反应,
并且该现象还能说明产生的气体具有 性。
(2)写出试管甲中所发生反应的化学方程式,并标明电子转移方向和数目。
。
(3)试管乙口部浸有碱液的棉花的作用是 ,此防范措施也说明产生的气体是 (填“酸性”、“中性”或“碱性”)气体, (填“有”或“无”)毒性。
(4)SO2的排放是造成酸雨的主要因素,某同学通过实验探究,得出酸雨pH随时间的增加而减小的结论。为进一步研究酸雨的成分,该同学取某一时段的这种雨水V L,加入0.5 mol/L的Ba(OH)2溶液至不再产生沉淀时,恰好消耗40.00 mL Ba(OH)2溶液。请计算:
①该雨水中共溶解SO2的体积是 mL(标准状况)。
②若生成沉淀物的质量为4.50 g,则沉淀物的组成为 (填写化学式)。
24.(16分)氯化铵是一种重要的化工原料,应用广泛。
(1)实验室通常用NH4Cl固体与Ca(OH)2固体混合共热制取氨气。
①写出实验室制取氨气的反应方程式 。
②浓氨水可以用来检验有毒气体氯气的泄漏,反应式为3Cl2 +8NH3= N2 + 6NH4Cl,在该反应中,氧化剂是 (填化学式),检测时观察到的现象是 ,21.3 g氯气能氧化氨气 mol。
(2)用浓氯化铵溶液处理的舞台幕布难着火,其原因是 (填字母)。
 ①幕布的着火点升高
①幕布的着火点升高
②幕布的质量增加
③氯化铵分解吸收热量,降低了温度
④氯化铵分解产生的气体隔离了部分空气
A.①② B.③④ C.①③ D.②④
(3)实验室可用NH4Cl溶液与饱和的NaNO2溶液反
 应制取纯净的氮气,反应方程式为:
应制取纯净的氮气,反应方程式为:
NaNO2+NH4Cl NaCl+N2↑+2H2O
实验装置如右图所示,试回答:
①装置中A部分的分液漏斗与蒸馏烧瓶之间连接
的导管所起的作用是 (填写编号)。
a.防止饱和溶液蒸发
b.保证实验装置不漏气
c.使饱和NaNO2溶液容易滴下
②加热前必须进行的一个操作步骤是 。
 ③收集N2最适宜的方法是
(填写编号)
③收集N2最适宜的方法是
(填写编号)
a.排空气法收集在集气瓶中
b.排水法收集在集气瓶中
c.直接收集在球胆或塑料袋中
23.(15分)化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等都离不开化学。
(1)硅是无机非金属材料的主角。请你举出两种含硅的材料名称 ;铝制品表面有一层氧化铝薄膜而经久耐用,但该氧化膜易被酸、碱破坏。若将氧化铝与氢氧化钠溶液作用,反应的离子方程式为 。
(2)氯气用于漂白时,实际上起漂白作用的物质不是Cl2而是它和水反应生成的
(写化学式)。缺铁性贫血患者补充的Fe2+,通常以硫酸亚铁的形式,而硫酸铁则没有这种药效。当用硫酸亚铁制成药片时外表要包有一层特殊的糖衣,这层糖衣的作用是 。
(3)从降低成本和减少环境污染的角度考虑,制取硝酸铜最好的方法是 (填代号)。
A.铜和浓硝酸反应 B.铜和稀硝酸反应
C.氧化铜和硝酸反应 D.铜先与浓硫酸共热,再加入硝酸钡
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com