
题目列表(包括答案和解析)
9. 某课外兴趣小组为了探究铁与硫在
某课外兴趣小组为了探究铁与硫在
隔绝空气的条件下反应所得固体M
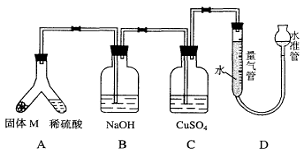
的成分,设计了如右图装置。倾斜A
使稀硫酸(足量)与固体M充分反应,
待反应停止后,B装置增重,C装置
中溶液无变化,反应后进入量气管气
体的体积为VmL(已折算成标准状
况)由上述实验事实可知:
(1)①固体M中一定有的物质是______________(填化学式) 理由是__________________
_____________②其中一种物质的质量可以确定为___________g(用代数式表示)。
(2)B装置的名称是_______。写出B装置中反应的离子方程式________________________。
(3)C装置的作用是_________________________,如果实验中没有B装置,则C装置中产生的现象是_____________________________________________________________。
(4)稀硫酸和固体M反应后溶液中还残留淡黄色固体,该固体是_____________,要分离出该固体,在实验操作中,除烧杯外还需要用到的玻璃仪器是_____________。
(5)通过进一步实验,测得固体M中各种成分的质量之和小于反应前铁粉和硫粉的质量之和,产生这种现象的原因可能是_____________
a.M中有未反应的铁和硫 b.测定气体体积时水准管的水面高于量气管的水面
c.A中留有反应生成的气体 d.气体进入D装置前未用浓硫酸干燥
答案:(1)①FeS、Fe B装置增重、量气管有气体。② V/400
(2)洗气瓶 2OH-+H2S → 2H2O+S2--
(3)证明H2S已被完全吸收 黑色沉淀
(4)硫 漏斗、玻璃棒 (5) b、C
8.用钠、镁、铝分别与盐酸反应,填写下面几种情况的空白。
(1)称取相同质量的钠、镁、铝,然后再分别与足量的盐酸反应,产生的氢气在通常条件下的体积比为______________。
(2)取相同物质的量的钠、镁、铝,后再分别与足量的盐酸反应,产生的氢气的质量比为________________________。
(3)如果要制取相同体积的氢气(同温、同压下),与足量盐酸分别反应时所消耗的钠、镁、铝的质量比为_____________;物质的量之比为__________。
7.如果1 mol金属投入含1 mol酸的溶液中产生1 mol H2,下列哪种情况是可能的____。
①一价金属和二元酸 ②二价金属和二元酸
③三价金属和二元酸 ④三价金属和一元酸
⑤二价金属和三元酸 ⑥一价金属和一元酸
8.由锌、铁、镁、铝四种金属中的两种组成的混合物10g,与足量的盐酸反应生成的氢气在 标准状况下为11.2L,则混合物中一定含有的金属是( )
A.锌 B.铁 C.铝 D.镁
7. 已知工业上真空炼铷的反应方程式为:2RbCl+Mg MgCl2+2Rb(g) ,对于此反应,能够进行正确解释的是( )
已知工业上真空炼铷的反应方程式为:2RbCl+Mg MgCl2+2Rb(g) ,对于此反应,能够进行正确解释的是( )
A.Rb比Mg金属性强
B.铷的沸点比镁的低,当把铷蒸气抽走时,平衡向正反应方向移动
C.MgCl2对热的稳定性比RbCl弱
D.高温下,Mg2+离子得电子的能力比Rb+离子弱
6.相等物质的量的钠、镁、铝分别与相等质量且过量的稀硫酸反应,反应完全后三种溶液的质量(用m金属表示)大小关系为 ( )
A.mNa>mMg>mAl B.mNa=mMg=mAl
C.mNa=mMg<mAl D.mNa<mMg<mAl
5.将8.4g铁粉和1.2g硫粉均匀混合加热至红热时,停止加热后使反应进行完全,冷却后,向所得固体加入足量的盐酸,在标准状况下得到的气体体积是 ( )
A.1.12L B.2.24L C.3.36L D.4.48L
4.14.0g的铜、银金属混合粉末,跟足量的某浓度的硝酸反应,将放出的气体与1.12L标准状况下的氧气混合,通过水中恰好完全被吸收。则原金属混合粉末中铜的质量分数( )
A.68.86% B.45.71%
C.22.86% D.11.43%
3.a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种。已知:①a、C都能跟稀硫酸反应放出气体;②b跟d的硝酸盐溶液反应,会有单质d析出;③C跟强碱溶液反应放出气体;④c、e在冷浓硝酸中发生钝化。由此可判断a、b、c、d、e依次为 ( )
A.Fe、Cu、Al、Ag、Mg B.Al、Cu、Mg、Ag、Fe
C.Mg、Cu、Al、Ag、Fe D.Mg、Ag、Al、Cu、Fe
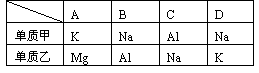
2.下表中的各组元素的单质,将0.02 mol甲放入1L 0.01 mol· L-1的盐酸中,完全反应后过滤,再往溶液中(假设无损耗)加入0.01 mol乙,整个过程中放出氢气的量最多的是 ( )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com