
题目列表(包括答案和解析)
3.T℃时,将某硫酸铜溶液蒸发掉55克水,或向该溶液中加入25克胆矾,都能得到该温度下的硫酸铜饱和溶液,则该温度下硫酸铜的溶解度为(单位:克)( )
A.45 B.25 C.29 D.39
2.室温下,有一硫酸铜饱和溶液,若向其中加入少许无水硫酸铜粉末,则有硫酸铜晶体析出。下列叙述正确的是( )
A.溶液中硫酸铜的质量分数增大 B.溶液中硫酸铜的质量分数不变
C.溶液中硫酸铜的质量分数减小 D.硫酸铜的溶解度减小
1.土壤胶粒带负电荷,在水稻田中,施用含氮量相同的下列化肥时,肥效较差的是
A.(NH4)2SO4 B.NH4HCO3 C.NH4NO3 D.NH4Cl
25.在100℃时,将0.200molN2O4气体充入2L抽空的密闭容器中,每隔一定的时间对该容器内的物质进行分析,得到如下表格:
|
时间(s) 浓度 (mol/L) |
0 |
20 |
40 |
60 |
80 |
100 |
|
C(N2O4) |
0.100 |
c1 |
0.050 |
c3 |
a |
b |
|
C(NO2) |
0.000 |
0.060 |
c2 |
0.120 |
0.120 |
0.120 |
试完成:
(1)该反应的化学方程式为______________________________表中c2__________ c3、
a_________b(填“ > ”、“<”、“ = ”)
(2)20s时N2O4的浓度c1=________mol/L,
在0s-20s时间段内,N2O4的平均反应速率为________ molL-1s-1。
(3)若在相同情况下最初向该容器的NO2气体,要达到上述同样的平衡状态,NO2的起始浓度是________mol/L。
24.某化学反应2A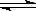 B+D在四种不同条件下进行,B、D起始浓度为零,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为零,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:

根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为 mol/(L·min)。
(2)在实验2,A的初始浓度C2= mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为V3,实验1的反应速率为V1,则V3 V1(填>、=、<=,且C3 1.0mol/L(填>、=、<=
(4)比较实验4和实验1,可推测该反应是 反应(选填吸热、放热)。理由是 。
23、在碘化钾和硫酸的混合液中加入过氧化氢水溶液,迅速发生反应放出大量气体,反应过程可表示如下:
①H2O2 + 2KI + H2SO4 == I2 + K2SO4 + 2H2O ;
②H2O2 + I2 = 2HIO ;
③H2O2 + 2HIO = I2 + O2 + 2 H2O ;
(1)H2O2在反应③中的作用是:
A、氧化剂 B、还原剂
C、既是氧化剂又是还原剂 D、既不是氧化剂又不是还原剂
(2)有人认为上述反应说明了碘单质是过氧化氢分解的催化剂,你认为____________(填“对”或“不对”),其理由是_________________________________________。
22.称取四份0.50g锌(相对原子质量65),按下列要求分别盛于四支试管里,塞上带导管的塞子,每隔一定时间分别测定生成的氢气的体积。
①0.50gZn + 5mL 3mol/L H2SO4
②0.50gZn + 5mL 3mol/L H2SO4 + 0.1gCu片
③0.50gZn + 5mL 3mol/L H2SO4+ 0.1gCu粉
④0.50gZn + 5mL 3mol/L H2SO4+ 0.39g胆矾(相当于0.1gCu)
(1)生成氢气的速率由快到慢的顺序为_____________________________;
(2)生成氢气的总量关系为_______________________________________。
21.某反应在催化剂的作用下按以下两步进行:第一步:X+Y=Z;第二步:Y+Z=M+N+X,此反应的总方程式是 ;
反应的催化剂为 。
20.在密闭容器里,通入x mol H2(g)和y mol I2(g),发生反应
H2(g)+I2(g)  2HI(g) △H<0。改变下列条件,正反应速率将如何改变?(填“增大”“减小”或“不变”)
2HI(g) △H<0。改变下列条件,正反应速率将如何改变?(填“增大”“减小”或“不变”)
(1)升高温度 ; (2)加入催化剂 ;
(3)充入更多的H2 ; (4)扩大容器的体积 ;
(5)容器容积不变,通入氖气 。
19.pH相同,体积也相同的稀硫酸与醋酸溶液,分别同时与过量的锌粒反应,则下列叙述正确的是( )
A.开始时产生氢气的速率 v (H2SO4)>v (CH3COOH)
B.开始时产生氢气的速率 v (H2SO4)<v (CH3COOH)
C.经过t min时,产生氢气的速率 v (H2SO4)<v (CH3COOH)
D.最终产生氢气的量 n (H2SO4)<n (CH3COOH)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com