
题目列表(包括答案和解析)
2.把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡,b、d相连时,b上有大量气泡产生,则四种金属活动顺序由强到弱正确的为( )
A、a>b>c>d B、a>c>d>b
C、c>a>b>d D、b>d>c>a
1.已知蓄电池在充电时作电解池,放电时作原电池;铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“-” ;关于标有“+”的接线柱,下列说法中正确的是( )
A.充电时作阴极,放电时作正极 B.充电时作阳极,放电时作负极
C.充电时作阴极,放电时作负极 D.充电时作阳极,放电时作正极
2.由电极变化情况确定:某一电极若不断溶解或质量不断减少,该电极发生氧化反应,则此电极为负极;若某一电极上有气体产生、电极的质量不断增加或不变,该电极发生还原反应,则此电极为正极,燃料电池除外。
金属腐蚀的快慢:
电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护措施的腐蚀
原电池正、负极的确定
1.由两极的相对活泼性确定:相对活泼性较强的金属为负极,一般地,负极材料与电解质溶液要能发生反应。
(1)析氢腐蚀(酸性较强环境中) 电池反应为 Fe + 2H+ == Fe2+ + H2↑
负极:Fe → Fe2+ + 2e- 正极:2H+ + 2e- → H2↑
(2)吸氧腐蚀(中性或酸性很弱环境中) 电池反应为 2Fe+ O2 + 2H2O == Fe(OH)2
负极: Fe → Fe2+ + 2e- 正极:2H2O + O2 + 4e- → 4OH-
3.氢氧燃料电池(以KOH为电解质溶液)
负极2H2 + 4OH- → 4H2O + 4e- 正极 O2 + 2H2O + 4e- → 4OH-
电池反应 2H2 + O2 == 2H2O
2. 铅蓄电池
铅蓄电池
 电池反应PbO2 + Pb + 2H2SO4
2PbSO4 + 2H2O
电池反应PbO2 + Pb + 2H2SO4
2PbSO4 + 2H2O
1.锌锰干电池
负极Zn +2OH- → Zn(OH)2 +2e-
正极2MnO2(S)+ H2O(l)+ 2e -→ Mn2O3 + 2OH-
电池反应为: Zn +2MnO2 +H2O == Zn(OH)2 + Mn2O3
5.C70分子是形如椭球状的多面体,该结构的建立基于以下考虑: (1)C70分子中每个碳原子只跟相邻的3个碳原子形成化学键; (2)C70分子中只含有五边形和六边形; (3)多面体的顶点数、面数和棱边数的关系遵循欧拉定理:顶点数+面数-棱边数=2。 根据以上所述确定:
①C70分子中所含的单键数和双键数;
②C70分子中的五边形和六边形各有多少?
4.晶体硼的基本结构单元都是由硼原子组成的正二十面体,其中含有
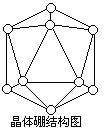 20个等边三角形的面和一定数目的顶角,每个顶角各有一个硼原子,
20个等边三角形的面和一定数目的顶角,每个顶角各有一个硼原子,
如图所示。回答: (1)键角 ____________;
(2)晶体硼中的硼原子数______________个;
(3)B-B键有_____________条。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com