
题目列表(包括答案和解析)
6.(09河南)草莓、香蕉等水果具有芳香气味,是因为其中含有乙酸乙酯(化学式为C4H8O2)等物质。下列关于乙酸乙酯的说法正确的是 [ ]
A.该物质属于氧化物 B.其分子由碳原子、氢原子和氧分子构成
C.该物质的相对分子质量为88 D.该物质中碳、氢、氧的质量比为12︰1︰16
5.(09安徽)我国著名化学家徐光宪因在稀土元素等研究领域做出杰出贡献,荣获2008年度“国家最高科学技术奖”。铈(Ce)是一种常见的稀土元素,下列关于铈的说法错误的是[ ]
A.原子序数是58 B.相对原子质量是140.1
C.质子数为58 D.铈元素是非金属元素
4.(09南昌)某阳离子的结构示意图为 则x的数值可能是[ ]
A.9 B.10 C.12 D.17
3.(09南昌)防止金属锈蚀是保护金属资源的有效途径,锌铬黄 (化学式位ZnCrO4)常用于制防锈涂料。锌铬黄中铬元素的化合价为[ ]
A.+1 B.+2 C.+6 D.+7
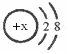
2.(09六盘水)下列粒子都能直接构成物质的是[ ]
A.分子、中子 B.原子、电子 C.原子、离子 D.离子、中子
1.(09新疆)抗雪灾中,为使道路的积雪迅速融化,使用一种融雪剂硅酸钠,化学式为Na2SiO3,其中硅元素的化合价为[ ]
A. +2 B. +3 C. +4 D. +6
35.(1)火焰中的燃素在加热过程能透过容器与汞结合形成红色物质,导致质量增加了(答“燃素与汞结合造成质量增加”即可)
(2)①不支持,因为从实骏知汞增加的质量并非来自于燃素而是来自于空气②氧气(或O2)③质量守恒
1.(2010.浙江台州)35. 18世纪中期,为了解释燃烧现象,有人提出了“燃素说”,其主要观点有:
①燃素是一种构成火的元素,火焰是自由的燃素,燃素能透过一切物体。
②一般条件下燃素被禁锢在可燃物中,是物体的一个成分。
③燃烧是可燃物中物体同燃素分解的过程。
(1)将汞装入密封容器中,置于火炉上加热,容器内形成丁质量增加的红色物质。请以上述燃素说的主要观点来解释质量增加的原因 。
(2)法国化学家拉瓦锡也做了加热汞的实验(装置如图),他在实验前后称量了容器及其中物质的总质量。结果发现:反应前后总质量不变,且汞变成红色物质(后知是氧化汞)增加的质量等于容器中空气减少的质量。之后,拉瓦锡还将反应形成的氧化汞加强热,使之重新释放出气体,并将该气体与原来容器中剩余的气体混合,发现混合气体的性质与最初的空气相同。根据上述资料,回答:
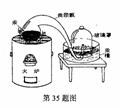
①拉瓦锡实验是否支持燃素说,并说明理由 。
②拉瓦锡实验中氧化汞受强热释放出的气体是 。
③拉瓦锡在实验中,均对反应前后的容器及其中物质的质量进行了称量,体现了他
对 规律的重要认识。
2.(2010.浙江杭州)39.氢气可被用作清洁能源,但它的制取、存储和运输都很困难。科学家开发出一种用糖类制取氢气的新技术,有望解决这几大问题。
以这项技术为基础,未来的氢动力汽车将携带易于存储的糖类,如淀粉,其化学式是(C6H10O5)。科学家使用由多种特殊的酶组成的混合物,将淀粉和水转变成CO2和H2的混合气体,将CO2除去后,H2进入燃料电池产生电力,驱动汽车前进。燃料箱容量为55升的汽车可携带约27千克淀粉和21千克的水,完全转变,可以产生4千克氢气,其余为CO2。根据以上材料,请回答下列问题:
(l)利用该项技术,汽车运动时时的机械能最终由下列哪种能量转化而来 ▲
A.化学能 B.太阳能 C.电能 D.热能
(2)混合物中的酶具有高效性、多样性和 ▲ 性。
(3)请根据质量守恒定律配平淀粉和水反应的化学方程式
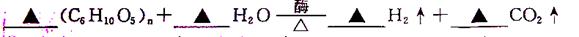
(4)若一辆氢动力汽车正常行驶时,功率是70千瓦,氢气的热值是1.4×108焦/千克,燃料电池的能量转化效率是50%,在阻力不变和不考虑其它能量损耗时,要使该车能正常行驶,汽车每小时至少消耗氢气 ▲ 千克
(5)这种技术的实用化,还存在较多的问题,如在汽车中怎样除去混合气体中的CO2就是问题之一。有人提出了下列:
①将混合气体通过澄清石灰,
②将混合气体通过溶质质量:
③在常温下对混合气体加压,使之液化分离(在20℃时,将CO2加压到5.73×106 Pa,即会液化;氢气在-239. 96℃以上温度时,加高压也不会液化)。从实用的角度考虑, 理论上你认为哪种方案更适合在氢动力汽车上应用 ▲ (填序号)。
答案:39.(1) B
(2) 专一
(3)
1 (C6H10O5)n + 7n H2O 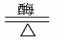 12n H2↑+ 6n CO2 ↑
12n H2↑+ 6n CO2 ↑
(4) 3.6;
(5)③
.
1.(10镇江)25.(2分)工业上采用电解饱和食盐水制备氢氧化钠:2NaCl+2H2O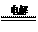 2NaOH+Cl2↑+H2↑。因饱和食盐水中混有一定量的NH4Cl,在电解时会引起爆炸。为除去NH4Cl,工业上常利用电解后的碱性废液、Cl2与NH4Cl反应(其中Cl2与NH4Cl化学计量数分别为3、2),使NH4Cl转化成N2。该反应的化学方程式为: ▲ ,请说出此方法的优点之一 ▲ 。
2NaOH+Cl2↑+H2↑。因饱和食盐水中混有一定量的NH4Cl,在电解时会引起爆炸。为除去NH4Cl,工业上常利用电解后的碱性废液、Cl2与NH4Cl反应(其中Cl2与NH4Cl化学计量数分别为3、2),使NH4Cl转化成N2。该反应的化学方程式为: ▲ ,请说出此方法的优点之一 ▲ 。
2NH4Cl+8NaOH+3Cl2=N2+8NaCl+8H2O (1分,不配平或配错不扣分)
利用废液作原料,变废为宝;或利用本厂生产的产品作原料,降低生产成本;
或将NH4Cl杂质转化为N2,对环境无污染。(1分,意思相近均给分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com