
题目列表(包括答案和解析)
5.500多年前,一艘载着天然苏打晶体的商船在航行中搁浅,船员们便在附近的沙滩上用几块苏打晶体支锅煮饭。事后,他们惊奇地发现,锅下苏打与沙粒接触处出现了许多晶莹剔透的珠子。请你分析,这些珠子可能是( )
A.无水碳酸钠 B.水晶 C.玻璃珠 D.金刚砂(SiC)
思路解析:海边的沙滩上有砂子,还有各种各样美丽的鹅卵石,前者的主要成分是SiO2,后者的主要成分是CaCO3,而天然苏打的成分是Na2CO3·10H2O,当它们一起灼烧时,正如与生产玻璃的原理相同。
答案:C
4.常见的氧化物分为酸性氧化物、碱性氧化物、两性氧化物和不成盐氧化物四类。二氧化硅属于酸性氧化物,理由是( )
A.Si是非金属元素 B.SiO2与水反应生成硅酸
C.SiO2与强碱反应只生成盐和水 D.SiO2不能与酸反应
思路解析:判断一种氧化物是不是酸性氧化物的主要依据是:①与水反应的产物是否只有酸;②与碱反应的产物是否是盐和水。二氧化硅既不溶于水,也不与水反应,所以B错误。C是正确的。
答案:C
3.碳酸的酸性比硅酸强,某化学课外小组搜集了大量的证据证明硅酸的酸性弱于碳酸酸性。其中能证明硅酸的酸性弱于碳酸酸性的实验事实是( )
A.CO2溶于水形成碳酸,SiO2难溶于水
B.CO2通入可溶性硅酸盐中析出硅酸沉淀
C.高温下SiO2与碳酸钙、碳酸钠等固体反应生成CO2
D.氯化氢通入可溶性碳酸盐溶液中放出气体,通入可溶性硅酸盐溶液中生成沉淀
思路解析:根据强酸制弱酸的规律,CO2通入可溶性硅酸盐中析出硅酸沉淀的事实可证明碳酸的酸性比硅酸强。
答案:B
2.水玻璃在工业生产上具有重要的用途,在建筑等行业应用非常广泛。下列不是水玻璃用途的是( )
A.肥皂填料 B.木材防火剂 C.纸板黏胶剂 D.制玻璃
思路解析:水玻璃用途广泛,可用作肥皂填料、木材防火剂、纸板黏胶剂、建筑材料黏合剂等。玻璃是一种硅酸盐,但其原料无需Na2SiO3。
答案:D
1.(2010广东高考,3)下列表述正确的是( )
①人造刚玉熔点很高,可用作高级耐火材料,主要成分是二氧化硅 ②化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐 ③提前建成的三峡大坝使用了大量水泥,水泥是硅酸盐材料 ④夏天到了,游客佩戴由添加氧化亚铜的二氧化硅玻璃制作的变色眼镜来保护眼睛 ⑤太阳能电池可采用硅材料制作,其应用有利于环保、节能
A.①②③ B.②④ C.③④⑤ D.③⑤
思路解析:本题考查我们身边的元素化合物知识。人造刚玉就是人造宝石,它的主要成分是Al2O3;玛瑙是带有特殊杂质的二氧化硅,它的主要成分不是硅酸盐;氧化亚铜不具有感光性,不能用作变色眼镜的制作,而常见的变色眼镜是利用AgBr的感光性制成的。
答案:D
7.用地壳中某主要元素生产的多种产品在现代高科技中占重要位置,足见化学对现代物质文明的重要作用。例如:
(1)计算机的芯片的主要成分是_______________。
(2)光导纤维的主要成分是_______________。
(3)目前应用最多的太阳能电池的光电转化材料是_______________。
(4)用作吸附剂、干燥剂、催化剂或催化剂的载体的人造分子筛大多是一类称为________的化合物。
(5)有一大类化合物,结构独特,兼备无机材料和有机材料的双重性能,具有耐温、电绝缘性好、难燃、憎水、耐腐蚀等特性,广泛用于航空航天、电子电气、建筑、运输等行业,主要用于密封、黏合、润滑、涂层、表面活性、防水、防潮等,已成为现代社会不可替代的新材料。这类材料在结构上的特点是_______________和_______________。
思路解析:现代社会中的重要材料同学们一定要有所了解。
答案:(1)硅(或Si或单晶硅)
(2)二氧化硅(或SiO2)
(3)硅(或Si)
(4)铝硅酸盐或硅铝酸盐(注:此题明确是分子筛,不应答硅胶,答硅酸盐也不对)
(5)具有Si-O键和与硅相连的烃基
快乐时光
敬业的小偷
一日,某君乘公交车时钱包被掏,气愤之余,在乘车前将一沓纸装进信封放进口袋,鼓鼓的,然后上车。中途摸摸,信封还在,到站下车一摸,没了,偷着乐。
翌日,此君再乘车,到站下车后,忽觉腰间有物,惊,掏出一看,信封装着纸。信封上几个歪歪斜斜的字:先生,请不要开这种玩笑,影响我的工作!
30分钟训练(巩固类训练,可用于课后)
6.元素M为一半导体材料,广泛应用于半导体材料工业中,用于制造光敏电阻、光电管及光电池,而且在自动控制、电视传真方面有广泛的应用。由于M具有可经受超电荷、耐高温、电稳定性好、轻盈的优点,常用于制造整流器。
(1)写出M的元素符号_______________。
(2)元素M为于周期表第_______________周期_______________族。
(3)与M处于同一主族的元素X,是生命中最重要的元素之一,它在地壳中的含量极高,请写出X的元素符号_______________。
(4)元素M和元素X可以形成化合物Y,写出其化学式____________________________。
思路解析:半导体材料在金属与非金属分界线附近,ⅣA族中分布较多。从其用途我们可以倒推出它就是电子工业中的重要材料--硅。
答案:(1)Si (2)3 ⅣA族 (3)C (4)SiC
5.载人飞船上两副硅太阳能电池帆板提供了飞船所需的电力。请画出硅原子的原子结构示意图_____________________________________________________________________________。
思路解析:硅的原子结构示意图是学习化学的基本功,可按照核外电子排布规律来排布。
答案:Si 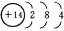
4.在实验室里氢氧化钠溶液为什么不能装在带玻璃塞的试剂瓶里,氢氟酸为什么不能装在玻璃瓶中而只能装在塑料瓶里?
思路解析:玻璃的主要成分是二氧化硅,它能够与氢氧化钠和氢氟酸发生反应。
答案:防止氢氧化钠与玻璃瓶塞反应而将瓶口粘住;防止氢氟酸将玻璃腐蚀。
3.硅单质为什么在常温下性质稳定?
思路解析:物质的性质是由物质的结构决定的,稳定的性质来自于稳定的结构。硅的正四面体的空间网状结构使它的原子间的作用力很强,在常温下,很难发生化学键的断裂,所以其化学性质也很稳定。
答案:硅的正四面体的空间网状结构使它的原子间的作用力很强,在常温下,很难发生化学键的断裂,所以其化学性质也很稳定。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com