
题目列表(包括答案和解析)
3.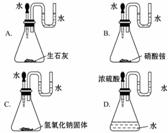 如图,加入水或酸后,各装置U形管中的液柱左边高于右边的是( )
如图,加入水或酸后,各装置U形管中的液柱左边高于右边的是( )
[解析]选B。生石灰、氢氧化钠固体、浓H2SO4溶于水时会放出大量的热,使锥形瓶内气体压强增大,导致U形管中的液柱左边低,右边高;硝酸铵固体溶于水时吸收热量,导致锥形瓶内气体压强减小,使U形管中液柱左边高,右边低,故选B。
2.下列反应既属于氧化还原反应,又属于吸热反应的是( )
A.铝片与稀盐酸反应
B.Ba(OH)2·8H2O与NH4+Cl的反应
C.灼热的碳与CO2的反应
D.甲烷在氧气中的燃烧反应
[解析]选C。金属与酸的反应是放热反应;燃烧是放热反应;Ba(OH)2·8H2 O和NH4+Cl的反应是吸热反应但不是氧化还原反应;碳和CO2的反应既是氧化还原反应又是吸热反应。
O和NH4+Cl的反应是吸热反应但不是氧化还原反应;碳和CO2的反应既是氧化还原反应又是吸热反应。
1.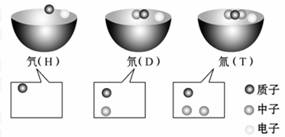 科学家们发现有3种氢原子,氕、氘、氚这3种氢原子中质子、中子
科学家们发现有3种氢原子,氕、氘、氚这3种氢原子中质子、中子 和电子的数量关系如图所示:
和电子的数量关系如图所示:
则下列说法不正确的是( )
A.H、D、T原子中质子数相同,核外电子数也相同
B.H、D、T原子属于三种不同核素
C.H、D、T原子互为同位素
D.元素的原子都是由质子、中子、电子构成的
[解析]选D。H、D、T是氢元素的三种不同核素,互称为同位素,同位素原子中质子数相同,核外电子数相同,不同的是中子数,且氕原子无中子,故只有D不正确。
10.以硅石为原料,选择合适的试剂来制备硅胶。
思路解析:硅石的主要成分是二氧化硅,而硅胶的主要成分还是二氧化硅,但这里的二氧化硅是多孔的固体,它一般通过硅酸脱水得到,所以主要的目的实际上是制硅酸。
答案:SiO2+2NaOH====Na2SiO3+H2O
Na2SiO3+2HCl====2NaCl+H2SiO3
H2SiO3 SiO2+H2O
SiO2+H2O
9.海战中为了掩蔽,常喷放SiCl4和液氨,而形成很浓的烟雾,若烟雾的成分是H2SiO3小颗粒和NH4Cl晶粒及水雾等,试写出生成它们的化学方程式。
思路解析:从题干中的信息可知,反应物应该有SiCl4和液氨,生成物则是H2SiO3和NH4Cl及H2O,将方程中的反应物和生成物写出来,然后配平即得。
答案:3H2O +SiCl4+4NH3====H2SiO3+4NH4Cl。
8.现代建筑的门窗框架常用电解加工成的古铜色硬铝制造。取硬铝样品进行如下实验(每步试剂均过量),由此可以推知硬铝的组成为( )
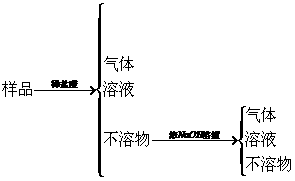
A.Al、Cu、Mg、Si、Mn B.Al、Mg、Si、Zn
C.Al、Fe、C、Cu D.Al、Si、Zn、Na
思路解析:B、D中的成分形成合金后不可能为古铜色。C中金属和碳加过量盐酸,C和Cu均不反应,过滤后,再加浓NaOH溶液也不反应。
答案:A
7.下列离子方程式,正确的是( )
A.澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2====CaCO3↓+H2O
B.碳酸钠溶液中加入二氧化硅: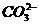 +SiO2====
+SiO2====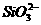 +CO2↑
+CO2↑
C.二氧化硅与烧碱溶液反应:SiO2+2OH-====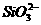 +H2↑
+H2↑
D.硅酸与烧碱溶液中和:H2SiO3+2OH-====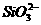 +2H2O
+2H2O
思路解析:过量二氧化碳通入澄清石灰水中生成可溶性的碳酸氢钙,碳酸钠溶液中加入二氧化硅不反应,二氧化硅与烧碱溶液反应生成硅酸钠和水,故A、B、C均错误。
答案:D
6.某无色溶液中加入过量盐酸有白色沉淀产生,过滤后向滤液中加入过量氨水又有白色沉淀产生。下列溶液符合此条件的是( )
A.Ag+、Fe3+、K+
B.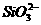 、
、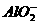 、K+
、K+
C.Ag+、Cu2+、Na+ D.Ag+、Ba2+、Na+
思路解析:加入过量盐酸时,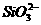 与H+结合生成硅酸白色沉淀,
与H+结合生成硅酸白色沉淀,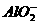 与过量盐酸反应生成Al3+,过滤后再加入过量氨水,Al3+与氨水反应生成氢氧化铝白色沉淀。
与过量盐酸反应生成Al3+,过滤后再加入过量氨水,Al3+与氨水反应生成氢氧化铝白色沉淀。
答案:B
5.500多年前,一艘载着天然苏打晶体的商船在航行中搁浅,船员们便在附近的沙滩上用几块苏打晶体支锅煮饭。事后,他们惊奇地发现,锅下苏打与沙粒接触处出现了许多晶莹剔透的珠子。请你分析,这些珠子可能是( )
A.无水碳酸钠 B.水晶 C.玻璃珠 D.金刚砂(SiC)
思路解析:海边的沙滩上有砂子,还有各种各样美丽的鹅卵石,前者的主要成分是SiO2,后者的主要成分是CaCO3,而天然苏打的成分是Na2CO3·10H2O,当它们一起灼烧时,正如与生产玻璃的原理相同。
答案:C
4.常见的氧化物分为酸性氧化物、碱性氧化物、两性氧化物和不成盐氧化物四类。二氧化硅属于酸性氧化物,理由是( )
A.Si是非金属元素 B.SiO2与水反应生成硅酸
C.SiO2与强碱反应只生成盐和水 D.SiO2不能与酸反应
思路解析:判断一种氧化物是不是酸性氧化物的主要依据是:①与水反应的产物是否只有酸;②与碱反应的产物是否是盐和水。二氧化硅既不溶于水,也不与水反应,所以B错误。C是正确的。
答案:C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com