
题目列表(包括答案和解析)
5.某烷烃的一种同分异构体只能生成一种一氯代物,则该烃的分子式不可能是( )
A.C2H6 B.C4H10 C.C5H12 D.C8H18

2.(2010·温州高一检测)下列物质中属于高分子化合物的是( )
①油脂 ②蔗糖 ③淀粉 ④丙氨酸 ⑤蛋白质
⑥聚氯乙烯 ⑦乙酸乙酯 ⑧纤维素
A.①③⑤⑥ B.③⑤⑥⑧
C.②④⑦ D.除②④⑦外
[解析]选B。多糖(如淀粉、纤维素)、蛋白质、聚氯
乙烯(高聚物)属于高分子化合物,而油脂、蔗糖、丙氨
酸(结构简式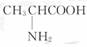 )、乙酸乙酯均不是高分子
化合物。
)、乙酸乙酯均不是高分子
化合物。


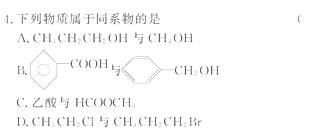
[解析]选A。同系物的前提是“结构相似”,理解为官能团相同,故A正确,B、D错误;C项两者属于同分异构体。
1.(2010·宣城同步检测)下列关于有机物的用途,说法不正确的是( )
A.甲烷是一种热量高、污染小的清洁能源
B.乙烯最重要的用途是作为植物生长调节剂
C.乙醇是一种很好的溶剂,能溶解多种有机物和无机物
D.酯类物质常用作饮料、糖果、香水、化妆品中的香料
[解析]选B。甲烷完全燃烧生成CO2和H2O,同时放出大量的热,A正确;乙烯的用途之一为植物生长调节剂,但不是最重要的用途,其重要用途应为作化工原料,B不正确;乙醇能溶解多种有机物和无机物,是一种很好的溶剂,C正确;酯类可作饮料、糖果、香水、化妆品中的香料,D正确。
0.001 mol×64 g/mol=0.064 g,故SO2的含量为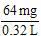 =200
mg/L>0.02 mg/L,所以SO2含量严重超标。
=200
mg/L>0.02 mg/L,所以SO2含量严重超标。
297.6 mL+22.4 mL=320 mL,其中SO2的质量为
15.0 g海带。
(2)因海带中碘元素并非以I2形式存在,而是KI,故可以对海带灼烧。
(3)过滤时,不能用玻璃棒搅拌,否则易将滤纸弄破。
(4)据加入A试剂现象,可选H2O2或新制氯水,若使用HNO3,则将KI氧化成高价态碘,而非I2,因此溶液不变蓝,因KMnO4(H+)本身有颜色影响实验观察,所以使用
KMnO4(H+)的实验未做。
答案:(1)准确 因为游码在零刻度
(2)不正确 海带中碘元素以KI形式存在
(3)不正确 过滤时不能用玻璃棒在漏斗中搅拌
(4)①H2O2或新制氯水 ②HNO3具有强氧化性,将KI氧化成高价态碘而非I2 ③KMnO4(H+)本身有颜色,影响实验观察
15.(14分)碘是人体生长发育不可缺少的微量元素,它在人体中仅有20-50毫克,人体用碘制造甲状腺素,调节新陈代谢,若摄入碘量不足,则人会得甲状腺肿大的粗脖子病即地甲病。那么,碘是从哪里来的呢?下面是一个研究性学习小组做了一个证明海带确实含有碘的实验,以下 是实验过程及学生讨论情况记录表:
是实验过程及学生讨论情况记录表:
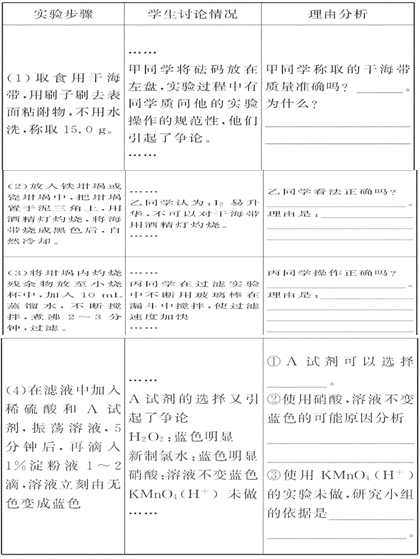
[解析](1)虽然操作时误将砝码放在左盘,因称15.0 g海带,没使用游码(或游码在零刻度)故能准确称取
13.(9分)钛(Ti)是一种活泼的金属,其作为金属材料,具有密度小、熔点高、可塑性强 、机械强度高、亲生物性好等优良的性能,有“未来金属”之称。工业上常用硫酸分解钛铁矿石(FeTiO3)的方法来制取二氧化钛(TiO2),再由二氧化钛制金属钛,主要有以下五个反应:
、机械强度高、亲生物性好等优良的性能,有“未来金属”之称。工业上常用硫酸分解钛铁矿石(FeTiO3)的方法来制取二氧化钛(TiO2),再由二氧化钛制金属钛,主要有以下五个反应:
①FeTiO3+2H2SO4====TiOSO4+FeSO4+2H2O;
②TiOSO4+2H2O====H2TiO3↓+H2SO4;
③H2TiO3 TiO2+H2O;
TiO2+H2O;
④TiO2+2C+2Cl2 TiCl4↑+2CO↑;
TiCl4↑+2CO↑;
⑤TiCl4+2Mg====2MgCl2+Ti。
△
△
(1)针对以上五个化学反应,下列叙述错误的是____ 。
A.反应①是非氧化还原反应
B.反应②生成了两种酸
C.反应④中的TiO2是氧化剂
D.反应⑤表现了金属镁比金属钛还原性强
(2)钛具有很强的耐腐蚀性,以下对其原因的分析中正确的是_____ (填写代号)。
①钛是像金、铂一样不活泼的金属
②金属钛的表面易形成致密的氧化膜
③钛与氧气、酸等腐蚀剂不发生化学反应
[解析](1)在反应①中没有元素发生化合价的变化,其中钛元素的化合价保持+4价;在反应②中,化学式H2TiO3符合酸的一般化学式,它是钛酸的化学式;在反应④中钛元素的化合价保持+4价,Cl2是 氧化剂,C是还原剂;在反应⑤中,Mg是还原剂,Ti是还原产物,所以还原性Mg>Ti。
氧化剂,C是还原剂;在反应⑤中,Mg是还原剂,Ti是还原产物,所以还原性Mg>Ti。
(2)“钛(Ti)是一种活泼的金属”“耐腐蚀性强”,活泼的金属应容易与氧气、酸等腐蚀剂发生化学反应,但因为钛表面易形成致密的氧化膜而耐腐蚀。
答案:(1)C (2)②
1 4.(13分)某研究性学习小组在实验室中模拟石油的催化裂化,装置如图:实验过程中可观察到烧瓶Ⅰ中固体石蜡先熔化,试管Ⅱ中有少量液体凝结,试管Ⅲ中酸性高锰酸钾溶液褪色,实
4.(13分)某研究性学习小组在实验室中模拟石油的催化裂化,装置如图:实验过程中可观察到烧瓶Ⅰ中固体石蜡先熔化,试管Ⅱ中有少量液体凝结,试管Ⅲ中酸性高锰酸钾溶液褪色,实 验后闻试管Ⅱ中液体气味,具有汽油的气味。
验后闻试管Ⅱ中液体气味,具有汽油的气味。
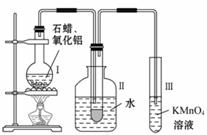
(1)该装置仪器连接的顺序应遵循的原则为_____ ,
加入药品之前的操作为_____ ,长导管的作用是____ ;
(2)试管Ⅱ中少量 液体凝结说明了_____ ;
液体凝结说明了_____ ;
(3)试管Ⅲ中溶液褪色说明了_____ ;
(4)能否用试管Ⅱ中的液体萃取溴水中的溴,理由是
_____。
(5)写出二十烷裂化得到癸烷和癸烯的化学方程式____。
(6)石油裂化的重要意义是_____ 。
[解析]仪器连接的顺序应遵循从下往上、从左到右的原则,装入药品之前要检验装置的气密性。依据石油分馏工业的分馏塔原理,设置了长导管,其作用除导气外,兼起冷凝气体的作用;依据催化裂化原理,下列反应皆有可能发生:

以上的烃大都呈液体。试管 Ⅲ 中 KMnO4 溶液褪色说明生成常温常压下 呈气态的5个碳原子数以下的烯烃;由于裂化产物中有烯烃生成,易与溴发生加成反应,所以不能用来萃取卤素单质;从以上变化可以看出,石油裂化的主要目的是为了获得更多的轻质燃油,特别是
呈气态的5个碳原子数以下的烯烃;由于裂化产物中有烯烃生成,易与溴发生加成反应,所以不能用来萃取卤素单质;从以上变化可以看出,石油裂化的主要目的是为了获得更多的轻质燃油,特别是 汽油的产量和质量。
汽油的产量和质量。
答案:(1)从下往上,从左往右检验装置的气密性
导气、冷凝气体
(2)裂化生成了5个碳原子数以上的烃
(3)裂化生成了碳原子数小于5的烯烃
(4)不能,因为裂化产物中有烯烃,易与溴发生加成反应
(5)C20H42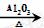 C10H22+C10H20
C10H22+C10H20
(6)可提高石油产品中轻质燃油特别是汽油的产量和质量
12.用足量的CO还原32.0 g某种氧化物,将生成的气体通入足量澄清石灰水中,得到60 g沉淀,则该氧化物是( )
A.FeO B.Fe2O3 C.CaO D.Cu2O
[解析]选B。此题可用原子守恒法来解。CO被氧化为
CO2,增加的氧原子全部来源于金属氧化物。
n(O)=n(CaCO3)= 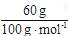 =0.6
mol;金属氧化物中金属
=0.6
mol;金属氧化物中金属
的质量为:32 g-0.6 mol×16 g·mol-1=22.4 g,则 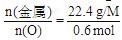 ,然后把各选项中的原子个数比及各金属的摩尔质量代入验证,只有B项中M=56 g·mol-1时合理。
,然后把各选项中的原子个数比及各金属的摩尔质量代入验证,只有B项中M=56 g·mol-1时合理。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com