
题目列表(包括答案和解析)
6.(14分)(2009·南阳高一检测)断开1 mol H-H键,
1 mol N-H键、1 mol N≡N键分别需要吸收的能量为436 kJ、391 kJ、946 kJ,求:
(1)1 mol N2生成NH3需_____ (填“吸收”或“放出”)能量_____ kJ。
(2)1 mol H2生成NH3需_____ (填“吸收”或“放出”)能量_____ kJ。
 [解析]本题可从断键吸收的能量数值与成键放出的能量数值的相对大小来判断,若E(断键)>E(生成),则为吸热反应;E(断键)<E(生成)则为放热反应。
[解析]本题可从断键吸收的能量数值与成键放出的能量数值的相对大小来判断,若E(断键)>E(生成),则为吸热反应;E(断键)<E(生成)则为放热反应。
(1)N2+3H2 2NH3,生成2 mol NH3形成6 mol N-H键
时要放出6 mol×391 kJ/mol=2 346 kJ的能量,拆开
1 mol N≡N键和3 mol H-H键时吸收的总能量为946 kJ+
3 mol×436 kJ/mol=2 254 kJ,整个过程中的能量变化为放出能量,为2 346 kJ-2 254 kJ=92 kJ。

[实验·探究]
5.(思维拓展题)已知25 ℃、101 kPa下,1 mol石墨完全燃烧生成CO2放出393.51 kJ热量、1 mol金刚石完全燃烧生成CO2放出395.41 kJ热量。据此判断,下列说法正确的是( )
A.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低
B.由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高
C.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低
D.由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高
[解析]选A。25 ℃、101 kPa下,1 mol石墨完全燃烧生成CO2放出的热量比1 mol金刚石完全燃烧生成CO2放出的热量少395.41 kJ-393.51 kJ=1.9 kJ。也就是说,石墨的能量比金刚石的低,由石墨制备金刚石必须从外界吸收能量,是吸热反应。
4.(2010·保定高一检测)下列图中能正确表示 X+3Y====2Z(放热反应)过程的能量变化的是( )
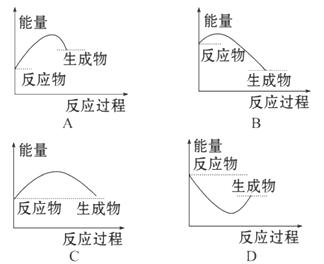
[解析]选B。反应放出能量,会导致生成物的总能量低于反应物的总能量,且反应需加热才能进行,故只有B项正确。
3.下列中和反应中放出热量最多的是( )
A.100 mL 0.3 mol/L的HCl和50 mL 0.3 mol/L的NaOH相混合
B.80 mL 0.3 mol/L的HCl和80 mL 0.3 mol/L的NaOH溶液相混合
C.80 mL 0.3 mol/L的H2SO4和80 mL 0.3 mol/L的NaOH溶液相混合
D.50 mL 0.3 mol/L的H2SO4和50 mL 0.6 mol/L的NaOH溶液相混合
|
 mol、0.024 mol、0.030 mol,即D项产生H2O的量最多,所以放出热量最多。
mol、0.024 mol、0.030 mol,即D项产生H2O的量最多,所以放出热量最多。 2.(2010·邯郸高一检测)研究物质变化时,人们可以从不同的角度、不同的层面来认识物质变化时所引起的化学键及能量变化。据此判断以下叙述中错误的是( )
A.金属钠与氯气反应生成氯化钠后,其结构的稳定性增强,体 系的能量降低
系的能量降低
B.物质燃烧可看成“储存”在物质内部的能量(化学能)转化为热能释放出来
C.氮分子内部存在着很强的共价键,故通常状况下氮气的化学性质很活泼
D.需加热才能发生的反应不一定是吸收能量的反应
[解析]选C。N2内部存在N≡N三键,分子很稳定,化学性质不活泼。
1.已知反应Na2S O4·10H2O Na2SO4·nH2O+(10-n)H2O。 有人将装有芒硝(Na2SO4·
O4·10H2O Na2SO4·nH2O+(10-n)H2O。 有人将装有芒硝(Na2SO4· 10H2O)的密闭聚乙烯管安装在房屋的外墙内就能达到白天蓄热使室内保持低温度,晚上把白天所蓄热量放出,使室内保持温暖。以下说法不正确的是( )
10H2O)的密闭聚乙烯管安装在房屋的外墙内就能达到白天蓄热使室内保持低温度,晚上把白天所蓄热量放出,使室内保持温暖。以下说法不正确的是( )
A.白天将太阳能转化为化学能
B.白天将化学能转化为太阳能
C.晚上将化学能转化为热能
D.晚上发生的是放热反应
[解析]选B。白天吸收太阳能使Na2SO4·10H2O分解,即太阳能转化为化学能,晚上,Na2SO4·nH2O与(10-n)H2O作用形成Na2SO4·10H2O放出热量,即化学能转化为热能。
23.(共13分)按要求填写下列实验报告:
|
|
实验内容 |
主要实验操作 |
主要结论 |
|
① |
除去FeSO4溶液中的少量Fe2(SO4)3, |
_____________,过滤 |
离子方程式为: |
|
② |
证明SO2既有漂白性又有还原性 |
www.k@s@5@
高#考#资#源#网 |
主要现象为: |
|
③ |
证明还原性: I- > Cl- |
取样,_______________ ___________________。 |
离子方程式为: |
|
④ |
证明CO2具有一定的氧化性(助燃性): |
|
化学方程式为: |

24(共8分)如右图所示是测定镁粉(含有少量杂质Al)纯度的实验装置,所用NaOH溶液的浓度为4.5mol/L,体积为100mL,不同时间段电子天平的读数如下表所示:
|
实验操作 |
时间(min) |
电子天平的读数(g) |
|
烧杯+NaOH溶液 |
|
120.0 |
|
烧杯+NaOH溶液+样品 |
0 |
135.6 |
|
1 |
135.1 |
|
|
2 |
134.7 |
|
|
3 |
134.4 |
|
|
4 |
134.4 |
(1)请列式计算样品中镁的质量分数?
(2)求反应后溶液中的c(OH-)?(假定反应前后溶液体积不变)
www.k@s@5@ 高#考#资#源#网
(3)若定义:平均反应速率==某物质发生变化的物质的量 / 反应经历的时间,则用H2物质的量的变化所表示的上述反应从开始到结束时的平均速率为多少?
22.(共7分)已知A、B、D、H 是中学范围内的常见的单质,J为蓝色溶液。相互转化关系如图所示(部分产物及反应条件已略去),试回答有关问题:
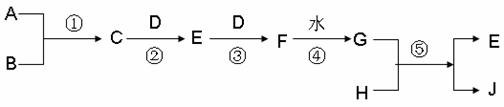
(1)若A为气体,B为固体时,已知反应:C + D → E + H2O,E是一种大气污
染物,且将C与E混合可生成淡黄色的B,写出C和E反应的化学方程式:
,
其中氧化产物与还原产物的物质的量之比为
(2)若A、B均为气体,当将C和G的浓溶液相互接触时会产生白烟,检验白烟
中含有的阳离子的方法是:
写出反应②的化学方程式
21.(共10分)如图所示:①-⑩分别代表有关反应中的一种物质,它们均为常
见物质。已知①-⑤和⑥-⑩中分别含有同一种元素。试回答下列问题:
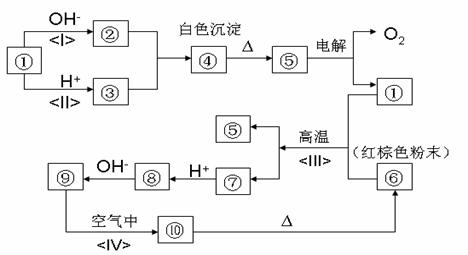
www.k@s@5@ 高#考#资#源#网
(1)写出指定物质的化学式:④ ;⑥
(2)写出反应(Ⅲ)的化学方程式
指出该反应的重要用途之一:
(3)写出反应(Ⅰ)的离子方程式
(4)反应(Ⅳ)的主要实验现象是
该反应的化学方程式为:
20.(共10分)已知重铬酸钾K2Cr2O7和浓盐酸在常温下反应可生成氯气,试回答下列问题:
(1)请完成并配平如下的化学方程式(将未知物的化学式和化学计量数填入)
()K2Cr2O7+()HCl==()KCl+()CrCl3 +()Cl2↑+( )□
(2)浓盐酸在上述反应中显示(填写序号)
A.只有还原性 B.只有氧化性 C.只有酸性
D.既有氧化性又有还原性 E.既有酸性又有还原性
(3)若反应中转移0.6mol 电子,则被氧化的还原剂的物质的量
为 mol,产生的Cl2的体积(STP)为 L。
(4)已知ClO2(气体)具有很强的氧化性,故常用作消毒剂,其消毒的效率(以
单位质量的消毒剂得到电子的物质的量大小来表示) 约是Cl2的 倍(保
留2位小数)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com