
题目列表(包括答案和解析)
4.(2009·襄樊高一检测)运用元素周期律分析下面的推断,其中推断错误的是( )
A.氢氧化铍[Be(OH)2]的碱性比氢氧化镁弱
B.砹(At)为有色固体,HAt不稳定
C.硫酸锶(SrSO4)是难溶于水的白色固体
D.硒化氢(H2Se)是无色、有毒,比H2S稳定的气体
[解析]选D。A项,Be和Mg同主族,金属性不如镁的强,故Be(OH)2的碱性比Mg(OH)2弱;B项,卤族元素的单质从上到下,颜色加深,氢化物越来越不稳定;C项,Sr和Ba同主族,故SrSO4也难溶于水;D项,Se的非金属性不如S强,故H2Se不如H2S稳定。
3.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A.原子半径:r(A)>r(B)>r(D)>r(C)
B.原子序数:d>c>b>a
C.离子半径:r(C3-)>r(D-)>r(B+)>r(A2+)
D.单质的还原性:A>B>D>C
[解析]选C。aA2+、bB+、cC3-、dD-都是短周期元素的离子,由于它们的电子层结构相同,因而C、D位于A、B的上一周期,为非金属元素,且原子序数:d>c;A、B为金属元素,且原子序数:a>b,因而四种元素的原子序数由大到小的顺序为:a>b>d>c。由于A、B在C、D的下一周期,又是原子半径较大的金属元素,因而A、B的原子半径肯定比C、D的原子半径大,根据同周期元素原子半径的递变规律知,r(B)>r(A)>r(C)>r(D)。电子层结构相同的离子,阴离子半径必然大于阳离子半径,且带负电荷越多,半径越大,阳离子带正电荷越多,半径越小,故离子半径由大到小的顺序为:r(C3-)>r(D-)>r(B+)>r(A2+)。单质中,还原性:B>A,C>D。故选C。
2.下列说法正确的是( )
A.金属元素不能得电子,不显负价,故金属元素不能形成阴离子
B.P、S、Cl元素最高正价依次升高
C.B、C、N、O、F原子半径依次增大
D.Li、Na、K、Rb的氧化物对应水化物的碱性依次减弱
[解析]选B。A选项中金属元素无负价,但可以形成阴离
子,如 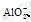 、
、 等,同周期元素从左向右,原子半径逐
等,同周期元素从左向右,原子半径逐
渐减小,元素的最高正价逐渐升高,从Li到Rb,金属性依次增强,所以对应的碱的碱性依次增强。
1.已知原子序数依次增大的A、B、C、D、E五种元素位于同一周期,下列关于该五种元素说法正确的是( )
A.若D的最高价氧化物的水化物是强酸,则E一定是活泼非金属
B.若A的最高价氧化物的水化物是强碱,则C一定是活泼金属
C.若B是金属元素,则C一定也是金属元素
D.若C是非金属元素,则D一定也是非金属元素
[解析]选D。同周期元素,随着原子序数的递增,非金属性增强,最高价氧化物的水化物酸性增强,金属性减弱,最高价氧化物的水化物碱性减弱。A项中D是活泼非金属,E可能是稀有气体元素,所以A项不正确;B项中只能说明A是活泼金属,列于A之后的C元素,可能是金属,也可能是非金属,所以B项不正确;同样C项也不正确。
7.(16分)现有部分短周期元素的性质或原子结构如下表:

(1)元素X的一种同位素可测定文物年代,这种同位素的符号是______(用元素符号表示),元素Z的离子结构示意图为______ 。
(2)元素Y与氢元素形成一种离子 则检测溶液中存
则检测溶液中存
在该离子的方法是______ 。
(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式: ______ 。
(4)元素X与元素Y相比,非金属性较强的是______ (用元素符号表示),下列表述中证明这一事实的是_____ 。
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应的水化物的酸性比X的最高价氧化物对应的水化物的酸性强
c.X与Y形成的化合物中X元素呈正价态
(5)探寻物质的性质差异性是学习的重要方法之一。X、Y、Z三种元素的单质中化学性质明显不同于其他两种单质的是______ (用元素符号表示),理由______。
[解析]根据X元素的核外电子排布特点可知是碳元素;Y的氢化物水溶液显碱性且单质是双原子分子,则Y必是氮元素;Z元素是第三周期简单离子中半径最小的,由于同周期元素的离子半径分成两种情况,阳离子半径依次减小,阴离子半径也是依次减小,但是阴离子半径明显比阳离子半径大很多,因此Z元素必定是第三周期的金属元素铝。其他内容可据题目要求逐一解决。
答案:(1) 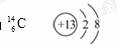
(2)向溶液(或待测液)中加入NaOH溶液后加热,能产生使湿润的红色石蕊试纸变蓝的气体,说明溶液中存在该离子,反之,不存在该离子
(3)Al(OH)3+OH- ==== +2H2O
(4)N b、c (5)Al 具有金属性
6.(14分)在第三周期元素中,置换氢能力最强的元素的符号为_____ ;化学性质最稳定的元素的符号是____ ;最高价氧化物的水化物酸性最强的酸的化学式是_____ ;碱性最强的碱的化学式是_____ ;显两性的氢氧化物的化学式是_____ ;该两性氢氧化物与盐酸、NaOH溶液分别反应的离子方程式是_____________、 ___________ ;
原子半径最大的金属元素的名称是_____ ,离子半径最小的离子的结构示意图为_____ 。
[解析]第三周期中的元素共有8种:Na、Mg、Al、Si、P、S、Cl、Ar。置换氢能力最强的是Na,化学性质最稳定的是Ar;Cl的非金属性最强,所以HClO4的酸性最强;碱性最强的是NaOH;Al(OH)3显两性;原子半径最大的是Na,离子半径最小的为Al3+。
答案:Na Ar HClO4 NaOH Al(OH)3
Al(OH)3+3H+ ====Al3+ +3H2O
Al(OH)3+OH-
==== 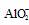 +2H2O 钠
+2H2O 钠 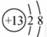
[实验·探究]
5.(思维拓展题)对四种金属G、L、M、R进行如下实验:
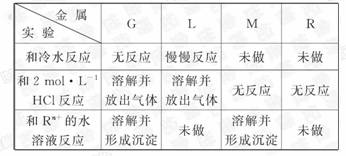
根据表中所给实验结果,判断这四种金属活动性由强到弱的次序正确的是( )
A.L、G、R、M B.G、L、M、R
C.L、G、M、R D.L、R、G、M
[解析]选C。L和冷水反应,而G不与冷水反应,活动性L>G,L、G与盐酸反应,而M、R与盐酸不反应,活动性L、G比M、R的强,M与Rn+ 的水溶液反应,知活动性:M>R,所以四种金属的活动性为:L>G>M>R。
4.(2008·广东高考)下列有关原子结构和元素周期律的表述正确的是( )
①原子序数为15的元素的最高化合价为+3
②ⅦA族元素是同周期中非金属性最强的元素
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为12的元素位于元素周期表的第三周期ⅡA族
A.①② B.①③ C.②④ D.③④
[解析]选C。因为原子序数为15的元素是磷元素,其最
高化合价为+5价,所以①错;按元素周期律,同一周期从左到右主族元素非金属性逐渐增强,②正确;碳元素
有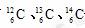 等几种同位素,其核电荷数都为6,但中 子数不惟一,故③错;原子序数为12的元素为镁元素,它 位于第三周期ⅡA族,④正确,故选C。
等几种同位素,其核电荷数都为6,但中 子数不惟一,故③错;原子序数为12的元素为镁元素,它 位于第三周期ⅡA族,④正确,故选C。
3.短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍。下列说法正确的是( )
A.X的氢化物溶于水显酸性
B.Y的金属性小于Na的金属性
C.Z的氢化物的水溶液在空气中存放不易变质
D.X和Z的最高价氧化物对应的水化物都是弱酸
[解析]选B。因X、Y、Z为短周期元素。X与Y、Z处于相邻周期,Z的最外层电子数是X内层电子数的3倍或者是Y原子最外层电子数的3倍,故X位于第二周期,Y、Z位于第三周期,且Y、Z的最外层电子数分别为2、6,又X、Y、Z原子最外层电子数之和为13,则X的最外层电子数为5,所以X、Y、Z分别为N、Mg、S。X的氢化物是氨气,其水溶液呈碱性,A项错误;Z的氢化物为H2S,其水溶液在空气中久置会变浑浊:2H2S+O2====2S↓+2H2O,C项错误;X和Z的最高价氧化物对应的水化物分别是硝酸和硫酸,都是强酸,D项错误。
2.有a、b、c、d四种元素,a、b为同周期元素,c、d为同主族元素。已知a的阳离子和d的阴离子具有相同的电子层结构。b的阴离子和c的阴离子电子层结构相同。且c离子的电荷数大于b离子。则下列说法正确的是( )
①原子序数d<b<c<a ②原子序数d<a<c<b
③原子序数d<a<b<c ④离子半径b>c>d>a
⑤离子半径b>c>a>d ⑥离子半径c>b>d>a
A.③④ B.②⑥ C.①⑤ D.②④
[解析]选B。本题考查元素原子结构与元素在周期表中位置的关系。根据题意可知,a、b、c、d四种元素在周期表中的相对位置为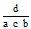 。又因为电子层结构相同的微
粒,原子序数越大,半径越小(稀有气体元素除外);同一主族元素由上至下原子半径逐渐增大,同一周期元素,原子序数越大,半径越小,所以原子序数d<a<c<b,离子半径c>b>d>a。
。又因为电子层结构相同的微
粒,原子序数越大,半径越小(稀有气体元素除外);同一主族元素由上至下原子半径逐渐增大,同一周期元素,原子序数越大,半径越小,所以原子序数d<a<c<b,离子半径c>b>d>a。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com