
题目列表(包括答案和解析)
4.(2010·福州高一检测)糖类、脂肪和蛋白质是维持人体生命活动必需的三大营养物质。下列说法错误的是( )
A.纤维素、淀粉、脂肪、蛋白质都是高分子化合物
B.淀粉水解的最终产物都能发生银镜反应
C.误食重金属盐而引起的中毒可服用大量豆浆或牛奶进行解救
D.脂肪能发生皂化反应,生成甘油和高级脂肪酸钠
[解析]选A。脂肪不是高分子化合物,A错误;淀粉水解的最终产物是葡萄糖,能发生银镜反应,B正确;服用豆浆或牛奶可对误食重金属盐的中毒者解救,C正确;脂肪在碱性条件下的水解反应称为皂化反应,水解产物为甘油和高级脂肪酸盐,D正确。
3.(2010·无锡高一检测)下列家庭化学小实验不能达到预期目的的是( )
A.用米汤检验食用加碘盐(含KIO3)中含有碘
B.用醋、石灰水验证蛋壳中含有碳酸盐
C.用银镜反应检验葡萄糖中是否含有醛基
D.用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验
[解析]选A。KIO3中的碘元素不是I2,不能与淀粉变蓝,A项不能达到预期目的;食醋中的醋酸能与蛋壳中的碳酸盐反应,放出CO2,CO2使澄清石灰水变浑浊;葡萄糖能发生银镜反应;蛋白质在浓盐溶液中能发生盐析而沉淀,再加入大量水,沉淀会溶解。B、C、D项均可达到实验目的。
2.(多选)(2010·中山高一检测)糖尿病人宜多吃蔬菜和豆类食品,豆类食品中富含蛋白质。下列说法正确的是( )
A.蛋白质可以通过灼烧时的特殊气味鉴别
B.人体内不含水解纤维素的酶,不能消化纤维素,因此蔬菜中的纤维素对人体没有用处
C.部分蛋白质溶液遇浓硝酸变黄,称为蛋白质的颜色反应
D.工业上常利用蛋白质的皂化反应来制取肥皂
[解析]选A、C。蛋白质在灼烧时具有烧焦羽毛的气味,A正确;虽然人体不能消化纤维素,但能加强肠胃的蠕动,B错误;部分蛋白质(分子中含有苯环)遇浓HNO3变黄,称为蛋白质的颜色反应,C正确;工业上利用油脂的皂化反应来制取肥皂,D错误。
1.硫酸在下列反应中,只起催化作用的是( )
①乙酸和乙醇的酯化反应 ②苯的硝化反应 ③油脂的水解反应 ④淀粉的水解反应
A.①④ B.②④ C.③④ D.②③
[解析]选C。在①②中浓H2SO4均作催化剂和吸水剂,③④中浓H2SO4作用是只作催化剂,故C正确。
0.1 mol·L-1NaBr溶液、0.1 mol·L-1NaI溶液、CCl4溶液等。
②仪器: ______ 、 _____ 、镊子、小刀、玻璃片等。
(3)实验内容(填写与实验方案对应的实验现象的标号和化学方程式):

(4)实验结论:____________________。
[解析]本题是一个设计实验题,题目较灵活,考查基础知识和运用知识能力;另外,今后在实验现象中应加强语言描述和记忆,这是许多学生的弱项。
答案:(1)探究同主族元素性质的相似性和递变性
(2)试管 胶头滴管
(3)

(4)同主族元素性质相似;自上而下元素原子失电子能力增强,得电子能力减弱
7.(16分)某同学做同主族元素性质相似性、递变性实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。

(1)实验目的:__________。
(2)实验用品:
①试剂:金属钠、金属钾、新制氯水、溴水、
6.(14分)下面是药物华素片(西地碘片)使用说明书中的部分内容。
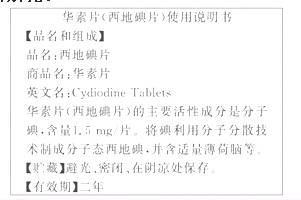
(1)根据上述说明和所学化学知识回答:
①华素片中含有的活性成分是_______(写分子式);
②请推断华素片_______ (“是”或“不是”)白色。
(2)某学生为验证华素片中确实含有上述活性成分,完成实验如下,请填写:
①取一粒药片放入研钵中研碎,再将药粉装入试管并加入约2 mL蒸馏水;向该试管中再加入约2 mL _______(填选项字母),并用力振荡;
A.酒精 B.NaOH溶液 C.四氯化碳 D.盐酸
②描述加入该溶液后可能观察到的现象_______ ;
③选用该溶液做实验的原因是_______ 。
(3)请再设计另一种方法,验证华素片中的活性成分(注意叙述实验原理、操作方法和实验结论) ______ 。
[解析]由题意知,华素片的活性成分是I2,因为I2为紫黑色固体,所以华素片也不会是白色。验证华素片的活性成分I2时,一般有两个途径:一是利用萃取原理,根据I2在有机溶剂中的颜色特点来检验;二是根据淀粉遇I2变蓝的特性,使用淀粉溶液进行检验。
答案:(1)①I2 ②不是
(2)①C ②溶液分上下层,上层无色下层紫色
③CCl4与水互不相溶,且碘单质在CCl4中的溶解度比在水中溶解度大
(3)取一粒华素片研碎,先溶于水配成溶液,再滴加淀粉溶液,如溶液变蓝,说明华素片中含碘单质
[实验·探究]
5.(2009·黄冈模拟)溴化碘(IBr)的化学性质类似卤素单质,它同水反应的化学方程式为IBr+H2O====HBr+HIO。下列有关IBr的叙述不正确的是( )
A.IBr跟水反应是非氧化还原反应
B.在很多反应中,IBr是强氧化剂
C.IBr的密度介于I2和Br2的密度之间
D.IBr跟NaOH稀溶液反应生成NaI、NaBrO和H2O
[解析]选D。分析反应IBr+H2O====HBr+HIO中元素价态变化可知,该反应为非氧化还原反应。IBr与Cl2等单质性质相似,是强氧化剂。由卤素单质的密度变化规律知IBr的密度应在I2和Br2之间。IBr与NaOH稀溶液反应生成NaBr、NaIO和H2O。
4.(多选)X、Y是元素周期表第ⅦA族中的两种元素。下列叙述中能说明X的非金属性比Y强的是( )
A.X原子的电子层数比Y原子的电子层数多
B.X的气态氢化物比Y的气态氢化物稳定
C.Y的单质能将X从NaX的溶液中置换出来
D.X在暗处可与H2反应,Y在加热条件下才能与H2反应
[解析]选B、D。X原子比Y原子的电子层多,X在Y的下方,则非金属性X比Y弱,A不正确;卤族元素氢化物越稳定,其非金属性越强,B正确;Y能置换NaX中的X,则非金属性X比Y弱,C不正确;单质与H2化合越容易,其非金属性越强,D正确。
3.下列各组给定原子序数的元素,形成的原子个数之比为1∶1 的稳定化合物中还原性最强的是( )
A.11和17 B.19和35 C.1和53 D.19和16
[解析]选C。四个选项中形成的化合物分别为NaCl、KBr、HI、K2S,其中K2S原子个数比不是1∶1,另三种还原性最强的是HI。故选C。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com