
题目列表(包括答案和解析)
6.(10分)某液态烃的分子式为CmHn,相对分子质量为H2的39倍。它不能使酸性KMnO4溶液褪色,不能同溴的四氯化碳溶液反应而使其褪色。在催化剂存在时,7.8 g该烃能与0.3 mol H2发生加成反应生成相应的饱和烃CmHp。则:
(1)m、n、p的值分别是m=____ ,n=____ ,p=____ 。
(2)CmHp的结构简式是:____ 。
(3)CmHn能和浓硫酸、浓硝酸的混合酸反应,该反应的化学方程式是____ ,该反应属于____反应,有机产物的名称是____ 。
[解析]解答本题可先由CmHn相对分子质量是H2的39倍,求出其相对分子质量,再由与H2加成推出不饱和键的情况。结合所学知识,可推断出CmHn的分子式,然后结合苯的性质和结构特点得出答案。
由题意知CmHn的相对分子质量为39×2=78,所以可推知
1 mol CmHn可与3 mol H2发生加成,习惯方法应推知其分子中有3个双键,但它不能与酸性KMnO4溶液和溴的四氯化碳溶液反应而使其褪色,根据所学知识,推测符合其情况的只有苯环的结构,从而推出CmHn的分子式为C6H6,C6H6能与3 mol H2加成生成C6H12,也能与浓硝酸发生取代反应。
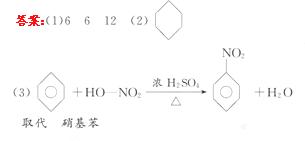
5.(2010·株洲高一检测)以苯为原料,不能通过一步反应而制得的有机物是( )
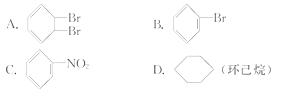
[解析]选A。苯分子不是单、双键交替结构,故不能与 Br2发生加 成反应生成
成反应生成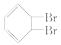 ;苯分子中六个化学键完
全相同
;苯分子中六个化学键完
全相同 ,这样结构的特殊性决定了苯易发生取代反应(如
与溴反应生成
,这样结构的特殊性决定了苯易发生取代反应(如
与溴反应生成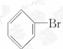 ,与混酸反应生成
,与混酸反应生成
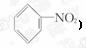 ),能发生加成反应(生成环己烷),难氧化
等性质,故选A。
),能发生加成反应(生成环己烷),难氧化
等性质,故选A。
4.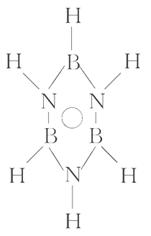 (2010·九江高一检测)B3N3H6
(2010·九江高一检测)B3N3H6
是一种平面形分子(如图所示),
因其分子结构的特殊性,被称为无
机苯,“无机苯”的二氯代物的同
分异构体的种类一共有( )
A.3种 B.4种
C.5种 D.6种
[解析]选B。B3N3H6的二氯代物有

3.(多选)科学家对物质性质的推断一般要基于一些实验事实。下列能说明苯与一般的烯烃性质不同的事实是( )
A.苯分子是高度对称的平面型分子
B.苯不与溴水反应
C.苯不与酸性KMnO4溶液反应
D.1 mol苯在一定条件下可与3 mol氯气发生加成反应
[解析]选B、C。碳碳双键也可以形成高度对称的平面型分子,所以A项不能证明;根据苯的结构简式,若有3个双键,也恰好与3 mol氯气发生加成反应,D项也不能证明;但是若有双键,则可以与溴水反应,也能使酸性KMnO4溶液褪色,但实际苯不具备这两种性质,所以B、C能证明。
2.下列实验能获得成功的是( )
A.苯与 浓溴水用铁作催化剂制溴苯
浓溴水用铁作催化剂制溴苯
B.将苯与浓硝酸混合共热制硝基苯
C.甲烷与氯气光照制得纯净的一氯甲烷
D.乙烯通入溴的四氯化碳溶液得到1,2- 二溴乙烷
[解析]选D。苯与液溴在加入Fe粉时才能反应生成溴苯,苯与浓溴水不反应,A错误;苯与浓HNO3和浓H2SO4的混合液在水浴加热时生成硝基苯,B错误;甲烷与Cl2光照时所得产物为混合物,C错误;乙烯与溴加成生成1,2- 二溴乙烷,D正确。
1.将等体积的苯、汽油和水在试管中充分混合后静置。下列图示现象正确的是( )
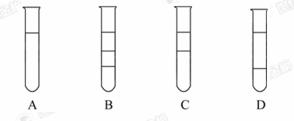
[解析]选D。题中苯、汽油和水的密度有差别,其中苯和汽油密度比水小,且能互溶,所以分两层,上下层比例为2∶1。
8.(12分)甲、乙两同学欲验证乙醇的性质,现做如下实验:
Ⅰ.甲同学做乙醇的催化氧化实验并考查催化剂的催化机理,现设计了如图装置(夹持装置仪器已省略),
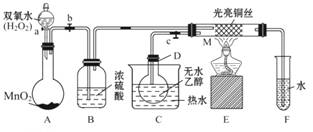
其实验操作为:先按图安装好,关闭活塞a、b、c,在铜丝的中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,而有节奏(间歇性)地通入气体,即可在M处观察到明显的实验现象。试回答以下问题:
(1)A中发生反应的化学方程式:_____ ,
B的作用:_____ ;C中热水的作用:_____ 。
(2)M处发生反应的化学方程式为:_____ 。
(3)从M管中可观察到的现象:_____。
从中可认识到该实验过程中催化剂_____(填“参加”或“不参加”)了化学反应,还可以认识到催化剂起催化作用需要一定的_____ 。
(4)实验一段时间后,如果撤掉酒精灯,反应_____ (填“能”或“不能”)继续进行,其原因是: _____。
Ⅱ.乙同学进行乙醇的沸点测定实验,设计装置如图,回答下列问题:
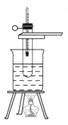
(1)盛乙醇的试管应浸入水浴中,水浴 的温度应保持在_____ 。
A.100 ℃ B.78.5 ℃ C.80 ℃ D.50 ℃
(2)测乙醇沸点时为什么不把整个试管浸在水里_____
为什么塞子上要有个豁口_____
[解析]Ⅰ.A装置的作用是产生O2,化学方程式为
2H2O2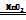 2H2O+O2↑,B中浓H2SO4干燥O2,C处热水浴作用
2H2O+O2↑,B中浓H2SO4干燥O2,C处热水浴作用
是使乙醇变为蒸气进入M处参加反应,在M中乙醇被催化氧
化,化学方程式为2CH3CH2OH+O2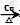 2CH3CHO+2H2O,生成的
2CH3CHO+2H2O,生成的
CH3CHO在F中收集,通过M中铜丝的颜色变化现象说明催化
剂参与化学反应,同时还需要一定的温度。因该反应为放
热反应,故撤去酒精灯,该反应仍能进行。
Ⅱ.在做测乙醇沸点的实验时应考虑必须使乙醇充分汽化,故水浴中应保持100 ℃,即沸水,测沸点时应在常压下,若试管封闭,则试管内压强增大。若将整个试管浸入水中,则试管内温度会升高,不能表示沸点。
答案:Ⅰ.(1)2H2O2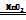 2H2O+O2↑
2H2O+O2↑
干燥O2 使D中乙醇变为蒸气进入M中参加反应
(2)2CH3CH2OH+O2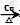 2CH3CHO+2H2O
2CH3CHO+2H2O
(3)受热部分的铜丝由于间歇性地鼓入氧气而交替出现变黑、变红的现象 参加 温度
(4)能 乙醇的催化氧化反应是放热反应,反应放出的热量维持反应继续进行
Ⅱ.(1)A (2)因为若将整个试管浸在沸水里,所测的温度为沸水的温度,而不是乙醇蒸气的温度 盛乙醇试管的塞子上留有豁口是使试管内外大气相通,压强相等
7.(10分)已知0.2 mol有机物和0.4 mol O2在密闭容器中燃烧后产物为CO2、CO和H2O(g)。产物经过浓H2SO4后,质量增加10.8 g;再通过灼热的CuO,充分反应后,CuO质量减轻3.2 g,最后气体再通过碱石灰被完全吸收,质量增加17.6 g。(已知两个羟基连在同一个碳原子上不稳定会自动失去一个水)
(1)试通过计算推断该有机物的分子式;
(2)若0.2 mol该有机物恰好将与9.2 g金属钠完全反应,试确定该有机物的结构简式;
(3)若改为0.2 mol该有机物恰好将与4.6 g金属钠完全反应,试确定该有机物的结构简式。



[实验·探究]
6.(8分)等物质的量的下列物质①甲醇(CH3OH)②乙醇(CH3CH2OH)③乙二醇(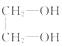 )④丙三醇
)④丙三醇
( 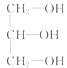 ),用物质的编号填空:
),用物质的编号填空:
(1)在空气中完全燃烧时,消耗氧气的质量由多到少的顺序_____ ,反应中生成CO2的体积(相同状况)由小到大的顺序_____ 。
(2)分别与足量的金属钠反应,放出H2的体积(相同状况)由少到多的顺序是_____ 。
[解析] (1)耗氧计算可先将四种物质改写成CxHy·nH2O的形式。
甲醇CH2·H2O 乙醇C2H4·H2O
乙二醇C2H2·2H2O 丙三醇C3H2·3H2O
可判断1 mol四种物质完全燃烧消耗氧气分别为1.5 mol、3 mol、2.5 mol、3.5 mol故顺序为④②③①。生成CO2的体积只与碳原子数有关,与H、O原子个数无关,故顺序为①<②=③<④。
(2)与足量金属钠反应生成H2体积与原分子中羟基个数有关,羟基数目越多生成H2的体积越大,故由少到多顺序为①=②<③<④。
答案:(1)④>②>③>① ①<②=③<④
(2)①=②<③<④
27.6 g-10.8 g
得出n(CO)=0.05 mol
m(CO)=n(CO)×28 g·mol-1=0.05 mol×28 g·mol-1
=1.4 g,故选C。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com