
题目列表(包括答案和解析)
7.如图所示,在盛有水的烧杯中,铁 圈和银圈的连接处吊着一根绝缘的细 丝,使之平衡,小心地从烧杯中央滴 入硫酸铜溶液。片刻后可观察到的现 象是(指悬吊的金属圈)( )
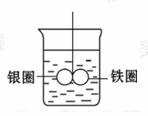
A.铁圈和银圈左右摇摆不定
B.铁圈和银圈仍保持平衡状态不变
C.铁圈向下倾斜,银圈向上倾斜
D.铁圈向上倾斜,银圈向下倾斜
[解析]选D。铁圈和银圈接触,在硫酸铜溶液中构成原电池,铁是原电池的负极,铁圈溶解,质量减小;银是原电池的正极,溶液中的铜离子在正极上被还原,产生单质铜附着在银圈上,质量增加,所以铁圈向上倾斜,银圈向下倾斜。
6.有A、B、C、D四块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;②C、D用导线相连后,同时浸入稀H2SO4溶液中,电流由D经导线流向C;③A、C相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;④B、D相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应。据此,判断四种金属的活动性顺 序是( )
序是( )
A.A>B>C>D B.A>C>D>B
C.C>A>B>D D.B>D>C>A
[解析]选B。利用原电池原理,金属与稀H2SO4溶液组成原电池,活泼金属为负极,失去电子,发生氧化反应,较不活泼的金属为正极,H+ 在正极表面得到电子,生成H2,电子的运动方向由负极移到正极,电流方向则由正极流向负极。在上述原电池中,A-B原电池,A为负极;C-D原电池,C为负极;A-C原电池,A为负极;B-D原电池,D为负极。综上可知,金属活动性:A>C>D>B。故选B。
5.下列叙述中正确的是( )
A.构成原电池的正极和负极的材料必须是两种金属
B.由铜、锌作电极与硫酸铜溶液组成的原电池中铜是负极
C.马口铁(镀锡铁)破损时与电解质溶液接触时锡先被腐蚀
D.铜锌原电池工作时,若有13 g锌被溶解,电路中就有 0.4
mol电子通过
0.4
mol电子通过
[解析]选D。两种活动性不同的金属与电解质溶液能够形成原电池,但不能因此说构成原电池的电极材料一定都是金属,例如锌和石墨电极也能跟电解质溶液组成原电池。在原电池中,活动性较强的金属失去电子流向活动性较弱的金属,因此活动性较强的金属是负极。镀锡铁表皮破损后与电解质溶液组成原电池,铁比锡活泼,铁失电子被腐蚀。铜锌原电池工作时,锌极失电子,电极反应为:Zn-2e- ====Zn2+,1 mol Zn失2 mol电子, 13 g(0.2 mol)
Zn被溶解,电路中有0.4 mol电子通过。
4.以下各反应中,生成物的总能量高于反应物的总能量的是( )
A.甲烷燃烧
B.Ba(OH)2·8H2O与NH4+Cl反应
C.铝片与盐酸反应
D.氧化钙与水反应
[解析]选B。当E反>E生时,反应放热,当E反<E生时,反应吸热。
2.(2010·重庆高一检测)一种化学冰袋中含有 Na2SO4·10H2O和NH4+NO3,使用时将它们混合用手搓揉就可制冷,且制冷效果能维持一段时间。以下关于其制冷原因的推测错误的是( )
A.Na2SO4·10H2O脱水是吸热过程
B.较长时间制冷是由于Na2SO4·10H2O脱水是较慢的过程
C.铵盐在该条件下发生的复分解反应是吸热反应
D.NH4+NO3溶于水会吸收热量
[解析]选C。Na2SO4·10H2O失水属于分解反应,也属于吸热反应;NH4+NO3吸收水并溶解于水中,是 一
一 个吸热的物理变化过程,整个过程中只是Na2SO4·10H2O的分解反应和NH4+NO3溶于水的过程,而并没有发生复分解反应,C项错误。
个吸热的物理变化过程,整个过程中只是Na2SO4·10H2O的分解反应和NH4+NO3溶于水的过程,而并没有发生复分解反应,C项错误。
|
|
 +H2(g)(放热反应)
+H2(g)(放热反应)
②SiHCl3(g)+H2(g)==== Si(s)+3HCl(g)
以下是对上述两个化学反应的叙述,其中错误的是( )
A.两个反应都是置换反应
B.反应②是放热反应
C.两个反应都有化学能与热能之间的转化
D.两个反应都是氧化还原反应
[解析]选B。反应①是放热反应,则
“Si(s)+3HCl(g)”的总能 量高于
量高于
“SiHCl3(g)+H2(g)”的总能量,进而可知反应②是吸热反应。
1.第十一届中国国际环保展览暨会议于2009年6月3日至6日在北京举行。海外展商有包括美国、法国的23个国家和地区。大会的主题是“节能减排,和谐发展。”你认为下列行为中有悖于这一主题的是( )
A.开发太阳能、水能、风能、可燃冰等新能源,减少使用煤、石油等化石燃料
B.将煤进行气化处理,提高煤的综合利用效率
C.研究采煤、采油新技术,提高产量以满足工业生产的快速发展
D.实现资源的“3R”利用观,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生( Recycle)
Recycle)
[解析]选C。化石燃料(以煤、石油、天然气为主的燃料)属于不可再生能源,且化石燃料的燃烧会产生大量污染物。所以应尽量提高化石燃料的利用率,而不能只专注于产量,故B正确,C错误,D正确。开发新能源,寻找替代品是一种较好的研究方向,A正确。
21.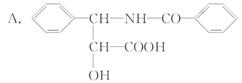 (10分)癌症严重威胁着人类的生命,为了战胜癌症,科学家正致力于研究癌症发生的机理和抗癌药物。紫杉醇(俗
(10分)癌症严重威胁着人类的生命,为了战胜癌症,科学家正致力于研究癌症发生的机理和抗癌药物。紫杉醇(俗 名)是一种新型抗癌药,其分子式为C47H51NO14,它是由如下的酸A和醇B形成的一种酯。
名)是一种新型抗癌药,其分子式为C47H51NO14,它是由如下的酸A和醇B形成的一种酯。
(分子式为:C16H15NO4)
B.R-OH(R中含C、H、O元素)
(1)写出R-OH的分子式:___________。
(2)根据A的结构,A可能发生的化学反应类型有______________________(填序号)。
①取代反应 ②消去反应 ③氧化反应 ④加成反应
(3)1 mol A与Na反应,最多可产生 _______mol H2。
(4)A中与N原子直接相连的C、H原子______(填“能”或“不能”)与N处于同一平面。
(5)已知反应:R-NH2+HCl R-NH3Cl(盐酸盐),则A在足量稀盐酸作用下可发生水解反应,其反应的化学方程式为______________________。
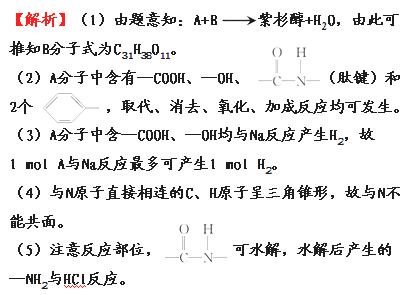
答案:(1)C31H38O11 (2)①②③④
(3)1 (4)不能
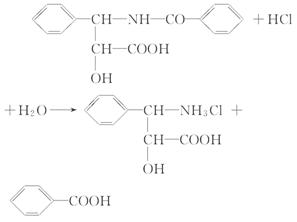 (5
(5
20.(11分)已知:A、B、F是家庭中常见的有机物,E是石油化工发展水平的标志。根据下图所示的转化关系回答问题。
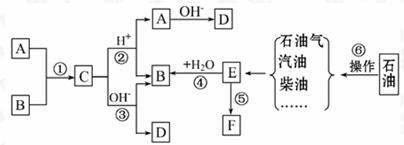
(1)操作⑥的名称为________。
(2)取代反应的范畴很广,①-⑤中属于取代反应的是_____________________(填序号)。
(3)请写出下列反应的化学方程式:
①__________________________________________;
③__________________________________________;
⑤__________________________________________。
(4)F是一种常见的高分子材料,它给我们带来了巨大的方便。然而,这种材料造成的当今的某一环境问题是______
___________________________________________。
[解析]根据“E是石油化工发展水平的标志”可知E为乙烯。一方面,乙烯可以转化成F,另一方面,乙烯与水反应生成B。结合B、F都是家庭中常见的有机物的信息,推断B是乙醇,F是聚乙烯。观察框图,C在酸性或碱性条件下都可以得到乙醇,说明C是某种酸与乙醇反应生成的酯。因为这种酸是家庭中常见的有机物,则A是乙酸。其他答案可依次推出。
19.(9分)工业上从海水中提取单质溴可采用如下方法:
(1)向海水中通入Cl2,将海水中的溴化物氧化,其离子方程式为____________________________________。
(2)向上述混合液中吹入热空气,将生成的溴吹出,用纯碱溶液吸收,其化学方程式为____________________
___________________________________________。
(3)将(2)所得溶液用H2SO4酸化,使NaBr、NaB rO3中的溴转化为单质溴,再用有机溶剂萃取溴后
rO3中的溴转化为单质溴,再用有机溶剂萃取溴后 ,还可得到副产品Na2SO4,这一过程可用化学方程式表示为_________
,还可得到副产品Na2SO4,这一过程可用化学方程式表示为_________
___________________________________________。
这样得到的溴中还混有少量Cl2,进一步净化后可得纯溴。
[解析](1)Cl2将海水中的Br- 氧化生成Br2。
(2)Br2在较高温度且碱性条件下发生自身氧化还原反应。
(3)NaBr、NaBrO3在酸性条件下发生氧化还原反应。
答案:(1)Cl2+2Br- =====2Cl- +Br2
(2)3Br2+3Na2CO3  5NaBr+NaBrO3+3CO2↑
5NaBr+NaBrO3+3CO2↑
(3)5NaBr+NaBrO3+3H2SO4 ==== 3Br2+3Na2SO4+3H2O
18.(8分)(2010·宣城高二检测)A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应。
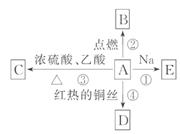
(1)A的名称_______;C的分子式为________。
(2)写出下列反应的化学方程式:
反应③______________________________________;
反应④______________________________________。
(3)比较反应① 与钠和水反应的现象有什么相同和不同:
与钠和水反应的现象有什么相同和不同:
相同点:____________________________________;
不同点:____________________________________。
[解析]本题考查了乙醇的化学性质,解题时要充分利用“结构决定性质”的思想,同时利用Na与乙醇、H2O的反应比较乙醇分子中羟基氢的活泼性,根据A能发生反应①、②、③、④,说明A为醇,又因为A为实验室中最常见的有特殊香味的有机物,所以A为乙醇,则C为乙酸乙 酯,D为CH3CHO,E为CH3CH2ONa,最后依据H2O中的羟基氢比乙醇中的羟基氢活泼即可比较出Na与乙醇、H2O反应现象的异同点。
酯,D为CH3CHO,E为CH3CH2ONa,最后依据H2O中的羟基氢比乙醇中的羟基氢活泼即可比较出Na与乙醇、H2O反应现象的异同点。
答案:(1)乙醇 C4H8O2
(2)CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
2CH3CH2OH+O2
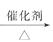 2CH3CHO+2H2O
2CH3CHO+2H2O
(3)都有无色气泡 产生,都有热量放出
产生,都有热量放出
乙醇与钠反应时,钠沉在液面下,反应更平稳
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com