
题目列表(包括答案和解析)
3.(2010·长春高一检测)下列关于有机物的说法错误的是( )
A.CCl4可由CH4制得,可萃取碘水中的碘
B.等物质的量的乙醇和乙烯完全燃烧时所需氧气的质量相等
C.乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别
D.苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应
[解析]选D。A项,CH4与Cl2发生取代反应,可生成CCl4,CCl4与水不相溶且对碘的溶解度比水大得多,可以萃取碘水中的碘;B项,乙醇分子式为C2H6O,乙烯分子式为C2H4,等物质的量的C2H6O和C2H4完全燃烧时,消耗的O2量相同;C项,乙醇与Na2CO3溶液互溶,乙酸能使Na2CO3溶液生成CO2气体,乙酸乙酯与Na2CO3溶液不相溶,可分层;D项,苯虽不能使KMnO4溶液褪色,但可以燃烧,能被氧化。
2.与乙烯所含碳、氢元素的质量分数相同,但与乙烯既不是同系物又不是同分异构体的是( )
A.环丙烷(C3H6) B.乙烷
C.甲烷 D.丙烯(CH3CH==CH2)
[解析]选A。环丙烷分子式C3H6与乙烯(C2H4)均具有相
同的最简式CH2,前者结构为 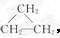 后者为CH2==CH2,
后者为CH2==CH2,
二者既不是同系物,又不是同分异构体,A正确;乙烷、甲烷属于烷烃,与乙烯中C、H元素的质量分数不同,B、C错误;丙烯与乙烯互为同系物,D错误。
1.享誉全球的2008年北京奥运会“祥云” 火炬的外壳主要采用高品质的铝合金材料 制造,在其燃烧系统内装有主要成分为丙 烷的环保型燃料。“祥云”火炬在零风速 下火焰高度达25 cm-30 cm,在强光和日 光情况下均可识别和拍摄。下列有关丙烷的叙述不正确的是( )

A.是直链烃,但分子中碳原子不在一条直线上
B.在光照条件下能够与氯气发生取代反应
C.丙烷比其同分异构体丁烷易汽化,耗氧量少
D.燃烧时主要是将化学能转变为热能和光能
[解析]选C。C3H8是直链烃,但其中的碳原子为饱和碳原子,与之相邻的四个原子为四面体结构,故3个碳原子不在一条直线上,A正确;C3H8在光照时与Cl2发生取代反应,B正确;丙烷与丁烷互为同系物,C错误;C3H8燃烧时主要是将化学能转化为热能和光能,D正确。
21.(8分)已知烯烃在氧化剂作用下,可按下式方式断裂其双键:
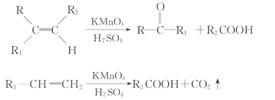
其中,R、R1、R2、R3均为烃基。
现有A、B、C三种有机物,它们之间有如下转化关系。

化合物C的结构简式为: 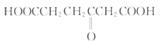
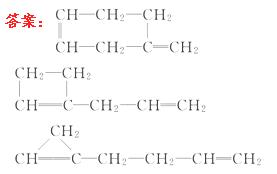
试写出A可能的三种结构简式:__________________、
__________________ 、 __________________ 。

20.(10分)取2.2 g饱和一元羧酸和饱和一元醇反应形成的液态酯,置于4 L氧气(足量)中点燃,酯完全燃烧,反应产生的气体经CaO吸收,体积减少了2.24 L(所有气体体积均换算在标准状况下)。
(1)2.2 g该酯中,C、H的物质的量分别是:C___ mol, H___ mol。该酯中,C、H、O的原子个数之比为______。
(2)根据(1)中C、H、 O的原子个数之比,能否求出该酯的分子式? _____(填“能”或“不能”),原因是___
O的原子个数之比,能否求出该酯的分子式? _____(填“能”或“不能”),原因是___
__________________________________。
(3)若该酯的分子式已求出,能否确定该酯一定是哪种酯?____(填“能”或“不能”),原因是________ _。
_。
[解析]本题的要求是确定有机物的分子式,需要用计算和推理相结合的方法解答。
(1)据题意,被CaO吸收的2.24 L气体是CO2,故2.2 g酯中含C原子0.1 mol。因为饱和一元羧酸和饱和一元醇形成的酯的通式为CnH2nO2,n(C)∶n(H)=1∶2,故2.2 g酯中含氢原子0.2
mol,则含氧原子: 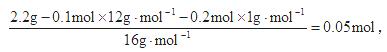
n(C)∶n(H)∶n(O)=0.1∶0.2∶0.05=2∶4∶1。
(2)因为该酯的最简式为C2H4O,则分子通式为(C2H4O)n,因为饱和一元羧酸和饱和一元醇形成的酯分子中氧原子数必为2,故可得该酯的分子式C4H8O2。
(3)分子式确定以后,要根据性质推导结构。因此,仅仅依据分子式不能确定是哪种酯,因为符合同一分子组成的酯,有多种同分异构体。
答案:(1)0.1 0.2 2∶4∶1
(2)能 该酯的分子式中氧原子个数为2
(3)不能 该酯有多种同分异构体
19.(10分)酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:
CH3COOH+C2H5OH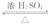 CH3COOC2H5+H2O
CH3COOC2H5+H2O
请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有_________、 _________等。
 (2)若用图所示的装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为___________、___________等。
(2)若用图所示的装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为___________、___________等。
(3)此反应以浓硫酸为催化剂,可能会造成________、________等问题。
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复作用。实验数据如表所示(乙酸和乙醇以等物质的量混合)。
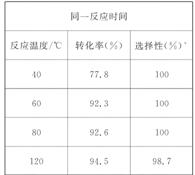

选择性100%表示反应生成的产物是乙酸乙酯和水
①根据表中数据,下列_______(填字母)为该反应的最佳条件。
A.120 ℃,4 h B.80 ℃,2 h
C.60 ℃,4 h D.40 ℃,3 h
②当反应温度达到120 ℃时,反应选择性降低的原因可能为_____________ 。
[解析](1)根据平衡移动原理可得。(2)从反应物反应的程度,是否发生副反应和冷凝的效果去考虑。(3)从催化剂重复利用,原料被炭化等角度分析。(4)①从表中数据综合分析,升高温度转化率提高,但120 ℃时选择性差,80 ℃为适宜温度,反应时间长,转化率提高,但4-6小时转化率提高不明显,可选C;②发生了副反应,有可能是乙醇脱水生成醚。
答案:(1)增大乙醇的浓度 移去生成物
(2)原料来不及反应就被蒸出 温度过高,发生了副反应 冷凝效果不好,部分产物挥发了(任填两种)
(3)产生大量的酸性废液(或造成环境污染) 部分原料炭化 催化剂重复使用困难 催化效果不理想(任填两种)
(4)①C ②乙醇脱水生成了乙醚
18.(8分)在国际环境问题中,一次性使用的聚苯乙烯
( 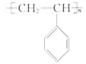 )材料所带来的白色污染问题甚为突
)材料所带来的白色污染问题甚为突
出。德国某公司开发出具有60天自行降解功能的绿色食品
袋--聚乳酸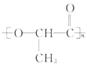 包装材料。
包装材料。
(1)聚苯乙烯造成“白色污染”的原因是____________
_____________________________。
(2)乳酸(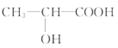 )可以从甜菜发酵的糖
)可以从甜菜发酵的糖
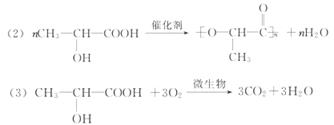
液中提取,通过缩聚反应可合成聚乳酸。合成聚乳酸的化学方程式为_______________________________ 。
(3)聚乳酸的降解可分为两个阶段,首先是化学水解成乳酸单体,然后乳酸单体在微生物的作用下分解,生成二氧化碳和水。聚乳酸自行降解的两步反应中第二步反应的化学方程式为_______________________________ 。
[解析]由乳酸合成聚乳酸实质上与由乙酸和乙醇合成乙酸乙酯一样,本质反 应是缩聚反应。
应是缩聚反应。
答案:(1)大量使用难以降解的聚苯乙烯等塑料制品,破坏土壤结构,影响市容卫生,焚烧塑料污染大气
17.(10分)现拟分离乙酸乙酯、乙酸、乙醇的混合物,如图是分离操作步骤流程图。请回答下列问题:
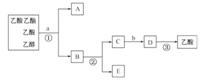
(1)写出各有关物质的名称:
A____________,B____________,C ____________,
D____________,E____________。
(2)写出加入的试剂:
a为____________ ,b为____________ 。
(3)写出有关的操作方法:
①____________,②____________,③____________。
[解析]分离3种物质要根据三者的性质进行。乙酸乙酯与饱和Na2CO3溶液不互溶,用分液法首先分离出去;然后将混合溶液与Na2CO3溶液反应,使乙酸变为乙酸钠后,熔点升高,采用蒸馏的方法分离出乙醇;再向蒸馏后的溶液中加入稀硫酸,乙酸钠还原为乙酸再蒸馏。
答案:(1)乙酸乙酯 乙酸钠和乙醇水溶液 乙酸钠溶液 乙酸和硫酸钠溶液 乙醇
(2)饱和Na2CO3溶液 稀硫酸
(3)分液 蒸馏 蒸馏
16.(9分)下列共有十种化学符号:
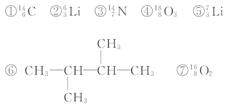
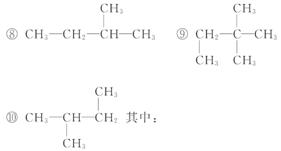
其中:
(1)互为同位素的是_________(填序号,下同)。
(2)互为同素异形体的是_____________。
(3)互为同分异构体的是_____________。
[解析]同素异形体指同种元素形成的不同单质;同分异构体是指分子式相同结构不同的化合物。
答案:(1)②和⑤ (2)④和⑦ (3)⑥和⑨
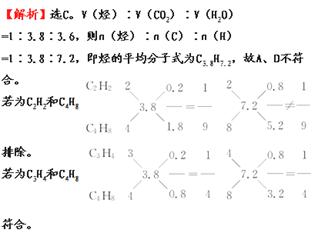
15. 有两种气态不饱和烃的混合物1体积,完全燃烧后可得3.8体积CO2和3.6体积水蒸气(气体体积均在相同条件下测定),则这两种烃是( )
有两种气态不饱和烃的混合物1体积,完全燃烧后可得3.8体积CO2和3.6体积水蒸气(气体体积均在相同条件下测定),则这两种烃是( )
A.C2H4、C4H6 B.C2H2、C4H8
C.C3H4、C4H8 D.C3H4、C3H6
第Ⅱ卷(非选择题 共55分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com