
题目列表(包括答案和解析)
2.下列气体不能用排水法收集的是( )
A.NO B.CO C.Cl2 D.NO2
思路解析:既不溶于水,又不与水反应的气体方可用排水法收集。
答案:CD
1.下列分子被称为信使分子的是( )
A.NO B.NO2 C.SO2 D.CO2
思路解析:根据学过的四种气体的性质分析四种气体中只有NO是信使分子。
答案:A
13.在一烧杯中盛有稀硫酸,有一塑料小球(与酸、碱均不发生反应)悬浮于溶液中,如右图所示。
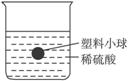
图2-1
(1)向烧杯中慢慢加入与稀硫酸密度相同(均大于1 g·cm-3)的Ba(OH)2溶液至恰好反应完全,在实验中可观察到的现象有:①_______________;②_______________。烧杯中所发生反应的化学方程式为____________________________________________________。
(2)若向烧杯中加入的不是Ba(OH)2溶液,而是锌粒,在实验中可观察到的现象有:①______________________________;②_____________________________________________。烧杯中发生反应的离子方程式为__________________________________________________。
思路解析:本题是物理与化学间的综合问题。向硫酸中加入氢氧化钡生成了硫酸钡沉淀和水,溶液中密度减小,浮力也随之减小,所以小球就会下沉;向硫酸溶液中加入锌粒,有气泡冒出,硫酸锌溶液的密度大于稀硫酸,所以浮力增大,小球上浮。
答案:(1)①溶液中有白色沉淀析出 ②塑料小球逐渐下沉 Ba(OH)2+H2SO4====BaSO4↓+2H2O
(2)①有较多气泡从溶液中逸出 ②塑料小球上浮 Zn+2H+====Zn2++H2↑
12.对溶液中的离子进行鉴定,下列实验所得结论不合理的是( )
A.溶液中加入稀硝酸后,再加入AgNO3溶液,有白色沉淀生成,则溶液中可能含有Cl-
B.溶液中加入BaCl2溶液有白色沉淀生成,再加入稀硝酸,沉淀不溶解,则溶液中一定含有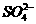
C.溶液中加入NaOH溶液,加热后产生使湿润的红色石蕊试纸变蓝的气体,则可推测该溶液中含有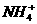
D.向溶液中加入盐酸,有使澄清石灰水变浑浊的无色无味的气体放出,可推测溶液中可能含有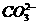
思路解析:离子鉴定的反应要符合反应规律和事实,同时现象要明显易观察。溶液中加入氯化钡后可产生的白色沉淀有多种,再加入稀硝酸,硫酸钡肯定不溶解,同时氯化银也不溶解,还有亚硫酸钡也可被稀硝酸氧化为硫酸钡而不溶解,所以B项中的结论是不可靠的。
答案:B
我创新 我超越
11.某种溶液可能含有下列阴离子中的一种或几种: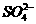 、
、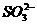 、
、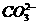 、Cl-。
、Cl-。
(1)当溶液中有大量H+存在时,则不可能有_____________存在。
(2)当溶液中有大量Ba2+存在时,溶液中不可能有_____________存在。
(3)当溶液中有_____________和_____________等阳离子存在时,上述所有阴离子都不可能存在。
思路解析:溶液中离子能共存,即是发生了离子反应。氢离子可与亚硫酸根和碳酸根反应,所以它们不能共存;钡离子可与硫酸根、亚硫酸根和碳酸根反应,所以它们在含有钡离子的溶液中不能存在;银离子可与氯离子产生沉淀,所以有钡离子和银离子的溶液中题干上的离子都不能存在。
答案:(1)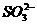 、
、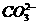
(2)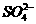 、
、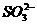 、
、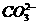
(3)Ba2+ Ag+
10.下列各组中的离子,能在溶液中大量共存的是( )
A.Mg2+、H+、Cl-、OH-
B.Na+、Ba2+、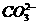 、
、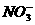
C.Na+、H+、Cl-、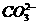 D.K+、Cu2+、
D.K+、Cu2+、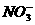 、
、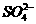
思路解析:溶液中离子能共存,即是发生了离子反应,而溶液中离子可大量共存则是没有发生离子反应。A项中氢离子与镁离子与氢氧根离子可发生反应;B项中钡离子与碳酸根离子可生成沉淀;C项中氢离子与碳酸根离子可生成气体。
答案:D
9.(2010全国高考理综Ⅰ,8)下列反应的离子方程式书写正确的是( )
A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O====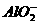 +4
+4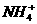 +2H2O
+2H2O
B.澄清石灰水与少量苏打溶液混合:Ca2++OH-+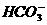 ====CaCO3↓+H2O
====CaCO3↓+H2O
C.碳酸钙溶于醋酸:CaCO3+2H+====Ca2++CO2↑+H2O
D.氯化亚铁溶液中通入氯气:2Fe2++Cl2====2Fe3++2Cl-
思路解析:Al(OH)3不溶于过量氨水,A正确写法为:Al3++3NH3·H2O====Al(OH)3↓+3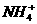 ;苏打是Na2CO3,B正确写法为:Ca2++
;苏打是Na2CO3,B正确写法为:Ca2++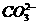 ====CaCO3↓;醋酸是弱酸,C正确写法为:CaCO3+2CH3COOH====2CH3COO-+Ca2++H2O+CO2↑;D正确。
====CaCO3↓;醋酸是弱酸,C正确写法为:CaCO3+2CH3COOH====2CH3COO-+Ca2++H2O+CO2↑;D正确。
答案:D
8.写出下列反应的离子方程式:
(1)用稀硫酸清洗铁锈(Fe2O3)
(2)碳酸钠溶液与盐酸混合
(3)硫酸铜溶液和氢氧化钡溶液混合
(4)向足量澄清石灰水中通入二氧化碳
思路解析:根据反应规律或事实首先写出化学方程式,再根据电离的实际将其改写为离子方程式即可。
答案:(1)Fe2O3+6H+====2Fe3++3H2O
(2)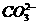 +2H+====H2O+CO2↑
+2H+====H2O+CO2↑
(3)Cu2++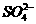 +Ba2++2OH-====BaSO4↓+Cu(OH)2↓
+Ba2++2OH-====BaSO4↓+Cu(OH)2↓
(4)Ca2++2OH-+CO2====CaCO3↓+H2O
我综合 我发展
7.将下列离子方程式改写成相应的化学方程式,正确的是( )
A.Cu2++2OH-====Cu(OH)2↓;CuCO3+2NaOH====Cu(OH)2↓+Na2CO3
B. 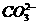 +2H+====CO2↑+H2O;BaCO3+2HCl====BaCl2+CO2↑+H2O
+2H+====CO2↑+H2O;BaCO3+2HCl====BaCl2+CO2↑+H2O
C.Ca2++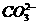 CaCO3↓;Ca(NO3)2+Na2CO3====CaCO3↓+2NaNO3
CaCO3↓;Ca(NO3)2+Na2CO3====CaCO3↓+2NaNO3
D.H++OH-====H2O;2KOH+H2SO4====K2SO4+2H2O
思路解析:将离子方程式改写成化学方程式时,因为一个离子方程式可以表示一类化学反应,所以写出的答案往往是多个。是否正确则可以将其改写成离子方程式再与已知离子方程式进行对照即可。
答案:CD
6.下列离子方程式正确的是( )
A.碳酸钙和盐酸反应: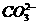 +2H+====H2O+CO2↑
+2H+====H2O+CO2↑
B.向氢氧化钡溶液中加硫酸溶液:Ba2++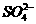 ====BaSO4↓
====BaSO4↓
C.向稀盐酸溶液中加铁:3Fe+6H+====3Fe3++3H2↑
D.向硝酸银溶液中加盐酸:Ag++Cl-====AgCl↓
思路解析:离子方程式首先要符合化学反应事实;其次因为它是化学方程式的一种特殊形式,即遵循质量守恒定律和电荷守恒定律;第三因为它反映的是离子反应的本质,所以须按电离的实际进行拆写。A项中碳酸钙不应拆写;B项中还有水,不应拆写后抵消;C项不符合化学反应的事实,因为铁只能被氢离子氧化为亚铁离子。
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com