
题目列表(包括答案和解析)
4.某有机物的结构简式为 关于该有机物的下列说法中不正确的是(
)
关于该有机物的下列说法中不正确的是(
)
A.在光照的条件下,该有机物可以与氯气发生取代反应
B.该有机物可以与溴水发生加成 反应
反应
C.该有机物可以与氢气发生加成反应
D.该有机物的分子式为C8H10
[解析]选B。光照时-CH2-CH3上的氢可被-Cl取代,A正确。该有机物不能与溴水发生加成反应,而是把溴水中的Br2萃取出来,B不正确。该有机物可在一定条件下与H2发生加成反应生成  C正确。有机物分子式
C正确。有机物分子式
为C8H10,D正确。
3.实验室用溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制:①蒸馏 ②水洗 ③用干燥剂干燥 ④10% NaOH溶液洗 ⑤水洗。正确的操作顺序是( )
A.①②③④⑤ B.②④⑤③①
C.④②③①⑤ D.②④①⑤③
[解析]选B。制得的粗溴苯中含有HBr、Br2和苯,先水洗除去HBr,再用1 0% NaOH溶液除去Br2,再水洗除去NaOH等溶液,干燥除水,最后蒸馏得纯净的溴苯。
0% NaOH溶液除去Br2,再水洗除去NaOH等溶液,干燥除水,最后蒸馏得纯净的溴苯。
2.(2010·嘉兴高一检测)绿色化学对化学反应提出了“原子经济性”(原子节约)的新概念及要求。理想的原子经济性反应是原料分子中的原子全部转变成所需产物,不产生副产物、实现零排放。下列几种生产乙苯(C6H5-C2H5)的方法中,原子经济性最好的是( )

[解析]选C。由“原子经济性”的概念可知,原料分子中的原子全部转变成所需产物,不产生副产物的反应即达到了原子经济性。分析四个选项,A、B、D反应中除了生成乙苯之外,都有副产物生成,而C选项中无副产物生成,故答案为C。
1.(多选)下列事实中,能说明苯与一般烯烃在性质上有很大差别的是( )
A.苯不与溴水发生加成反应
B.苯不与酸性KMnO4溶液反应
C.1 mol 苯可与3 mol H2发生加成反应
D.苯燃烧时冒黑烟
[解析]选A、B。苯既不能使酸性KMnO4溶液褪色,也不能与溴水发生加成反应,这是其与烯烃的明显区别之处。烃燃烧是否冒黑烟与烃含碳量的高低有关。
7.(16分)对乙醇实验的探究,包括定性探究和定量探究两个方面,本文就定性探究剖析一例,供参考。
例如有关催化剂的催化机理等问题可以从“乙醇催化氧化实验”得到一些认识,某教师设计了如图装置(夹持装置仪器已省略)。
知识支持:①有机物中含有的醛基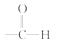 在加热条件下可与新制备的Cu(OH)2悬浊液进行反应,产生红色的沉淀--氧化亚铜(Cu2O)。实验原理为: ]
在加热条件下可与新制备的Cu(OH)2悬浊液进行反应,产生红色的沉淀--氧化亚铜(Cu2O)。实验原理为: ]
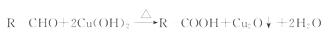
②乙醛易溶于水
实验操作:按图安装好实验装置后,先关闭活塞a、b、c,在铜丝的 中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,而有节奏(间歇性)通入气体,即可在M处观察到明显的实验现象。试回答以下问题:
中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,而有节奏(间歇性)通入气体,即可在M处观察到明显的实验现象。试回答以下问题:
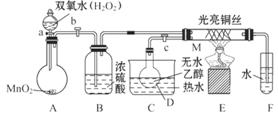
(1)A中发生反应的化学方程式:________________,
B的作用: __________________________________;
C中热水的作用:______________________________。
(2)M处发生反应的化学方程式:________________。
(3)从M管中可观察到的现象:__________________,从中可认识到该实验过程中催化剂________(填“参加”或“没参加”)化学反应,反应前后质量________(填“有”或“无”)变化。
(4)实验一段时间后,如果撤去酒精灯,反应________(填“能”或“不能”)继续进行,其原因是________。
(5)有同学认为该实验装置有不足之处是__________,
如何改善?__________________________________。
(6)验证乙醇氧化产物的化学方法是______________。
[解析](1)A是氧气发生装置,其中的二氧化锰是催化剂,化学方程式2H2O2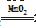 2H2O+O2↑。B是干燥氧气的装置。乙醇的沸点为78 ℃,C装置中的热水能将乙醇从液态转化成气态,乙醇蒸气进入M中参加反应。
2H2O+O2↑。B是干燥氧气的装置。乙醇的沸点为78 ℃,C装置中的热水能将乙醇从液态转化成气态,乙醇蒸气进入M中参加反应。
(2)M处发生的是乙醇的催化氧化反应,总反应式:
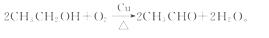
(3)装置M中的现象是:受热部分的铜丝由于间歇性地鼓入空气而交替出现变黑、变红。根据观察到的实验现象可以说明催化剂(Cu)参加了化学反应,并且催化剂起催化作用需要一定的温度(在本实验中是“加热”)。
(4)由于乙醇的催化氧化是放热反应,所以移走酒精灯反应仍可继续进行。
(5)因乙醛易溶于水,F中易产生倒吸现象,应将F改为
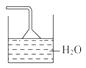
(6)要检验产物(乙醛)的存在,可以根据乙醛官能团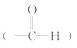
的性质,通过与新制Cu(OH)2悬浊液共热是否产生红色沉淀来判断(注:乙醛的检验这个内容,在后面还要继续学习的,这里暂不拓展,特此说明)。
答案:(1)2H2O2====2H2O+O2↑ 干燥O2
使D中乙醇变为蒸气进入M中参加反应
(2) 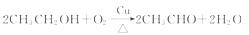
(3)受热部分的铜丝由于间歇性地鼓入空气而交替出现变黑、变红的现象 参加 无
(4)能 乙醇的催化氧化为放热反应
(5)F中易倒吸将 F改为 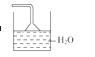
(6)实验结束后,取下装置F中盛有少量蒸馏水的小试
管,从中取出少许溶液,使之与新制Cu(OH)2悬浊液反应来证明乙醛的生成
6.(14分)中国在新工业化发展过程中,开发可再生能源以缓解石油短缺引起的能源危机是一个重要的课题。辽宁省投资建设了一个年生产500万吨工业酒精的工厂,目的是为了将工业酒精与汽油混合作为汽车燃料而减少汽油的消耗量。已知制酒精的方法有三种:
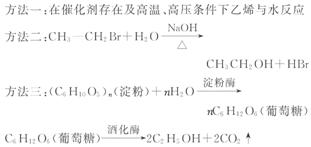
(1)你认为应用哪一种方法生产工业酒精能够缓解石油短缺带来的能源危机?为什么?______________________
________________________________________。
(2)方法一的化学反应方程式是_________________。
(3)汽车使用乙醇汽油能减少有害气体的排放吗?_____(填“能”或“不能”),为什么?________________
__________________________________________。
(4)乙醇完全燃烧的化学方程式是________________。
[解析]淀粉可以由绿色植物通过光合作用得到,是一种可再生资源,以淀粉为原料制酒精,原料来源广;而乙烯、溴乙烷都是以石油为原料制得的,石油的蕴藏量是有限的,是不可再生资源,所以以淀粉为原料制酒精的方法最佳。因为乙醇燃烧仅生成CO2和H2O,而汽油成分复杂,燃烧后除生成CO2和H2O外还会产生CO、NOx、SO2及含铅化合物等有害物质,因此汽车使用乙醇汽油可减少有害气体的排放。
答案:(1)应用方法三,因为淀粉是可再生资源,而乙烯、溴乙烷都是来自于以石油为原料制得的产品,是不可再生资源,利用它们制成酒精还不如直接利用石油
(2) 
(3)能 因为乙醇燃烧仅生成CO2和H2O,而汽油成分复
杂,燃烧后除生成CO2和H2O外还会产生CO、N Ox、SO2及含铅化合物等有害物质
Ox、SO2及含铅化合物等有害物质
(4) 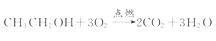
[实验·探究]
5.(思维拓展题)按如图装置,持续通入X气体,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体是( )
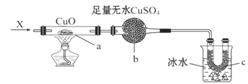
A.H2 B.CO和H2 C.NH3 D.CH3CH2OH(气)
[解析]选D。a处有红色物质生成,说明CuO被还原,而H2、CO、NH3、CH3CH2OH均能将CuO还原,b处变蓝,说明有H2O生成,A、B、C、D均可,而C处有液体生成,则A、B、C均不符合,只有CH3CH2OH+CuO
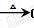 CH3CHO+Cu+H2O,所以c处为CH3CHO,故D正确。
CH3CHO+Cu+H2O,所以c处为CH3CHO,故D正确。
4.(2010·汕头高一检测)在一定温度下,乙烯和乙醇的混合气体V L,完全燃烧生成CO2和H2O,消耗相同状态下的O2
3V L,则混合气体中乙烯和乙醇的体积比为 (
)
(
)
A.1∶1 B.2∶1 C.1∶2 D.任意比
[解析]选D。C2H4-3O2,C2H6O-3O2,1体积的乙烯和乙醇均需3体积的氧气,所以二者可以任意混合。
3.(2010·临沂高一检测)类比乙烯和乙醇的化学性质,推测丙烯醇 可发生的化学反应有( )
可发生的化学反应有( )
①加成反应 ②氧化反应 ③燃烧 ④加聚反应
⑤取代反应 ⑥与Na2CO3溶液反应放出CO2
A.只有①②③⑥ B.只有①②③④
C.只有①③④⑥ D.①②③④⑤
[解析]选D。丙烯醇分子中含碳碳双键和醇羟基,故应具有烯烃和 醇的性质,但不具有酸性,以上反应中,除⑥外均可发生。
醇的性质,但不具有酸性,以上反应中,除⑥外均可发生。
2.一定质量的某饱和一元醇与金属钠反应得到3 g H2,如果把等质量的 该醇完全燃烧可得到132 g CO2,则该醇是( )
该醇完全燃烧可得到132 g CO2,则该醇是( )
A.甲醇 B.乙醇 C.丙醇 D.丁醇

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com