
题目列表(包括答案和解析)
6.( 6分)实验室制CH4是用无水醋酸钠和碱石灰固体共
6分)实验室制CH4是用无水醋酸钠和碱石灰固体共 热制取,其方程式为:H3COONa+NaOH
热制取,其方程式为:H3COONa+NaOH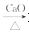 Na2CO3+CH4↑。回答:
Na2CO3+CH4↑。回答:
(1)实验室制取下列气体时,气体发生装置与实验室制取甲烷气体发生装置相同的是_______。
①H2 ②O2 ③NH3 ④NO ⑤Cl2
 (2)现有如图所示的装置,可用它来收集CH4
(2)现有如图所示的装置,可用它来收集CH4
气体。收集时,配以不同的操作方法,会形成
不同的收集方式。请简述CH4的三种收集方式。
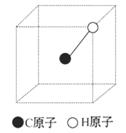 (3)已知CH4分子在空间呈四面体形状,1个C原子与4个H原子各共用一对电子形成4条共价键,C原子位于中心,4个H原子位于4个顶点。如图所示为一个立方体,已画出1个
(3)已知CH4分子在空间呈四面体形状,1个C原子与4个H原子各共用一对电子形成4条共价键,C原子位于中心,4个H原子位于4个顶点。如图所示为一个立方体,已画出1个 C原子(在立方体中心)、1个H原子(在立方体顶点)和1条共价键(实线表示),请画出另3个H原子的合适位置和3条共价键。
C原子(在立方体中心)、1个H原子(在立方体顶点)和1条共价键(实线表示),请画出另3个H原子的合适位置和3条共价键。
(2)瓶口朝上时可采用排空气法和排水法收集CH4,瓶口朝下时也可采用排空气法收集CH4。
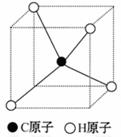
(3)由于碳原子在立方体中心,1个H原子在顶点,又因为CH4为正四面体构型,所以另3个H原子也应在立方体的顶点上,立方体余下的7个顶点可分成三类;与已知H原子同在一条棱上有3个H原子;与已知氢原子为面对 角线的位置上有3个H原子;与已知H原子为体对角线位置上有1个H原子。显然三个面对角线上的顶点即为另3个H原子的位置。
角线的位置上有3个H原子;与已知H原子为体对角线位置上有1个H原子。显然三个面对角线上的顶点即为另3个H原子的位置。
答案:(1)②、③
 (2)①瓶口朝上,B口进气;②瓶口朝上,瓶内盛满水,B口进气;③瓶口朝下,A口进气。
(2)①瓶口朝上,B口进气;②瓶口朝上,瓶内盛满水,B口进气;③瓶口朝下,A口进气。
(3)




[实验·探究]
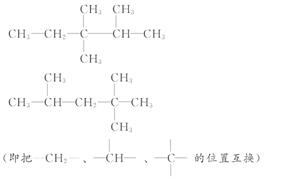
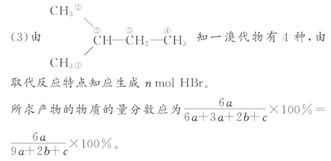
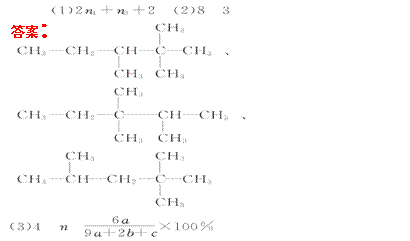
5.(2010·长春高一检测)已知丙烷的二氯代物有4种同分异构体,则其六氯代物的同分异构体的数目为( )
A.2种 B.3种 C.4种 D.5种
[解析]选C。某烃CxHy与Cl2发生取代反应,m氯取代物和n氯取代物,当m+n=y时,种类个数相同。丙烷有8个氢,则其二氯代物和六氯代物的同分异构体的数目相同,故选C。
22.4 L·mol-1=26.0 g·mol-1,在所有烷烃中,只有甲烷的相对分子质量小于26,所以A正确,B、D错误;因己烷(C6H14)在标准状况下为液体,故C也错误。
1.16 g·L-1,则关于该混合物组成的说法正确的是( )
A.一定有甲烷
B.一定有乙烷
C.可能是甲烷和己烷的混合物
D.可能是乙烷和丙烷的混合物
[解析]选A。混合物的平均摩尔质量为1.16 g·L-1×
4.有两种气态烷烃的混合物,在标准状况下其密度为
0.25 mol×(1+2+3+4)=2.5 mol。
3.1 mol CH4与一定量的Cl2在光照条件下发生取代反应,生成的四种氯代甲烷的物质的量相等,则参加反应的Cl2的物质的量是( )
A.2 mol B.2.5 mol C.3 mol D.4 mol
[解析]选B。因为生成的四种氯代甲烷的物质的量相等,即生成的氯代甲烷每种为0.25 mol,而每取代一个氢原子,则需要一个氯气分子,故所需氯气的物质的量为
2.(2010·湖南师大附中高一检测)正丁烷与异丁烷互为同分异构体的依据是( )
A.具有相似的化学性质
B.具有相同的物理性质
C.分子具有相同的空间结构
D.分子式相同,但分子内碳原子的连接方式不同
[解析]选D。分子式相同、结构不同的物质互称同分异构体,同分异构体空间结构不同,化学性质也不一定相似,物理性质不相同。
1.(2010·如东高一检测)有机化合物与人类生活水平的提高和人类社会的发展密不可分。下列对有机化合物的认识 正确的是(
)
正确的是(
)
A.有机化合物都是共价化合物
B.有机化合物都含有碳、氢元素
C.有机化合物都具有同分异构现象
D.有机物种类多是由碳原子的成键特征决定的
[解析]选D。有机化合物如CH3COONa中存在离子键,故A错。有的有机化合物中不含氢元素,如CCl4,故B错;甲烷只有一种结构,故C错;碳原子间可以形成单键,双键或叁键,同时也可形成链状结构或环状结构,故D正确。
8.(10分)为 探究乙烯与
探究乙烯与 溴的加成反应,甲同学设计并进行如下实验:先用乙醇和浓硫酸为原料制取乙烯
溴的加成反应,甲同学设计并进行如下实验:先用乙醇和浓硫酸为原料制取乙烯
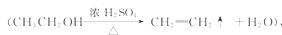
将生成 的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水
发生了加成反应。
乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量还原性的杂质气体,由此提出必须先除去杂质,再与溴水反应。
请你回答下列问题:
(1)甲同学设计的实验______(填“能”或“不能”)验证乙烯与溴水发生了加成反应,其理由是______。
A.使溴水褪色的反应,未必是加成反应
B.使溴水褪色的反应,就是加成反应
C.使溴水褪色的物质,未必是乙烯
D.使溴水褪色的物质,就是乙烯
(2)乙同学推测此乙烯中必定含有一种杂质气体是_____
____,它与溴水反应的化学方程式是______________,
在验证过程中必须全部除去。为此,乙同学设计了如图所示的实验装置:
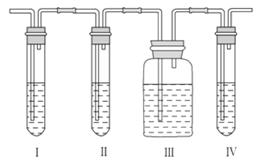
请回答:Ⅰ、Ⅱ、Ⅲ、Ⅳ装置中可盛放的试剂是:
Ⅰ______ 、Ⅱ______ 、Ⅲ______ 、Ⅳ______ 。(填序号)
A.品红溶液 B.NaOH溶液
C.溴水 D.酸性高锰酸钾溶液
能说明杂质气体存在的现象是______________________
_________ ________________。能说明乙烯与Br2发生加成反应的
________________。能说明乙烯与Br2发生加成反应的 现象是____________。
现象是____________。
(3)为验证这一反应是加成反应而不是取代反应,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是______
______________________________________。
[解析]在实验室制备乙烯过程中,由于浓硫酸具有强氧化性,可以将一部分乙醇氧化,本身被还原成SO2,SO2具有较强的还原性,可以将溴水还原,所以,要想证明乙烯能与溴水反应,必须除去SO2。证明SO2存在应在Ⅰ中加入品红溶液,由于乙烯可与酸性KMnO4溶液反应,因此,除SO2只能在Ⅱ中加入NaOH溶液。SO2有没有被彻底除去?在Ⅱ装置后必须加一个盛有品红溶液的试剂瓶,也就是说,Ⅲ中盛放的是品红溶液,在确认完全除去SO2后将气体通入盛有溴水的试管中,溴水褪色,则一定是乙烯与溴水反应的结果,但决不能认为,二者一定发生的是加成反应。
如何证明二者发生的不是取代反应呢?只能根据两种反应的特点,加成反应只有一种产物,而取代反应除了有机产物外,还有HBr生成,我们可以设法证明反应后的溶液中无HBr,则可知二者发生的反应是加成反应而不是取代反应。
答案:(1)不能 A、C
(2)SO2 SO2+Br2+2H2O====H2SO4+2HBr
A B A C Ⅰ中品红溶液褪色 Ⅲ中品红不褪色,Ⅳ中溴水褪色
(3)如发生取代反应,必定生成HBr,溶液酸性将会明显增强,故可用pH试纸验证
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com