
题目列表(包括答案和解析)
6.(14分)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫和铁的化合物。
(1)冶炼铜的反应为
8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是
_____ (填元素符号)。
(2)上述冶炼过程产生大量SO2。下列处理方案中合理的是_____ (填代号)。
a.高空排放 b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
高温
(3 )利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为:
)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为:
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
根据以上信息回答下列问题:
a.除去Al3+ 的离子方程式是_____ 。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液
NaOH溶液 碘水
所选试剂为___。证明炉渣中含有FeO的实验现象为___。

具有强还原性 ,因此,可以使高锰酸钾溶液褪色。选用的试剂是稀硫酸和高锰酸钾溶液。
,因此,可以使高锰酸钾溶液褪色。选用的试剂是稀硫酸和高锰酸钾溶液。
答案:(1)Cu、O (2)b、c (3)a.Al3+
+4OH-
====  +2H2O b.稀硫酸、KMnO4溶液 稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色
+2H2O b.稀硫酸、KMnO4溶液 稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色
[实验·探究]
4.下列说法错误的是( )
A.回收照相业中的定影液可提取镁
B.回收不锈钢可提取铬或镍以及铁
C.回收可口可乐易拉罐可回收铝
D.回收精炼铜的阳极泥可得金、银等贵重金属
[解析]选A。本题主要考查生活中常见物质的组成元素。不锈钢的主要成分是铁,并含有少量碳、铬、镍;易拉罐为铝制品;而阳极泥中则含有金、银等杂质,故B、C、D都正确。照相底片上涂有AgBr,故从定影液中可提取银而不是镁。

[解析]选D。 海水中Mg2+ 浓度比较低,首先要完成对Mg2+
的富集(用石灰乳使Mg2+ 变为沉淀)。MgO的熔沸点远高于MgCl2,故电解MgO要比电解MgCl2更耗能。
海水中Mg2+ 浓度比较低,首先要完成对Mg2+
的富集(用石灰乳使Mg2+ 变为沉淀)。MgO的熔沸点远高于MgCl2,故电解MgO要比电解MgCl2更耗能。
3.(2010·朝阳区高一检测)下表中金属的冶炼原理 与方法不完全正确的是( )
与方法不完全正确的是( )
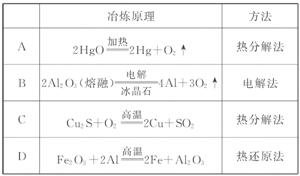
[解析]选C。活泼金属K、Ca、Na、Mg、Al等用电解法冶炼,中等活泼金属Zn、Fe、Sn、Pb、Cu等用热还原法冶炼,不活泼金属Hg、Ag利用热分解法冶炼,故A、B、D正确,C错误。
2.下列说法不正确的是( )
A.自然界中不存在游离态的金属单质
B.金属活动性不同,冶炼方法也有所不同
C.地球上金属矿物资源是有限的,因此,应提高金属矿物的利用率
D.废旧金属的回收利用,有利于环境保护
[解析]选A。自然界中的金属绝大多数以化合态形式存在,极少数金属如Au、Pt等以游离态存在,A错误;金属活动性不同,金属阳离子被还原的难易程度不同,冶炼方法不同,B正确;金属资源是有限的,既要提高金属矿物的利用率,又要回收利用 废旧金属,C、D正确。
废旧金属,C、D正确。
1.(多选)下列物质在冶炼过程中,需加入还原剂的是( )
A.HgO B.Al2O3
C.Fe2O3 D.CuSO4
[解析]选C、D。在冶炼金属的方法中,只有热还原法需要加入还原剂。这种方法适合冶炼金属活动性顺序表中间部分的金属如Fe、Cu,而后面的金属如Hg适合用热分解法,前面的金属如Al适合用电解法。
(四)______________________________ 。
(2)框图中加入的试剂①应该是_____ (填“化学式”);加入的试剂②是 _____ (填“化学式”);工业上由无水MgCl2制取镁的化学方程式为: _____。
[解析](1)因为海水中Mg2+ 浓度小,直接向海水中加入沉淀剂,必然消耗大量的沉淀剂,浪费原料,方法1不正确;若高温加热蒸发海水,虽然能提高Mg2+ 的浓度,但这样会消耗大量能源,方法2不正确;可以向太阳光蒸发浓缩后的海水中加入沉淀剂,这样既提高了Mg2+ 浓度,又节约能源与原料,最合理。
(2)试剂①的作用是将Mg2+ 沉淀为Mg(OH)2,再结合原料经济方面考虑,试剂①应为Ca(OH)2,试剂②作用是将
Mg(OH)2溶解生成MgCl2,结合不引入新的杂质分析,试剂②应为盐酸。
答案:(1)(一)海水中镁离子浓度小,沉淀剂的用量大,不经济
(二)不正确 (三)能源消耗大,不经济 (四)向太 阳光蒸发浓缩后的海水中,加入沉淀剂(合理均可)
阳光蒸发浓缩后的海水中,加入沉淀剂(合理均可)
(2)Ca(OH)2 HCl
MgCl2(熔融) Mg+Cl2↑
Mg+Cl2↑
(三)_____________________ _________
;
_________
;
(二)______________________________ ;
(一)______________________________ ;
6.(10分)海水中溴元素以Br- 形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如图:

(1)步骤①反应的离子方程式是_____ 。
(2)步骤③反应的化学方程式是_____ ,
从理论上考虑,下列也能吸收Br2的是_____ 。
A.NaO H B.FeCl2 C.Na2SO3 D.H2O
H B.FeCl2 C.Na2SO3 D.H2O
(3)Br的原子序数是_____ ,在周期表中位于第_____
周期_____族。
(4)步骤⑤蒸馏的过程中,温度应控制在80℃-90℃。温度过高或过低都不利于生产,请解释原因________。
(5)为什么不直接用“溴水混合物Ⅰ”而要用“溴水混合物Ⅱ”进行蒸馏得到液溴________。
[解析](1)(2)(3)问相对简单,读懂流程图,结合学过的重点方程式,可以写出2Br- +Cl2====Br2+2Cl-,
SO2+Br2+2H2O====2HBr+H2SO4;只从理论上考虑,NaOH具有
强碱性,能吸收Br2,Fe2+ 、 具有强还原性也能吸收
Br2,但Br2在水中的溶解度较小,不能充分吸收。溴是35号元素,位于第四周期ⅦA族。
(4)温度过高,大量水蒸气随溴排出,溴气中水蒸气的含量增加,温度过低,溴不能完全蒸出,产率太低。
(5)“溴水混合物Ⅰ”中虽然含有溴单质,但浓度低,如果直接蒸馏,处理量大,生产成本高。经过“空气吹出、SO2吸收、氧化”等步骤实际上是将溴水浓缩了。
答案:(1) 2Br- +Cl2====Br2+2Cl-
(2)SO2+Br2+2H2O====2HBr+H2SO4 A、B、C
(3)35 四 ⅦA
(4)若温度过高,大量水蒸气随溴排出,溴气中水蒸气的含量增加,温度过低,溴不能完全蒸出,产率太低
(5)“溴水混合物Ⅰ”中虽然有溴单质,但浓度低,如果直接蒸馏,处理量大,生产成本高,而“溴水混合物Ⅱ”实际上将溴水浓缩了
7.(10分)海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了如图所示实验:
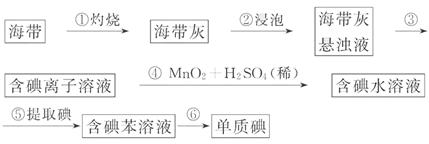
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是_____ (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯
F.干燥器
(2)步骤③的实验操作名称是_____ ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是_____ 。
(3)步骤④反应的离子方程式是_____ 。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是___。
(5)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法:_____。
[解析](1)灼烧用到的仪器有:酒精灯、三脚架、泥三角、坩埚、坩埚钳。列出实验仪器的方法是:①从实验装置由下而上;②从实验步骤先后用到顺序列出。(2)物质分离方法是:固液分离用过滤;液液不互溶用分液,液液互溶用蒸馏。(3)利用MnO2的氧化性把I- 氧化。(4)因为苯与水互不相溶,且I2在苯中的溶解度比在水中大,故萃取剂可用苯。
(5)利用I2遇淀粉变蓝的特性来检验。
答案:(1)B、D、E
(2)过滤 蒸馏
(3)2I- +MnO2+4H+ ====Mn2+ +I2+2H2O
(4)苯与水互不相溶,碘在苯中的溶解度比在水中大
(5)取少量提取碘后的水溶液于试管中,加入几滴淀粉试液,观察是否出现蓝色(如果变蓝,说明还有单质碘)
[实验·探究]
8.(10分)目前世界上60%的镁是从海水中提取的。学生就这个课题展开了讨论。已知海水提镁的主要步骤如下:

 (1)关于加入试剂①作沉淀剂,同学们提出了不同方法。请你参与他们的讨
(1)关于加入试剂①作沉淀剂,同学们提出了不同方法。请你参与他们的讨 论:
论:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com