
题目列表(包括答案和解析)
25.(12分)D、E、X、Y、Z是短周期元素,且原子序数逐渐增大,D、E的最简单氢化物分子的空间结构依次是正四面体、三角锥型,X原子的最外层电子数是次外层电子数的一半,Y元素的最高正价和最低负价的代数和为4,Z元素的原子是所处周期中原子半径最小的。回答下列问题:
(1)D和Z形成的化合物的结构式是_________;D和Y形成的分子的名称是_ ___。
(2)Y和Z的简单离子的半径大小为__________(用离子符号和“>”、“=”或“<”表示)。
(3)比较元素非金属性的强弱有很多方法,关于D和X的非金属性强弱的研究方案中不可行的是_________(填序号)。
①比较氢化物的稳定性 ②依据两元素在周期表的位置 ③比较两种单质的颜色
④比较单质与H2化合的难易程度 ⑤比较最高价氧化物对应水化物的酸性
(4)当满足一定比例时,Z的单质可与E的最简单氢化物反应生成一种盐和另一种单质,试写出该反应的化学方程式________________________。
(5)写出下列反应的化学方程式:
①工业上用D的单质制X的单质___________________________________;
②E的最高价含氧酸的浓溶液与单质D反应__________________________。
(6)E有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L甲气体与0.5L氧气混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,则生成的E的含氧酸盐的化学式是__________。
24.(10分)下表中的实线表示元素周期表的部分边界。①-⑥分别表示元素周期表中对应位置的元素。
|
① |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
③ |
④ |
⑤ |
|
|
|
② |
|
|
|
|
|
|
|
|
|
|
|
|
⑥ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1 )请在表中用粗实线补全元素周期表边界。
)请在表中用粗实线补全元素周期表边界。
(2)②号元素位于第 周期 族。
(3)写出由①、③两种元素组成的摩尔质量最小的化合物的电子式 ,上述元素中能和⑤号元素形成的原子晶体的化学式是
(4)上述元素中的一种元素其气态氢化物和该元素的最高价氧化物的水化物能发生化合反应,该反应的化学反应方程式为_____________,该生成物质含有的化学键类型是 。
23. (6分)指出硫酸在下列用途或反应中表现的性质A.高沸点B.强酸性C.吸水性D.脱水性E.强氧化性F.催化作用(填序号)
(1)实验室制取H2 ;(2)可用作H2、SO2等气体的干燥剂
(3)铝制容器可盛放浓H2SO4 ;
(4) 浓H2SO4使湿润的蓝色石蕊试纸先变红后变黑
(5)浓H2SO4溶解金属铜 (6)浓H2SO4加到浓盐酸中产生白雾
22.下表为元素周期表前三周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
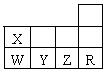 A.常压下五种元素的单质中Z单质的沸点最高
A.常压下五种元素的单质中Z单质的沸点最高
B.Y、Z、W的阴离子的还原性强弱顺序为:Z- >Y2->W3-
C.最高价含氧酸的酸性强弱顺序为:H2YO4>HZO4>H3WO4
D.五种元素对应的单质固态时均为分子晶体
21. 某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如下图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3的物质的量浓度之比为( )
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如下图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3的物质的量浓度之比为( )
A.2∶1∶4 B.1∶2∶4
C.1∶2∶1 D.1∶1∶4
20.浅绿色的Fe(NO3)2溶液中逐渐加入少量稀盐酸时,溶液的颜色变化应该是( )A.颜色变浅 B.变为红色 C.没有改变 D.变为黄色
19.某0.01mol/L的稀硝酸溶液恰好氧化一定质量的铁、铝混合物,已知两种金属均被氧化为最高价态,还原产物只有NO。若用0.01mol/ L的NaOH溶液溶解相同质量的该混合物,所需碱液的体积是稀硝酸溶液的1/5,则样品中铁、铝的物质的量之比为( )
L的NaOH溶液溶解相同质量的该混合物,所需碱液的体积是稀硝酸溶液的1/5,则样品中铁、铝的物质的量之比为( )
A.2:3
B.1:3  C.1:4
D.5:3
C.1:4
D.5:3
18. 类推的思维方式在化学学习研究中有时会产生错误的结论,因此类推的结论最终要经过实践的检验才能决定其正确与否,以下几个类推的结论中不正确的是( )
①由H2O在液态时分子间存在氢键,类推出C2H5OH在液态时分子间也存在氢键。
②SO2能与碱反应,推测:非金属氧化物都能与碱反应
③金属钠着火不能用CO2扑灭,推测:金属钾着火也不能用CO2扑灭
④由不能用电解熔融状态AlCl3来制取铝,类推出也不能用电解熔融状态MgCl2溶液制取镁。
A.①② B.②④ C.②③④ D.①②③④
17.已知短周期元素的离子:aAm+、 bBn+、cCm-、 dDn-(m>n)都具有相同的电子层结构,则下列叙述正确的是( )
A.原子半径:A>B>C>D B.原子序数:d>c>b>a
C.离子半径:C>D>B>A D.单质的还原性:A>B>D>C
16.北京大学和中国科学院的化学工作者已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子晶体,具有良好的超导性。下列有关分析正确的是( )
A.K3C60中只有离子键 B.K3C60中碳元素显-3价
C.该晶体在熔融状态下能导电 D.C60与12C互为同素异形体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com