
题目列表(包括答案和解析)
联系:分子是由原子构成的。分子、原子都是构成物质的微粒。
区别:化学变化中,分子可分,原子不可分。
6.物质的分类:
物质的分类:
根据组成物质的成份不同,可分为纯净物和混合物。在纯净物中含有不同种元素的物质称化合物,如P2O5、KClO3、CuCl2等。含有同种元素的纯净物的称单质,如:Fe、Cu、O2、He等。由两种元素组成的化合物,若其中有一种元素是氧元素,这种化合物称为氧化物,必须注意的是氧化物一定含氧元素,但含氧元素的化合物不一定是氧化物,如KMnO4、H2SO4等都含氧元素,但它们分别由三种元素组成,不属氧化物。
 组成:物质(纯净物)由元素组成
组成:物质(纯净物)由元素组成
 原子:金属、稀有气体、碳、硅等。
原子:金属、稀有气体、碳、硅等。
物质 构成 分子:如氯化氢由氯化氢分子构成。 H2、O2、N2、Cl2。
离子:NaCl等离子化合物,如氯化钠由钠离子(Na+)氯离子(Cl-)
 混合物(多种物质)
混合物(多种物质)
 分类 单质 :金属、非金属、稀有气体
分类 单质 :金属、非金属、稀有气体
纯净物 (一种元素)
 有机化合物
CH4、C2H5OH、C6H12O6、淀粉、
有机化合物
CH4、C2H5OH、C6H12O6、淀粉、
 化合物:
氧化物
H2O Cu
化合物:
氧化物
H2O Cu
无机化合物 酸 HCl H2SO4 HNO3
碱 NaOH Ca(OH)2
盐 NaCl CuSO4 Na2CO3
重难点例题:
例1.下列说法正确的是
A、由一种元素组成的物质一定是单质
B、由不同种元素组成的物质一定是混合物
C、由不同种元素组成的物质叫化合物
D、自然界存在的河水、泉水均为混合物
简析:本题考查对纯净物、混合物、单质、化合物的认识。单质、化合物一定是纯净物,同种元素可以组成不同的单质,如磷元素可组成红磷、白磷,因此由一种元素组成的物质可以是纯净物,也可以是混合物,由同种元素形成的混合物不是单质。由不同种元素组成的物质可以是混合物,也可以是纯净物,若为纯净物,这类物质属于化合物。自然界的水:河水、海水、泉水、井水等均属混合物。
答案:D
例2.用分子观点对下列常见现象的解释,错误的是
A、热胀冷缩-分子大小随温度的变化而变化
B、花香四溢-分子不停地运动
C、酒精挥发-分子间间隔变大和分子运动
D、食物腐败-分子发生了变化
简析:本题是对分子性质的考查。每种物质的分子其组成、结构等是一定的,热胀冷缩只是组成物质的分子之间距离发生变化,分子大小是不变的。花香四溢是由于花中具有香味的分子运动使人嗅到香味。酒精挥发是酒精由液态变为气态,不仅说明分子运动,也说明分子间的间隔变大了,因此B、C、D的解释都正确。A不正确
答案:A
例3.水是人类生活不可缺少的物质。下列有关水的叙述不正确的是
A、水是由氢元素和氧元素组成的氧化物
B、用肥皂水可以区分硬水和软水
C、氢气燃烧生成水和电解水的基本反应类型相同
D、净化水的常用方法有吸附、沉淀、过滤和蒸馏
简析:本题是有关水知识的综合性试题,试题的知识内涵比较丰富,A考查对氧化物概念的认识,B是区分硬水和软水的最简便、快捷的方法,硬水中含有较多的可溶性钙、镁化
合物,遇肥皂水会产生白色的垢状物,且泡沫很少。氢气燃烧生成水是化合反应
|
|
答案:C
例4.右图为自来水厂净化过程的示意图。请判断净水过程中,有化学变化发生的是
A、从水库取水
B、通过过滤池
C、通过活性炭吸附池
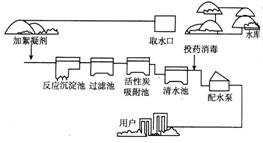 D、投药消毒
D、投药消毒
简析:本题以自来水的净化过程为知识载体,考查学生对自来水净化过程中物质变化的认识。自来水的净化过程中,取水、沉淀、过滤、用活性炭吸附等都没有新物质生成,因此只发生了物理变化,而投药消毒所投入的是一些具有强氧性的物质。如O3(臭氧)、Cl2(氯气)等通过化学反应杀死水中的病毒,达到消毒的目的。
答案:D
例5.渭河被称为“陕西的母亲河”。长期以来,渭河的污染严重。地方政府投入大量的资金进行综合治理。下列是互联网上网民对水卡污染治理的一些建议,你认为不合理的是
A、坚决杜绝使用农药和化肥
B、严禁在河边随意堆放生活垃圾
C、工业废水经过处理,达到标准后再排放
D、严禁在河边两岸新建化工、造纸等严重污染的工厂
简析:本题以综合治理水污染为背景材料考查学生对于水污染的认识。
农药、化肥对农业生产起着重要的作用,但过量使用会造成水污染,因此,必须合理使用,不能因噎废食。河边堆放生活垃圾,垃圾中的废液渗入土壤以及随雨水等流入河中。河边建有严重污染的工厂,工厂废水直接排入河里等均能污染河水。
答案:A
例6.2008年5月12日14时28分,在四川汶川县发生了8.0级的地震,地震是一种突发的自然灾害,震后的生态环境和生活条件都受到了极大的破坏,卫生基础设施损坏严重,供水设施受到了破坏,饮用水受到污染,是导致传染病传染的潜在因素,能否解决群众的供水问题是关系到震后能否控制大疫的一个关键问题,灾区人们日常生活用水及饮用水都要经过一系列的净化才能使用,请你解决如下问题:
(1) 为了出去水中的不溶性杂质,可以采取的措施:
(2) 当地震过去后,你如何将污水变成清洁的用水?
(3) 除去河水中的不溶性的杂质后,请你设计一个实验证明水师硬水:
(4) 有人说:饮用天然的矿泉水对人体的健康是有益的,矿泉水中微量的元素的含量越多越好。你认为这种说法正确吗,为什么?
点拨:在众多的净化与处理方法中,既有物理方法也有化学方法,有的时候是物理方法和化学方法共同使用,只要明确他们的基本原理就不会出错了。
答案:(1)过滤 (2)先静置,加入明矾,沉淀,再加入活性炭,过滤(其他合理的答案均可) (3)取适量的水样品,加入肥皂水,观察泡沫的多少,泡沫较少,则为硬水
(4)不正确,人体对元素的需求是均衡的
综合训练:
2、根据氢氧化钠和氢氧化钙的组成和性质,对下表内容进行研究和讨论
|
碱溶液的组成特点 |
|
|
碱溶液的共同性质 |
|
|
碱有共性的原因 |
|
[经典例题]
实验探究:氢氧化钠溶液中哪一种粒子(H2O、Na+、OH-)能使无色酚酞试液变红。
|
你的问题 |
实验步骤 |
实验现象 |
实验结论 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[分析]氢氧化钠溶液能使无色酚酞试液变红色,在溶液中存在H2O、Na+、OH-等粒子,哪一种粒子能使无色酚酞试液变红呢?围绕问题进行探究。
1、小结学习过的氢氧化钠、氢氧化钙和氨水的知识,并作交流。
|
名称 |
化学式、俗称 |
物理性质 |
化学性质 |
重要用途 |
|
氢氧化钠 |
|
|
|
|
|
氢氧化钙 |
|
|
|
|
|
氨水 |
|
|
|
|
3、学会用探究的方法认识碱的性质。
[知识整理]
2、会用酸碱指示剂检验溶液的酸碱性和使用PH试纸测定溶液的酸碱度;知道酸碱性
对生命活动和农作物生长的影响;会用溶液酸碱性的知识解释生活中的一些有关现象。
1、知道烧碱、消石灰、氨水的物理性质;了解氢氧化钠、氢氧化钙的主要化学性
质及用途;认识强碱的腐蚀性。
3、会用溶液酸碱性的知识解释生活中的一些有关现象。学会用探究的方法认识酸的
性质。
[知识整理]
小结学过的盐酸、硫酸的知识,并作交流
盐酸、硫酸相关知识
|
酸 |
物理性质(浓酸) |
化学性质(稀酸) |
相似的化学性质 |
重要用途 |
|
盐酸 |
|
|
|
|
|
硫酸 |
|
|
|
[经典例题]
盐酸和硫酸是实验室里常用的试剂,现有两瓶没有标签的稀盐酸和稀硫酸,请你设计出
三种不同的实验方案来鉴别它们,并要求三种方案的实验现象不相同。
|
项目 |
实验步骤 |
实验现象和结论 |
|
方案1 |
|
|
|
方案2 |
|
|
|
方案3 |
|
|
[分析]盐酸、硫酸是初中化学学习的重要物质,它们的性质有相似之处,又有许多不同之处,利用它们不同的性质多角度加以鉴别
2、会用酸碱指示剂检验溶液的酸碱性和会使用PH试纸测定溶液的酸碱度;知道酸
碱性对生命活动和农作物生长的影响。
1、 知道浓硫酸、浓盐酸的物理性质;了解盐酸、稀硫酸的主要化学性质及用途;认
识酸的腐蚀性。
11、(2)NaHCO3+HCl==NaCl+CO2↑+ H2O
(4)①应先将导管从烧杯中取出,再熄灭酒精灯
②碳酸氢钠受热会分解,碳酸钠受热不分解(或碳酸钠比碳酸氢钠稳定)
(5)碳酸氢钠的水溶液呈碱性,能使酸碱指示剂变色;它可与酸发生反应;它可与碱反应;它受热能分解。(任选三个性质)
(6)方案:取10g固体样品加热,可利用质量守恒定律,称量残留固体质量,得到质
量差(4.4g)即为气体二氧化碳的质量,可计算得到碳酸氢钠质量和质量分数。或取10g
固体样品加入盐酸50g(足量)充分反应,可利用质量守恒定律,称量反应后溶液质量,
得到差量(4.4g)即为气体二氧化碳质量,可计算得到碳酸氢钠质量和质量分数。或取
10g固体样品,加入7.3%的稀盐酸至恰好不再有气泡产生,共消耗了盐酸50g,将盐酸的
溶质质量代入计算,可计算得到碳酸氢钠质量和质量分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com