
题目列表(包括答案和解析)
8.有M和R两种短周期主族元素,已知M+与R2-核外电子数之和为20,则下列说法正确的是 ( )
A.R一定是第二周期元素
B.M一定是第三周期元素
C.M与R是同一周期元素
D.R与M元素组成的化合物中可能存在非极性键
7.下列说法中正确的是 ( )
A.IA族元素的金属性比IIA族元素的金属性强
B.熔融状态下能导电的物质一定是离子化合物
C.在NaCl晶体中存在单个小分子
D.构成单质分子的微粒可能不含化学键
6.下列说法正确的是( )
A.阳离子的氧化性:Li+<Na+<K+
B.碱金属单质的熔沸点随着核电荷数的增大而升高
C.卤素单质的密度随核电荷数的增大而增大
D.卤素单质氧化性强的可以将氧化性弱的从它的盐溶液中置换出来
5.根据下表信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价
|
元素代号 |
L |
M |
Q |
R |
T |
|
原子半径/nm |
0.160 |
0.143 |
0.112 |
0.104 |
0.066 |
|
主要化合价 |
+2 |
+3 |
+2 |
+6、-2 |
-2 |
A.氢化物的还原性为H2T>H2R
B.单质与稀盐酸反应的速率为L<Q
C.L、M、R的最高价氧化物的水化物两两之间均能反应
D.离子半径:L2+<R2-
4.9.2g金属钠投入到足量的重水中,则产生的气体中含有( )
A.0.2mol中子 B.0.4mol电子 C.0.2mol质子 D.0.4mol分子
3.W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是 ( )
A.金属性;Y>Z B.氢化物的稳定性:X>W
C.离子的还原性:X>W D.原子及离子半径:Z>Y>X
2. 下列有关化学用语使用正确的是 ( )
下列有关化学用语使用正确的是 ( )
A.硫原子的原子结构示意图:
B.NH4Cl的电子式:
C.氮气的结构式::N≡N:
D.原子核内有10个中子的氧原子:
1.某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为152.0,原子核外的电子数为63。下列叙述错误的是 ( )
A.它是副族元素 B.它是第六周期元素
C.它的原子核内有63个质子 D.它的一种同位素的核内有89个中子
28.为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,
其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥
管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的打气球。
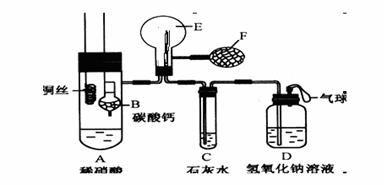
⑴实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先除去其中的空气。
其中第一步实验操 作为 ▲
。从装置的设计看,
作为 ▲
。从装置的设计看,
确定E中空气已被赶尽的实验现象是 _____▲_________。
⑵将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反
应的离子方程式为 ▲ 。有人认为E中收集
到的可能是H2而不是NO,如何证明? ▲ 。
⑶氮氧化物进入大气后,不仅会形成硝酸 型酸雨,还可能形成光化学烟雾。因此装
型酸雨,还可能形成光化学烟雾。因此装
置D的作用是 ▲
⑷用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
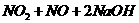 =
=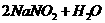
在该反应中,氧化剂是 ▲ ,还原剂是 ▲ 。
⑸汽车尾气中含有一氧化氮和一氧化碳,经过排气管中的催化转化器转化为对大气
无 污染的物质。写出该反应的化学方程式:
▲ 。
污染的物质。写出该反应的化学方程式:
▲ 。

27.(19分)
|
① |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
② |
③ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
④ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
丙 |
|
|
丁 |
|
甲 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
乙 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
⑴ 在上面元素周期表中,全部是金属元素的区域为 ▲ (填字母代号)
A.甲 B.乙 C.丙 D.丁
 ⑵用实线画出金属与非金属的分界线(在答题卷图上完成)。 ▲
⑵用实线画出金属与非金属的分界线(在答题卷图上完成)。 ▲ 
⑶已知R元素的某种原子的质量数为28,且质子数与中子数相等,请在答题卷中的周期表中标出“R” 元素的位 置(在答题卷图上完成)。 ▲
置(在答题卷图上完成)。 ▲
⑷在我们常用的周期表中,①元素的位置比较尴尬,它是第1列的唯一非金属元素。有人认为也可把①元素放在VIIA族,支持这个理由的观点是___ ▲ _______。
A.HF B.H+ C.NaH D.H2O2
⑸请问,若用①②④三种元素 ▲ (填“能”或“不能”)形成离子化合物;
若能,请写出该物质的化学式____▲_____(若不能,此格不填)
 若用球棍模型表示①和③形成的化合物的分子结构,应该是 ▲ 。
若用球棍模型表示①和③形成的化合物的分子结构,应该是 ▲ 。
(6)常温下,D与R相邻,D原子的电子层数与最外层电子数相等,请写出D原子
形成的简单离子的结构示意图 ▲ 。D单质能与④元素的最高价氧化物
对应水化物反应,请写出该反应的离子方程式为 ▲ (该格3分)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com