
题目列表(包括答案和解析)
13.活泼金属氢化物是火箭燃料的重要供氢剂,如氢化钠、氢化钙等。例如,氢化钙的供氢原理是CaH2+2H2O=Ca(OH)2+2H2 下列有关分析中正确的是( )
A.氢化钙中含共价键,水中含非极性键
B.氢氧化钙只存在离子键
C.水分子和氢分子中都存在氢氢非极性共价键
D.该反应断裂离子键和共价键,生成离子键和共价键
12、等质量的两份锌粉a、b中分别加入过量的稀硫酸,同时向a中加入少量的CuSO4溶液,下列各图表示的是产生H2的体积V与时间t的关系,其中正确的是 ( )
 A、
B、
C、
D、
A、
B、
C、
D、
11.下列事实能说明氯元素原子得电子能力比硫元素强的是( )
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强 ③HCl的稳定性比H2S强 ④HCl的还原性比H2S强 ⑤HClO的酸性比H2SO4强 ⑥Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑦Cl2能与H2S反应生成S ⑧还原性:Cl-<S2-
A.③④⑤⑦⑧ B.③④⑥⑦⑧ C.③⑥⑦⑧ D.①②③④⑤⑥⑦⑧
10.下列电子式中正确的是( )
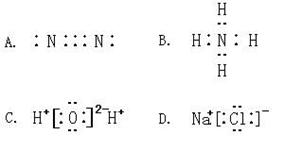
9.下列说法不正确的是( )
A.元素周期表中,除第一和第七周期外,第n周期所含非金属元素(包括稀有气体元素)的种数均为(8-n)
B.SiCl4、PCl3分子中各原子最外层均达到8电子稳定结构
C.同素异形体之间的相互转化都属于物理变化
D.由ⅠA族和ⅥA族短周期元素形成的原子个数比为1∶1,电子总数为38的化合物,是含有共价键的离子型化合物
8.下列各组化合物中,化学键的类型相同的是( )
①CaCl2和Na2S ②Na2O和Na2O2
③CO2和CS2 ④HCl和NaOH
A.①③ B. ②④ C.①④ D.③④
7. 下列说法正确的是( )
A.化学反应速率是对可逆反应而言的,非可逆反应不谈化学反应速率
B.在可逆反应里,正反应的化学反应速率是正值,逆反应的化学反应速率是负值
C.在同一化学反应里,其化学反应速率可以用反应物浓度的改变来表示,也可以用生成物浓度的改变来表示,其数值可能相同,也可能不相同
D.化学反应速率的单位可以是g·L-1·s-1,也可以是Kg·L-1·s-1,甚至可以用t·L-1·s-1等来表示。
6.元素在周期表中的位置, 反映了元素的原子结构和元素的性质,下列说法正确的是( )
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层都达到8电子稳定结构
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
5.已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系
正确的是( )
A.质子数c>d B.离子的还原性Y2->Z-
C.氢化物的稳定性H2Y>HZ D.原子半径X<W
4.某元素的一种同位素X的质量数为A,含N个中子,它与氢原子组成HmX分子。在a g HmX中所含质子的物质的量是( )

 A. (A-N+m)
mol B. (A-N)
mol
A. (A-N+m)
mol B. (A-N)
mol

 C. (A-N)
mol D.
(A-N+m) mol
C. (A-N)
mol D.
(A-N+m) mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com