
题目列表(包括答案和解析)
15. 北京大学和中国科学院的化学工作者合作已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子化合物,且有良好的超导性。下列关于K3C60的组成和结构的分析正确的是
A. K3C60中只含离子键,不含有共价键 B. 1 mol K3C60中含有的离子数目为63×6.02×1023个
C. 该化合物在熔融状态下能导电 D. 该物质的化学式可定为KC20
14. 有下列五种说法:①相邻原子间强烈的相互作用,叫做化学键;②两个非金属原子间不可能形成离子键;③非金属原子间不可能形成离子化合物;④离子化合物中不能存在共价键;⑤某化合物的水溶液能导电,则该化合物中一定存在离子键,其中正确的是
A.①② B.②③④ C.②④⑤ D.①②③④⑤
13. 为了探究温度对化学反应速率的影响,下列实验方案可行的是.k*s5*u
A.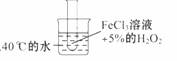
B.
C.
D.
12. 当A、B两种元素的原子分别获得2个电子形成稳定结构时,A放出的能量大于B放出的能量;当C、D两种元素的原子分别失去1个电子形成稳定结构时,D吸收的能量大于C吸收的能量。A、B、C、D之间分别形成化合物时,属于离子化合物可能性最大的是
A.D2A B.C2B C.C2A D.D2B
11. 根据表中信息,判断以下叙述正确的是
部分短周期元素的原子半径及主要化合价
|
元素代号 |
L |
M |
Q |
R |
T |
|
原子半径/nm |
0.160 |
0.143 |
0.112 |
0.104 |
0.066 |
|
主要化合价 |
+2 |
+3 |
+2 |
+6
-2 |
-2 |
A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性 D.L2+ 与R2- 的核外电子数相等
10. 已知自然界氧的同位素有16O、17O、18O,氢的同位素有H、D,从水分子的原子组成来看,自然界的水一共有
A.3种 B.6种 C.9种 D.12种
9. 国际无机化学命名委员会在1989年作出决定,把长式周期表原先的主、副族及族号取消,从左到右改为第 1-18列,第ⅠA族为第1列,稀有气体元素为第18列。按这个规定,下列说法不正确的是
A.第15列元素的最高价氧化物为R2O5 B.第2列元素中肯定没有非金属元素
C.第17列元素的第一种元素无含氧酸 D.第16、17列元素都是非金属元素
8. 三种最外层电子数相同的非金属元素A、B、C,其氢化物的化学式分别是HxA、HxB、HxC,经测定HxA在500 ℃时有1%分解,HxB在150 ℃时有10%分解,HxC在1 000 ℃时仍未分解。判断A、B、C三种元素的原子序数大小关系
A.C>A>B B.A>C>B C.B>A>C D.A>B>C
7. 下列各组顺序的排列不正确的是
A.离子半径:F->Na+>Mg2+>Al3+ B.热稳定性:HCl>H2S>PH3
C.酸性强弱:H2CO3<H3PO4<H2SO4 D.碱性强弱:NaOH>KOH>CsOH
6. 某元素R的原子的质量数为70,其核内中子数为39,它的离子有28个电子,则此元素的氧化物的化学式应为
A.RO B.R2O3 C.RO2 D.R2O5
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com